| TRATAMIENTO | CONCENTRACION DE IBA (mg L-1 por 24 h |
|
T1 *
T2 T3 T4 |
0
100 200 300 |
|
|
| (*) Tratamiento testigo. |
En Cuadro 3 se presentan los resultados obtenidos para las siguientes variables: largo total de raíces por estaca (LTR), número de raíces por estaca (NRE), número de brotes por estaca (NBE), largo total de brotes por estaca (LTB), número total de hojas por estaca (NTH) y peso fresco de la estaca (PEE).
Se encontraron diferencias para los parámetros LTR, NRE, NBE, LTB y PFE. Se puede apreciar que los mejores resultados para LTR y NRE se obtuvieron con el tratamiento de 200 mg L-1 de IBA. Esto se puede explicar debido a la presencia de la hormona en el tratamiento, que ayudó a la estimulación del número y crecimiento de las raíces. Con respecto a NBE y LTB, la mejor respuesta se obtuvo también con el tratamiento de 200 mg L-1 (T2). Para el parámetro NTH no se encontraron diferencias entre tratamientos, es decir, la aplicación de una hormona no influiría en la cantidad de hojas por estaca, ya que la planto hace uso de sus reservas para el desarrollo de las hojas, con las cuales capta fotosintatos necesarios para su sobrevivencia (Riquelme, 1995).
Las diferencias que se observaron en el peso fresco de la
estaca (PFE) se debieron al escaso enraizamiento presentado por el testigo,
siendo mayor en aquellas estacas en que se encontró un mayor número
de raíces por estaca y brotes más vigorosos.
Según Hartmann y Kester (1992), la aplicación
de una auxina para realizar propagación de plantas por estacas es aconsejable
ya que ésto podría aumentar la velocidad de enraizamiento de
las estocas. Por otro lado, Bounous et al. (1992),
indican que estacas de falso espino tratadas con 3000 mg L-1, recolectadas
tarde en junio (para el hemisferio norte), responden positivamente. Otro factor
que influye en el enraizamiento de estacas, es la temperatura del medio de
enraizamiento, ya que bajas temperaturas en el sustrato inhiben crecimiento
de las raíces (Hartmann y Kester 1992; Trunov
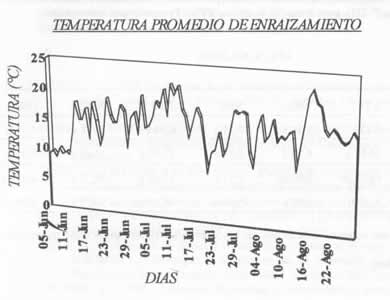
1994). En la Figura 1 se muestran temperaturas promedios
del sustrato de enraizamiento en falso espino. Se puede apreciar que la temperatura
promedio del sustrato de enraizamiento fue adecuada para él, coincidiendo
con lo que afirma Trunov (1994), en lo referente a temperatura
del sustrato de propagación para el falso espino, ya que temperaturas
entre 9°y 16°C son óptimas para un buen enraizamiento de las
estacas.
CONCLUSIONES
De los resultados obtenidos y bajo las condiciones en que
fueron realizados estos trabajos, es posible concluir lo siguiente:
Aplicaciones en dosis de 200 y 300 mg L-1 por 24 h de IBA para
la propagación de estacas de falso espino, resultan exitosas para la
propagación de este frutal, dando un muy buen desarrollo de las estacas.
Figura 1. Temperatura promedio de medio de enraizamiento en falso espino, xxx
| Cuadro 2. Número
de estacas con callos (NEC), número de estacas con raíz
(NER), número
de estacas con brotes (NEB) y número de estacas con nodulaciones
(NEN)
en Sanddorn después de 3 meses. |
| TRATAMIENTO |
NEC
|
NER
|
NEB
|
NEN
|
|
T1 *
|
7,22
|
6,87
|
10,02 a
|
1,91 a
|
|
T2
|
8,97 a
|
8,80 a
|
9,89 a
|
3,26 a
|
|
T3
|
8,90 a
|
8,20 ab
|
9,76 a
|
2,86 a
|
|
T4
|
8,34 ab
|
7,33 ab
|
10,02 a
|
1,34 a
|
| Letras iguales en cada columna indican que no hay diferencias significativas entre tratamientos (P> 0.05). |
(*) Tratamiento control. |
| Cuadro 3. Largo total de
raíces (LTR), número de raíces por estaca (NRE),
número de brotes
por estaca (NBE), largo total de brotes por estaca (LTB), número
total de
hojas por estaca (NTH), peso fresco de la estaca (PFE). Promedio por
tratamiento. |
| TRATAMIENTO |
LTR
|
NRE
|
NBE
|
LTB
|
NTH
|
PFE
|
|
T1 *
|
5,17
|
1,30 b
|
2,75 c
|
8,55 c
|
44,5 a
|
3,55 b
|
|
T2
|
16,65 a
|
4,20 a
|
2,97 a
|
17,55 a
|
55,45 a
|
5,35 a
|
|
T3
|
14,77 ab
|
3,90 ab
|
2,35 c
|
12,85 b
|
46,77 a
|
4,47 ab
|
|
T4
|
8,17 b
|
1,97 b
|
2,90 b
|
13,70 ab
|
50,27 a
|
4,00 ab
|
| Letras iguales en cada columna indican que no hay diferencias significativas entre tratamientos (P> 0.05). |
(*) Tratamiento control. |
BIBLIOGRAFIA
ABBE, E. C. 1974. Flowers and inflorescens of the Amentiferae, The botanical review 40(2): 159-161.
ARAOS, R. 1989. Injertación de hipocotilo sobre semilla germinada y de epicotilo sobre plántulas de castaño. Tesis Ing. Agr. Universidad de Chile. Santiago. 63p.
BOUNOUS, G., F BULLANO, C PEANO. 1992. Softwood cuttings of Amelanchier canadiensis, Cornus mas, Elaeagnus umbellata and Hippophae rhamnoides. Monti e boschi 43(4): 51-57. (Abstr).
BUZETA, A., F SANCHEZ, A CHAVEZ. 1995. Sanddom: un regalo de la naturaleza. Agroeconómico, Agosto- Septiembre 1995.
CORPORACION DE FOMENTO DE LA PRODUCCION. 1987. Propagación de algunas especies frutales de interés para el sur de Chile: manzano, castaño y avellano europeo. Santiago 90p.. COREO.
HARTMANN, H. Y D. KESTER. 1992. Propagación de plantas. Principios y prácticas. México, Ed. Continental.
KOCH, H. . Falso espino: una nueva variedad frutal cultivable en la República Democrática Alemana.
KONDRASHOV, V. T. 1994. New technology of creating stands of Sea Buckthom and other horticultural crops. Russian Agricultural Sciences 11: 24-28. (Abstr.).
KRYLOVA, Y. 1991. Mineral nutrition of softwood cuttings of top and soft fruit crops. Sadovodstro i Vinogradarstro 4: 16-18. (Abstr.).
MAC-CHLIS, L. and TARREY J. 1959. Plants in action. A laboratory manual of plant physiology. Freeman and Co., San Francisco.
RIQUELME, M. 1995. Evaluación de la producción de propágulos y enraizamiento de brotes de Alcachofa. Tesis Lic. en Agronomía Universidad Austral de Chile. Valdivia. 72p
SAAVEDRA, O. 1981. El castaño. En CORFO, Perspectivas para el desarrollo de frutales tipo nuez en Chile. Santiago, Chile. CORFO.
SANTAMOUR, F. 1988. Graft incompatibility related to cambial peroxidase isozymes in Chinese chestnut. Journal of Environmental Horticulture 6 (2): 33-69. (Abstr.).
SUDZUKI, F. 1983. Cultivo de frutales menores. Santiago, Ed. Universitaria.
SUDZUKI, F. 1993. Proyecto: Frutales menores: nuevas alternativas de cultivo. Universidad de Chile, Fac. de Ciencias Agrarias y Forestales. Santiago.
TRUNOV, I.1994. Effect of soil temperatura on root growth in top and small fruit crop. Sadovodstro i Vinogradarstro 5: 7-8. (Abstr.)
VIEITZ, M. y A. VIEITZ. 1981. Injerto de Hipocotilo de plántulas de castaño. Anales de edafología y Agrobiología 40 (3/4): 647-655.
VIEITZ, M. y A. VIEITZ. 1982. Observaciones sobre el injerto juvenil del castaño. Anales de Edafología y Agrobiología 41 (9/10): 1999-2002.