Daniel Alomar y Rita Fuchslocher
Universidad Austral de Chile
Facultad de Ciencias Agrarias
Instituto de Producción Animal
Casilla 567. Valdivia. Chile.
1 Proyecto FONDECYT 1961056
Recepción de originales: Julio 07 de 1997.
Fundamentals of near infrared reflectance spectroscopy as a method of forage analysis
Key words: Near infrared reflectance spectroscopy, NIRS, forage analysis.
As near infrared reflectance spectroscopy (NIRS) has evolved as arapid, precise and non-destructive global technique of analysis of agricultural products, this paper intends to review the aspects related to the physical fundamentals of NIRS, technical advances in instrumentation and the steps to develop and evalúate calibrations. Some examples of forage evaluation by NIRS are given in terms of chemical composition, digestibility, energy value and ruminal degradability, among other applications.
Ante el desarrollo experimentado por la espectroscopia de reflectancia
en el infrarrojo cercano (NIRS) a nivel mundial, como técnica rápida,
precisa y no destructiva, en su aplicación al análisis de productos
agrícolas, se revisan sus fundamentos físicos, se describen los
avances experimentados en la instrumentación y se exponen las etapas
para desarrollar y evaluar una calibración. Se entregan algunos ejemplos
del uso de NIRS en la evaluación de forrajes, en términos de composición
química, digestibilidad, valor energético y degradabilidad ruminal,
entre otras aplicaciones.
Los recursos forrajeros constituyen el fundamento de la producción en base a rumiantes. La producción de estos recursos depende de ciclos biológicos básicamente estacionales que determinan períodos deficitarios en su disponibilidad y calidad, lo que constituye un factor regulador de la productividad de los sistemas ganaderos. Por ello, la producción y la conservación de forrajes, son prácticas de gran trascendencia en el manejo de sistemas ganaderos intensivos. Dadas las condiciones de clima templado húmedo imperantes en la X Región de Chile, el ensilaje es la práctica de conservación de forrajes más recomendada en sistemas intensivos de producción (Torres, 1994). El conocimiento de la calidad de los forrajes en general y del ensilaje en particular, en forma rápida y confiable es por tanto un tema relevante para los técnicos y productores en este tipo de zonas. La preocupación por estudiar, promover y mejorar el proceso de ensilado, es un asunto recurrente en este medio (Hiriart, 1981; Alomar y Marambio, 1984; Universidad Austral de Chile, 1985; Wernli y Hargreaves, 1988; Latrille y Alomar, 1993; González, 1994). Lo mismo ocurre en países de la Unión Europea, donde la producción de leche se ha basado en forma creciente en forrajes producidos en el predio (Moss et al., 1992). Ante el desarrollo experimentado por la espectroscopia de reflectancia en el infrarrojo cercano (NIRS), como método de análisis de productos agrícolas en general, el objetivo de este trabajo es el de aportar antecedentes acerca de los fundamentos y la aplicación de esta técnica, como método de predicción de la composición nutricional de forrajes y otros recursos.
Existen numerosos trabajos en que se describen o evalúan técnicas para estimar la composición nutricional de forrajes (Givens, 1986; Givens et al, 1989; Givens, 1993; Thomas y Thomas, 1985; Dumont, 1994; Hiriart, 1994). Las principales limitaciones de estas técnicas, especialmente aquellas referidas a la valoración energética, es que son muy lentas, como ocurre con los métodos de digestibilidad in vitro, ya sea con licor ruininal (Tilley y Terry, 1963) o enzimáticos (Jones y Hayward, 1975; Dowman y Collins, 1982), o son debajo valor predictivo, como los métodos basados en el contenido de fibra. Los métodos in vitro en general, permiten una mejor predicción de la digestibilidad, o de entes asociados a ella, como el "valor D" (materia orgánica digestible como porcentaje de la materia seca), que a su vez sería un buen estimador del contenido de EM. Sin embar-go, estos métodos dificultan el realizar análisis masivos, debido a su lentitud. Por otra parte, los métodos basados en la determinación de fracciones fibrosas, poseen como ventaja su relativa sencillez y rapidez, por lo que se han utilizado extensivamente para estimar valores energéticos. Como ejemplo, Hirsh-Reinshagen (1992) en una tabla de composición de alimentos para las zonas centro y centro-sur de Chile, entrega valores para numerosos recursos forrajeros, incluyendo subproductos industriales, en que el contenido de energía metabolizable (EM) y energía neta de lactación (Enl) se calculan a partir de su contenido de fibra cruda. Según la misma publicación, las regresiones empleadas (generadas en el extranjero) tendrían un R=0,60, lo cual representa un valor predictivo de conflabilidad discutible. En el Reino Unido se utiliza la predicción del contenido de EM a partir del contenido de fibra detergente ácido modificada o MADF (Clancey y Wilson, citados por Givens et al, 1989) que permite dar masivos servicios de análisis a los productores, en forma rápida y a un costo razonable. Este método se usa también en Chile con el mismo propósito (Hiriart, 1994). Sin embargo, su validez ha sido cuestionada por Givens et al, (1989) quienes compararon varios métodos de predicción del contenido de EM in vivo paramás de l00 ensilajes, concluyendo que MADF era el peor predictor, ya sea tomado en forma aislada o combinado con otras técnicas.
NIRS
Desde la década del setenta se perfila a nivel mundial la espectroscopia de reflectancia cercana al infrarrojo (NIRS), como una técnica alternativa a los métodos químicos y químico-biológicos tradicionales, con muy buen potencial para obtener estimaciones seguras y muy rápidas de la composición química nutricional de forrajes (Givens, 1993; De la Roza, 1993), así como de otros productos de muy diversa índole. Esta es una técnica no destructiva, rápida, de gran precisión y exactitud, siempre que se sigan los procedimientos adecuados para generar las ecuaciones de predicción requeridas (Marten et al., 1989; Murray, 1993; Garrido et al, 1993). En los últimos años se han desarrollado numerosas aplicaciones para evaluar composición, monitorear procesamiento y certificar calidad de alimentos, tanto para animales, como para la población hu-mana y todo hace suponer que las aplicaciones aumentarán (Givens et al 1997).
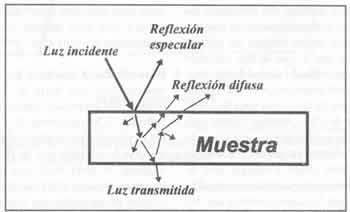
Bases físicas. Cuando la luz incide sobre una muestra (Li), una piule de los fotones puede transmitirse a través de la muestra (Lt) y el resto es reflejado (Lr), o absorbido (La) por algunos enlaces covalentes que actúan como resortes oscilantes que se acoplan con la frecuencia (cm-1) o longitud de onda (nm) exacta de la radiación lumínica (Murray, 1993). Al absorber energía, los enlaces de las moléculas vibran en dos formas fundamentales: se extienden, aumentando la distancia interatómica a lo largo del eje entre dos átomos (lo que ocurre a frecuencias más altas o menor longitud de onda); o se doblan (a frecuencias más bajas o mayor longitud de onda), cambiando el ángulo de enlace entre dos átomos (Workman, 1996). Las vibraciones de extensión pueden ser simétricas o asimétricas y aquellas que producen pliegues, los pueden ocasionar dentro del plano, como movimiento de tijera y oscilaciones; o fuera de éste, en forma de coleteos y torcedoras (Shenk y Westerhaus, 1995). La vibración resultante se disipa, provocando un mero calentamiento de la muestra. La absorción es selectiva y depende de los grupos moleculares involucrados. Así, la absorción de luz se estima por diferencia entre la luz incidente y la reflejada o transmitida. Cuando se trabaja en el modo de reflexión, se utiliza una muestra lo suficientemente opaca para que la transmisión (Lt) sea igual a cero, calculándose la absorción de luz por diferencia: La = Li - Lr, (Murray, 1993).
En el modo de transmisión, se define absorbancia (A), como log 1/T, en tanto que en el modo de reflexión, A corresponde al log 1/R. Se asume que ambos casos obedecen a la ley de Beer-Lambert, que establece que la absorbancia a cualquier longitud de onda, es proporcional al número o concentración de moléculas absorbentes presentes en el camino recorrido por la radiación (Murray, 1993).
En términos más rigurosos, la energía total reflejada por una muestra, es la suma de la reflexión especular (superficial o en forma de espejo) más la reflexión difusa, que es aquella temporalmente absorbida y luego re-emitida por la muestra (Figura 1). Sólo esta última forma (reflexión difusa) entrega información útil acerca de la naturaleza o composición de lamuestra (Davies y Grant, 1987), lo que pone de manifiesto el problema de dispersión de luz, que afecta a la reflexión difusa y que depende del tamaño de partícula de la muestra. Esto complica el análisis NIRS, especialmente en reflexión, en que no se controla el camino recorrido por la luz debido a la dispersión y hace indispensable el uso de un computador (Murray, 1993).
Figura 1. Interacción de la luz con la materia.
Interaction of light with matter.
Las bandas de absorción en la región NIR del espectro electromagnético (700-2.500 nm), están relacionados a las de la región infrarroja (2.500-25.000 nm), donde se producen las bandas de absorción fundamentales por la vibración de los átomos en las moléculas constituyentes. Las bandas de absorción en NIR corresponden a "ecos" o "rebotes" deesas absorciones fundamentales, consistentes en sobretonos armónicos de las bandas fundamentales de absorción y sus combinaciones, aproximadamente a un medio o un tercio de la longitud de onda en que ellas ocurren (Coleman y Murray, 1993; Davies y Grant, 1987; Barton, 1989). Esto determina que para una muestra de naturaleza química heterogénea, o con numerosos componentes químicos, como sería un forraje, el espectro obtenido en la región NIR, será una compleja combinación de bandas o picos de absorción parciales sobrepuestos o muy cercanos, que suelen confundirse en una línea suavizada en que se encuentran picos, valles y curvaturas en forma de hombros y que sólo cobran sentido cuando dicha información se puede interpretar con la ayuda de un computador.
En su aplicación al análisis de forrajes y otros compuestos, la técnica se basa entonces en que el espectro lumínico cercano al infrarrojo puede proporcionar información acerca de los principales elementos estructurales asociados a los organismos vivos, ya que los grupos funcionales que responden a laradiación en este espectro son C-H, O-H, N-H y probablemente S-H y C=O (Davies y Grant, 1987; Shenk y Westerhaus, 1993). Así, los principales componentes del tejido vegetal, que consisten en combinaciones muy diversas de llos grupos citados, tienen por lo mismo, propiedades de absorción en esta piule del espectro, es decir, entre los 800 y 2500 nm (Barton, 1989), que pueden usarse para diferenciar un componente de otro (Norris, 1989). En el Cuadro 1, se presentan las bandas de absorción de los principales componentes orgánicos en los alimentos y los enlaces tentativos que los representan.
| Cuadro 1. Bandas de absorción de enlaces químicos en
la región NIRS. Absorption bands of chemical bonds in NIR región. |
|
|
||
|
Longitud de
onda (nm) |
Constituyentes
|
Enlace asignado
|
|
|
||
|
1200
1440 1730 1780 1940 1980 2080 2180 2320 2350 |
Lípidos
Agua y Carbohidratos Lípidos Lípidos Agua Proteínas Carbohidratos Proteínas Lípidos Lípidos |
C-H |
|
|
||
| (Davies y Grant, 1987). | ||
Una ventaja de trabajar en la región NIR del espectro, consiste en que al utilizar longitudes de onda menores (en relación al infrarrojo medio, o MIR), la penetración de la radiación es mayor, debido a que el grado de absorción es más débil con cada armónico sucesivo, en comparación con la banda de absorción fundamental en el sector MIR. Esto determina que es posible analizar por reflectancia una muestra sólida de mayor grosor, obteniendo información más representativa y al mismo tiempo/es posible trabajar en modo transmisión (o transmitancia) en muestras húmedas heterogéneas bastante más gruesas y con más facilidad de manejo que en la región MIR (Murray, 1993).
Avances. Desde las primeras incursiones en el uso de esta técnica en la valoración de forrajes, en que se llegó a predecir la composición, digestibilidad y hasta el consumo voluntario potencial de los animales (Norris et al, 1976), el avance ha sido tal, que al comparar diversas técnicas de laboratorio de uso común para predecir la digestibilidad de más de 150 ensilajes evaluados in vivo, en Gran Bretaña, Barber et al., (1990) concluyeron que NIRS es la mejor técnica disponible en la actualidad en términos de precisión y exactitud, siempre que se cuente con calibraciones apropiadas.
Los principales adelantos que explican el éxito de esta técnica, están en las áreas de diseño de los equipos (filtros fijos, filtros incunables y monocromadores) y del software desarrollado e incorporado por las compañías especializadas, el que, junto a la posibilidad de contar hoy con computadores personales de alto poder, permite utilizar la información espectral y química, para generar, evaluar y aplicar, mejores ecuaciones de calibración. De este modo, los programas disponibles pueden seleccionar según su espectro a las muestras más apropiadas para el desarrollo de una calibración y pueden también identificar en la fase de calibración y en la posterior de análisis de rutina, a aquellas muestras que, por sus características espectrales, no corresponden al mismo tipo de producto, marcándolas como muestras extrañas, aberrantes o "outliers" (Garrido et al., 1993). La ventaja de esto último es que permite ya sea descartar la muestra por pertenecer a otro tipo de sustancia, o incorporarla a la calibración enriqueciendo su cobertura y mejorando su valor predictivo.
Instrumentos de filtros fijos o de interferencia.
Se basan en el uso de filtros especiales que al ser iluminados por la fuente
emisora, sólo dejan pasar una longitud de onda. Al disponer de varios
filtros que al desplazarse se interpongan en el camino seguido por la radiación,
se pueden generar distintas longitudes de onda para irradiar la muestra (Figura
2).
Figura 2. Diseño de un equipo NIRS de filtros fijos.
Design of a NIRS equipment with fixed filters.
Estos equipos de filtros de interferencia, llevan entre 6 y 20 filtros montados en un dispositivo (rueda o tórrela) que permite cambiar fácilmente la posición y generar una longitud de onda específica. Son equipos útiles para análisis de rutina de sustancias poco complejas. Uno de los primeros equipos de este tipo que se comercializó, corresponde a una analizador de granos, dotado de 6 filtros, para la medición de agua (1940 nm), carbohidratos ( 2100 nm), proteína (2180 nm) y aceite (2310 nm). Además se incluían dos filtros con mínima absorción para esos constituyentes (1680 y 2230 nm), los que servían como referencia (Norris, 1989).
Instrumentos de filtros incunables. Estos poseen varios filtros, típicamente 3 en los más simples y hasta 7 en los más complejos, los que se montan en un eje que al girar provoca una inclinación del filtro, cambiando el ángulo de la luz incidente sobre él, lo que cambia la longitud de onda que pasa a través (Figura 3). Con esto se pueden obtener muchas longitudes de onda, considerando al conjunto de filtros (Clark et al, 1991).
Figura 3. Diseño de un equipo NIRS de filtros incunables.
Design of a NIRS equipment with tilting filters.
Los intrumentos de filtros incunables se pueden usar igual que los de filtros fijos, para generar longitudes de onda fijas, o como espectrofotómetros de barrido, con un rango limitado de longitudes de onda (Norris, 1989). Davies y Grant (1987) citan como ejemplo un equipo de filtros incunables con 7 filtros, que puede generar un rango de barrido continuo entre 1380 y 2380 nm.
Monocromadores de barrido. Utilizan el mis-mo concepto del modelo de filtros incunables, sin embargo, en lugar de usar filtros, utilizan una especie de prisma (red de difracción) que provoca dispersión de la luz, generando diferentes longitudes de onda (Clark et al., 1991). Uno de los modelos más avanzados que se encuentra hoy en día, permite irradiar las muestras en el rango de 400 a2.500 nm, es decir, desde el espectro visible, hasta el final del NIR (ISI, 1992). Estos equipos, por su versatilidad, permiten amplias perspectivas de desarrollo de nuevas aplicaciones, siendo la alternativa más apropiada para centros de investigación. Son también los más costosos y eso indudablemente constituye una seria limitación, ya que su costo normalmente excede el límite que financian algunas agencias de apoyo a la investigación.
Con respecto a las marcas de equipos disponibles en el mercado, existen diversas marcas y compañías fabricantes de equipos NIRS, aunque a través de los años varias han cambiado de nombre y propiedad, concentrándose ésta en po-cas compañías. Entre las marcas más conocidas están NIRSystems (ex Pacific Scientific, USA), Tecator (Suecia), Bran+Luebbe (ex Technicon, Alemania) y Perten (Suecia). Las dos primeras son fabricadas por la compañía Perstorp Analytical, originalmente del grupo Perstorp de Suecia, pero que ha sido adquirida por Foss Electric, de Dinamarca. El boletín NIRnews de abril de 1997, publicado por The International Cominee for Near Infrared Spectroscopy, con sede in Inglaterra, informa de una docena de compañías que están ofreciendo nuevos productos en la línea NIRS, incluyendo espectroscopios y accesorios para la presentación y el manejo de muestras, con ocasión de la conferencia internacional de EEUU sobre química analítica y espectroscopia aplicada (PittCon-97).
Colección de los espectros. Existen diferentes estrategias de diseño para colectar los espectros o presentar las muestras al respectivo instrumento. Algunos equipos disponen de una cavidad donde se introduce la muestra, la que se presiona contra una ventana de vidrio o cuarzo (Davies y Grant, 1987). Otros disponen de celdas o cubetas removibles que se insertan con la muestra en su interior. Los primeros equipos disponían de pequeñas celdas que se leían en posición fija, lo que limitaba la superficie de barrido y arrojaba un grado importante de error, especialmente en muestras heterogéneas, como son los forrajes (Abrams et al., 1988). Hoy se dispone de accesorios más apropiados para evaluar este tipo de producto, incluso al estado fresco, con mayor superficie de barrido, reduciendo el error de valoración espectral (Murray, 1993). El elevado costo de éstos y otros componentes, sin embargo, continúa siendo un obstáculo para su uso masivo.
Entre las opciones disponibles, hay celdas con una ventana de cuarzo, apropiadas para muestras secas y relativamente homogéneas; cubetas rectangulares de mayor superficie, para muestras fibrosas (forrajes) y más heterogéneas (forrajes, carnes). También se dispone de cubetas de cuarzo con doble ventana, para muestras líquidas, o pastosas, para trabajar en el modo de transmisión. Estas celdas o cubetas se insertan en un módulo específico que, adosado al instrumento, permite irradiar la muestra dentro de su celda, la que, según el diseño del instrumento, puede estar fija, girar, o desplazarse en forma rectilínea, para aumentar la superficie de barrido y permitir así un mayor número de lecturas por muestra, las que se promedian. Existen también accesorios que permiten tomar lecturas espectrales por medio de sondas provistas de fibra óptica, apropiadas para trabajar en reflectancia o transmitancia, que pueden ser utilizados en diferentes aplicaciones. Los espectros de muestras sólidas se colectan por reflectancia, en tanto que los de muestras líquidas, por transmitancia. Los ensilajes al estado fresco, se pueden leer por reflectancia, si se pone una capa lo suficientemente gruesa en una cubeta apropiada, que no permita que la luz la atraviese totalmente (Murray, 1993).
Una vez que se irradia la muestra, la luz difusa reflejada (R) por la muestra, es registrada por detectores, normalmente de sulfuro de plomo, amplificada, digitalizada, transformada en log 1/R y comunicada a un computador para su almacenamiento o procesamiento. En forma pareada a la señal digital de luz reflejada, el computador recibe una señal que representa la longitud de onda utilizada, de modo que a cada valor de reflectancia almacenado, le corresponde una longitud de onda, lo que permite el ulterior procesamiento de los datos (Norris, 1989a). El conjunto de valores a diferentes longitudes de onda para una muestra dada, constituye su espectro, que representa una suerte de "huella dactilar" de esa muestra. En la Figura 4 se presenta un conjunto de 150 espectros de ensilajes de pradera de la zona sur de Chile (IX y X Regiones) que representan una amplia cobertura en términos de calidad nutricional y rasgos espectrales (Alomar y Fuchslocher, no publicado).
Figura 4, Colección de 150 espectros de ensilajes
de pradera.
A collection of 150 spectra of pasture silage.
Manejo de datos espectrales. Los datos de reflectancia (R), en la forma de log 1/R, se pueden someter a transformaciones y, aunque los instrumentos basados en filtros sólo pueden utilizar la forma logarítmica, hoy es común la transformación del espectro obtenido con monocromadores de barrido, lo que permite reducir el efecto de tamaño de partícula de la muestra, destacar rasgos del espectro y facilitar el análisis de regresión. La transformación sirve entonces a dos objetivos básicos: Reducir el "ruido" en los datos y aislar o destacar la información espectral que se pueda relacionar con los datos químicos (Westerhaus, 1989a).
El tratamiento más común corresponde al cálculo de una primera o segunda diferenciación o pseudoderivada (Figura 5) que aunque también se denomina derivada, en realidad corresponde a una diferencia entre segmentos del espectro, que previamente se han suavizado o promediado (Murray, 1988, Davies y Grant, 1987). Se puede calcular una segunda diferenciación (u otra de mayor orden), repitiendo el proceso en un espectro previamente derivalizado y este nivel de transformación ha dado buenos resultados en forrajes (Barton, 1989).
Otros tratamientos permiten eliminar "ruido" en los valores espectrales, a través de suavización de los datos, como es la transformación de Fourier (Davies y Grant, 1987). Se dispone de software específico para éstas y otras transformaciones, dependiendo del tipo de instrumento a utilizar. Un ejemplo de tratamiento de datos sería: 1-10-5. El primer número indica el orden de derivación o diferenciación, el segundo es la amplitud o distancia entre los segmentos a sustraer y el tercero la longitud del segmento (puntos de datos) a ser suavizado (Dardenne et al, 1996). En la Figura 5 se muestran los mismos 150 ensilajes de la Figura 4, pero sometidos a un tratamiento 1-10-10 (Alomar y Fuchslocher, no publicado). Se aprecia una notable reducción de variación de línea base entre ensilajes.
No existe una regla fíja en cuanto al tratamiento matemático más conveniente de los datos, sino que esto dependerá de la calidad de la calibración obtenida, luego de probar diferentes combinaciones (ISI, 1992). Como ejemplo de esto, Dardenne et al, (1996) en la aplicación de NIRS al análisis de muestras de alfalfa fresca, describen la aplicación de 60 tratamientos matemáticos a los datos espectrales, previamente a someterlas al análisis de regresión o desarrollo de la calibración propiamente tal. Trabajando con forrajes frescos, estos autores encontraron que el elevado contenido de agua causa fuertes bandas de absorción y sólo una segunda derivación con una gran amplitud (tratamiento: 2,20,5) es eficiente para mejorar el modelo de predicción.
Figura 5. Espectros de 150 ensilajes de pradera con una primera
diferenciación.
Spectra of 150 pasture silage after a first differentiation.
Desarrollo de calibraciones. Para estimar la composición química de una muestra, se requiere previamente hacer calibraciones, para lo cual se necesita contar con un conjunto amplio de muestras representativas de una misma población, colectar sus espectros, analizar las muestras mediante un método de referencia confiable, desarrollar las ecuaciones de calibración que relacionen los datos espectrales con los resultados del método de referencia y, finalmente, validar dichas ecuaciones con otras muestras de la misma población general, pero que no formen parte del set de calibración (Gabrielsen et al, 1988; Barber et al., 1990; Garrido et al, 1993).
Según Murray (1988), el set de muestras
se-leccionadas para desarrollar una calibración debe cumplir ciertas
condiciones ideales:
• representar un rango amplio de composiciones o calidades;
• tener una distribución uniforme y pareja (no normal) respecto
de la población total;
• ser típicas de las que se encuentren en la realidad, y
• contarse con datos precisos de su composición analítica.
Las ecuaciones de calibración tienden a tener mejor valor predictivo cuando se desarrollan sobre muestras de naturaleza relativamente homogénea o correspondientes a un mismo tipo de producto (ej., henos de alfalfa). En cambio, cuando se intenta desarrollar calibraciones para poblaciones más heterogéneas de base más amplia (ej. pajas, henos y ensilajes de distintas especies vegetales en conjunto), la precisión y exactitud tienden a disminuir. Un ejemplo lo entrega Reeves (1994), quien trató de evaluar mediante NIRS, muestras de 18 alimentos diferentes, que incluían henos de gramíneas, leguminosas y mixtos; pajas, corontas de maíz, cascaras de maní, soya y arroz. Todo ello, combinado con diferentes tratamientos químicos. En estas condiciones, el uso de NIRS no fue satisfactorio, a pesar de que las predicciones mejoraron algo al eliminar muestras marcadas como extrañas o aberrantes por el software respectivo. Por ello, es importante establecer los límites apropiados de compromiso entre la amplitud de cobertura y el error de las predicciones.
Uno de los primeros aspectos que se plantean al desarrollar una calibración, es el número de muestras que será necesario incluir para obtener resultados satisfactorios. No existe un número mínimo definido, sino que éste dependerá de la entidad a predecir y de la naturaleza del producto a evaluar. Cuando se pretende analizar entidades químicas simples, de productos relativamente homogéneos, como es el nivel de nitrógeno (para estimar proteína bruta) en granos de trigo, puede bastar con 30 a 40 muestras; en cambio, si se pretende evaluar el contenido de proteína en productos más heterogéneos, o productos con mayores niveles y variedad de proteínas, se requieren más de 100 muestras (Shenky Westerhaus, 1993). En este sentido, Murray (1993) indica que es poco probable obtener calibraciones robustas en su uso rutinario para analizar forrajes, si se cuenta con menos de 100 muestras, excepto cuando se utilizan para predecir componentes simples como el contenido de humedad y nitrógeno.
Otro aspecto a destacar, es la posibilidad de transferir calibraciones
desarrolladas desde un equipo a otro. Dado que los aparatos presentan variaciones
en sus lecturas, provenientes del mecanismo óptico, fuente emisora de
luz, sustancias de referencia interna y en los detectores, es necesario estandarizarlos
para corregir estas desviaciones. Ello es posible a través del uso de
software especializado (Shenk y Westerhaus, 1991). Aun-que
esto abre interesantes posibilidades, se puede usar una calibración "importada",
siempre que se trate del mismo tipo de muestras, ya que no se debe extrapolar
en NIRS. Además, obliga a utilizar los mismos métodos de referencia
y la misma manera de presentar la muestra a la lectura, en la operación
de rutina posterior. Esto puede constituir una seria limitación para
transferir ecuaciones de un lugar a otro, debido a diferencias entre laboratorios
en la forma de preparar las muestras y conducir los métodos analíticos.
Parece interesante entonces, desarrollar ecuaciones de calibración de
valor local y al mismo tiempo, estudiar el comportamiento de calibraciones externas.
Cálculo de ecuaciones. Al desarrollar una cali-bración,
se relaciona la información espectral con la información de referencia
(composición quí-mica), definiendo entre otras cosas, el tratamiento
matemático de los datos, el segmento del espectro a incluir y el método
de regresión a emplear. Existen valias alternativas para modelar la relación
entre los datos espectrales y los datos de referencia. Para esto se utiliza
el análisis de regresión y entre las técnicas disponibles
están la regresión múltiple, regresión múltiple
paso a paso, componentes principales y cuadrados mínimos parciales. En
general se encuentran mejores resultados con las últimas dos técnicas,
en que se reduce toda la información espectral a un grupo más
pequeño de variables independientes (componentes principales) y al mismo
tiempo se controla el riesgo de sobreajuste (ISI, 1992). El
uso de redes neuronales es otra técnica que se perfila con gran potencial,
ya que es capaz de resolver relaciones no lineales en los datos espectrales,
lo que mejora la exactitud (Shenk y Westerhaus, 1995).
Debe tenerse presente que una buena correlación entre los datos espectrales y los de referencia, puede ser el resultado de un sobreajuste de los datos, cuando se cuenta con pocas muestras (menos de 50) y se incorporan demasiados términos a la ecuación. Si eso ocurre, la ecuación será de validez para esos datos o muestras en particular, pero probablemente se comportará pobremente al probarla en un set de muestras de validación, en una población abierta (Murray, 1993).
Dentro del software disponible para desarrollar calibraciones, destaca el elaborado por Infrasoft International, que permite realizar una validación cruzada con las muestras empleadas en la calibración. Este proceso consiste en subdi-vidir el grupo de muestras en varios subgrupos, separando uno como si fuera un grupo de muestras "externas" para validación y generando con el resto una ecuación de calibración. Este proceso se repite hasta que todos los grupos de muestras han sido predichos a partir de los restantes, lo cual permite una mayor confiabilidad en la ecuación generada, ya que limita automáticamente el número de términos en la ecuación, evitando el sobreajuste (ISI, 1.992).
Criterios de selección de ecuaciones. Las diferentes opciones de tratamientos matemáticos y técnicas de regresión permitirán disponer de muchas ecuaciones posibles para cada una de las variables a predecir. Es necesario entonces seleccionar aquella que se considere más confiable, es decir, que tenga un elevado coeficiente de determinación (R2) y un bajo error estándar de calibración (SEC).
El SEC corresponde en general al error estándar de la diferencia (ISI, 1992) y, aunque no tiene una forma de expresión umversalmente empleada, al parecer la más aceptada (Davies y Grant, 1987; Murray, 1993; ISI, 1992) es:
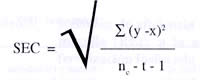
donde:
y = es el valor de referencia (laboratorio).
x = Valor predicho por NIRS.
nc = Número de muestras en el set de calibración.
t = Número de términos en la ecuación de regresión.
Una vez seleccionada una o más ecuaciones, deben someterse a prueba con una muestra inde-pendiente de validación, que no debe formar parte del grupo de calibración. Como situación intermedia, el software de ISI, que incluye la validación cruzada de las muestras de calibración, entrega un error estándar de validación cruzada. Al predecir un set de muestras externas para validación, se calcula también un R2 y, con los desvíos de los valores predichos respecto de los valores de referencia, se calcula un error estándar de predicción, o performance, (SEP) que en gene-ral se acepta como:
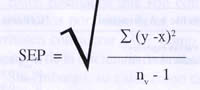
donde:
y, x = igual que en SEC
nv = número de muestras en el set de validación.
El SEP es un indicador confiable de la calidad de la ecuación desarrollada, ya que a diferencia del SEC, que mejora (disminuye) a medida que se le agregan nuevos términos a la ecuación, el SEP mejora sólo hasta que comienza a producirse un sobreajuste de la ecuación, aumentando (empeorando) posteriormente con cada nuevo término (Westerhaus, 1989b).
El SEP siempre será algo mayor que el SEC, pero como criterio general, se puede afirmar que una ecuación es considerada como aceptable cuando la magnitud del SEP es menor a un tercio de la desviación estándar de los datos de referencia (Kennedy et al, 1996).
Muestras extrañas o outliers. En el desarrollo de una ecuación, una de las primeras fases a atender, es detectar muestras que se consideren extrañas o aberrantes (en inglés referidas como "outliers"), que no encajan o no corresponden a la calibración. Para clasificar una muestra como extraña, se usan dos criterios. Uno es el residual (desvío) entre el valor de predicción (NIRS) y el de referencia (laboratorio), para cada muestra. El software disponible calcula un término t, que equivale a la relación entre el valor residual (desvío) y el SEC para el grupo. El valor t límite es definido arbitrariamente, pero frecuentemente se utiliza un valor de 2,5 por defecto (Murray, 1993; ISI, 1992). El otro criterio estadístico para caracterizar, ahora desde el punto de vista de sus valores espectrales a una muestra, es el valor H, calculado mediante técnicas de análisis multivariado a través de componentes principales, y que corresponde a lo que en estadísticas se conoce como la distancia de Mahalanobis (Murray, 1993). Este valor permite por tanto, discriminar si una muestra forma o no paite del grupo de calibración a través de su distancia al valor espectral promedio. Dado que cada grupo puede tener diferencias, se usa un valor H estandarizado, al dividir por el valor espectral promedio del set de calibración. Frecuentemente se establece un valor límite 3,0 y muestras con valor H estandarizado mayores, se consideran aberrantes (ISI, 1992).
Cuadro2. Aplicaciones de NIRS alanálisis de forrajes
y estimadores de su eficiencia predictiva.
NIRS applications to forage analysis and estimators of prediction efficiency.

R2cal: Coeficiente de determinación de la calibración: R2pred: Coeficiente de determinación para la validación; SEC: Error estándar de calibración; SEP: Error estándar de predicción (Validación); SEValid.Cruz: Error estándar de validación cruzada; Prom: Promedio datos de referencia ± desviación.
Cuando aparecen outliers t, es recomendable repetir el análisis de referencia y si repetido éste permanece como muestra discriminada, eliminarse de la calibración. Si los outliers H representan muestras que se considera que deben estar en la calibración, pueden retenerse. Una alternativa es acumular más muestras de éstas y agregarlas al sel de calibración para ampliarlo. Si el nuevo modelo no mejora el ajuste para las muestras aberrantes, éstas deberían separarse para intentar conformar con ellas una calibración diferente (Shenk y Westerhaus, 1993).
Aplicaciones. Por la diversidad de trabajos encontrados en la literatura especializala.Casì se podria decir que las aplicaciones limitan con la imaginacion. En el cuadro2 se entraga un listado parcial de ejemplos de uso de NIRS en valoracion de forrajes.
En algunas experiencias no se han logrado predicciones seguras de ciertas fracciones analíticas (coeficientes de determinación bajos o variables y términos de error elevados). Entre ellas se encuentran fracciones fibrosas (Valdés et al., 1985) como la fibra detergente neutro (FDN) y fibra detergente ácido (EDA), (Goering y Van Soest, 1970). Debe tenerse presente sin embargo, que es probable que los datos espectrales obtenidos en NIRS representen con mayor exactitud la estructura química real de la muestra, que entes determinados por "química húmeda" como la fibra cruda, FDN, EDA, etc., que no corresponden a entidades moleculares definidas (Abrams et al., 1987) sino más bien a determinaciones empíricas que, por tanto, no permiten definir los reales grupos químicos involucrados (Barnes y Marten, 1979).
Los métodos químicos utilizados como referencia para desarrollar las calibraciones, están sujetos a errores y variaciones que pueden ser mayores que los datos espectrales. Como ejemplo puede citarse que el contenido de humedad y por consiguiente el contenido de materia seca, habitualmente se estima mediante secado de las muestras a 105° C. A esa temperatura ocurre pérdida de algunos compuestos, obteniéndose más bien una suerte de "humedad bruta" (Garrido et al, 1993). Tal es el caso del ensilaje, en que hay pérdida de alcoholes y otros compuestos volátiles. Por otra parte, en la preparación de la muestra para propósitos analíticos, debe tenerse presente que el calor excesivo en el proceso de secado, puede producir "artefactos" indigestibles. Por esto, si se desea mantener la integridad estructural y química de las muestras, el método más recomendable de secado sería el de liofilización (Coleman y Windham, 1989) o alternativamente, analizarlas muestras directamente al estado fresco. Deinum y Maassen (1994) demostraron que las condiciones de secado (tiempo, temperatura) y manejo previo (congelación) de muestras, pueden afectar la determinación de paredes celulares en varios forrajes, debido a formación de productos de Maillard y desnaturación de proteínas que pierden solubilidad en detergente neutro.
Entre las aplicaciones estudiadas para productos agropecuarias diferentes a los forrajes, se puede citar, aparte de las ya mencionadas, la predicción del nivel de nitrógeno y proteína degradable ruminal en poroto soya (Tremblay et al., 1996), proteína, aceite y humedad en poroto soya intacto (Takahashi et al., 1996), proteína y Usina en granos de higo y cebada (Williams et al., 1984), calidad cervecera de cebada (Li et al., 1996), contenido de proteína y fracciones proteicas de leche de oveja (Pascual y Molina, 1996), composición y parámetros de calidad en peces (Solsberg, 1996), propiedades sensoriales en carne bovina (Hildrum et al, 1995), distintas fracciones en la carne de conejo (Masoero et al., 1994) y calidad del tejido adiposo de jamones de cerdo (Bellati et al., 1996).
El uso de NIRS se proyecta también al análisis cualitativo, que permite diferenciar sustancias parecidas, pero con diferentes grupos funcionales, a través de análisis discriminante (Downey, 1994). Esto abre un importante campo de aplicación en el control de calidad a nivel agropecuario e industrial. Entre las aplicaciones novedosas que se han reportado en esta línea, está la predicción (con un 97% de exactitud) del sexo de larvas vivas de gusanos de seda, así como larvas muertas, mientras aún se encuentran dentro de sus capullos (Jin et al., 1995).
ABRAMS,S.M., J.S.SHENK y H.W.HARPSTER. 1988. Potential of Near Infrared Reñectance Spectroscopy for Analysis of Silage Composition. J. Dairy Sci. 71:1955-1959.
ABRAMS,S.M., J.S.SHENK, M.O.WESTERHAUS y F.E.BARTON. 1987. Determination of Forage Quality by Near Infrared Reflectance Spectroscopy: Efficacy of Broad-Based Calibration Equations. J. Dairy Sci. 70:806-813.
ALOMAR, D. y J. MARAMBIO. 1984. Premarchitamiento y ácido fónnico en ensilajes de praderas: Calidad fermentativa. Agro Sur, 12:178-180.
ALOMAR, D. y R. FUCHSLOCHER. 1996. Aplicación de la espectroscopia de reflectancia en el infrarrojo cercano (NIRS o ERIC) al análisis de ensilajes de pradera. Libro de Resúmenes, XXI Reunión Anual SOCHIPA, Coyhaique, Pp: 147-148.
BAKER, C.W.; D.I. GIVENS y E.R. DEAVILLE. 1994. Prediction of organic matter digestibility in vivo of grass silage by near infrared reflectance Spectroscopy: effect of calibration method, residual moisture andparticle size. Anim. Feed Sci. and Technol., 50:17-26.
BARBER,G.D., D.I.GIVENS, M.S.KRIDIS, N.W.OFFER y I.MURRAY. 1990. Prediction of the Organic Matter Digestibility of Grass Silage. Anim. Feed Sci. and Technol. 28:115-128.
BARNES, R.F. y G.C. MARTEN. 1979. Recent developments in predicting forage quality. J. Anim. Sci., 48:1554-1560
BARTON II, F.E. 1989. Spectra. En: MARTEN, G.C., J.S.SHENK and F.E.BARTON II (editors). 1989. Near Infrared Reflectance Spectroscopy (NIRS): Analysis of Forage Quality. U.S. Department of Agriculture, Agriculture Handbook No.643 (revised with supplements), pp:30-32.
BARTON II, F.E. y W. WINDHAM. 1988. Determination of Acid-Detergent Fiber and Crude Protein in Forages by Near Infrared Reflectance Spectroscopy: Collaborative Study. J. Assoc. Off. Anal. Chem., 71:1162-1167.
BELLATTI, M.; G. PEZZANI, M. REVERBERI y R. VOLTA. 1996. Rapid method for estimating tlie quality of adipose tissue in green pig hams. Rivista di Suinicoltura, 37:69-72 (Qrig. No consultado).
BEYER, E. 1997. Dinámica de degradación ruminal de la materia seca de ensilajes y su predicción por espectroscopia de reflectancia en el infrarrojo cercano (NIRS). Tesis Licenciado en Agronomía, Facultad Ciencias Agrarias, Universidad Austral de Chile, Valdivia, 118 p.
CLARK, D., M. WINSRIG y E. HOWERY. 1991. Basics of near infrared reflectance Spectroscopy. In: National Forage Testing Association; Forage Analysis Workshop, May 1991, Milwaukee, Wi. Pp: 18-37.
COLEMAN, S. W. y I. MURRAY. 1993. The use of near-infrared reflectance spectroscopy to define nutrient digestion of hay by cattle. Animal Feed Sci. and Technology, 44:237-249.
COLEMAN, S.W. y W.R.WINDHAM. 1989. In Vivo and In Vitro Measurements of Forage Quality .En: MARTEN, G.C., J.S.SHENKand F.E.BARTONII (editors). 1989. Near Infrared Reflectance Spectroscopy (NIRS): Analysis of Forage Quality. U.S. Department of Agriculture, Agriculture Handbook No.643 (revised with supplements), pp:83-95.
DARDENNE, P., R. AGNEESSENS y G. SINNAEVE.
1996. Fresh forage analysis by near infrared Spectroscopy. In: A.M.C. Davies
y P. Williams (Eds.), Near Infrared Spectroscopy: The Future Waves. Proceedings
of the 7th International
Conference on Near Infrared Spectroscopy, Montreal, Canada, 6-11 August 1995.
NIR Publications, Chichester, UK, pp:531-536.
DAVIES, A.M. y A. GRANT. 1987. Review: Near infra-red analysis of food. Int. J. Food Sci. Technol, 22:191-207.
DE BOEVER, J.L.; J. VAN WAES, B.G. COTTYN y CH.V. BOUCQUE. 1994. The prediction of forage maize digestibility by near infrared reflection spectroscopy. Netherlands Journal of Agricultural Sciences, 42(2): 105-113.
DE LA ROZA, B. 1993. Uso de la técnica NIRS en trabajos de I+D en el lEPA. En: A.Gómez Cabrera y E.J. de Pedro Sauz (Eds.), Nuevas Fuentes de Alimentos para la Producción Animal IV, Junta de Andalucía, Consejería de Agricultura y Pesca, pp: 271-278.
DE LA ROZA, B.; A. MARTINEZ, S. MODROÑO y B. SANTOS. 1996.Determination of the quality of fresh silages by near infrared reflectance spectroscopy. In: A.M.C. Davies y P. Williams (Eds.), Near Infrared Spectroscopy: The Future Waves. Proceedings of the 7th International Coníerence on Near Infrared Spectroscopy, Montreal, Cemada, 6-11 August 1995. NIR Publications, Chichester, UK,pp:537-541.
DEINUM, B. y A. M A AS SEN. 1993. Effects of drying temperatura on chemical composition and in vitro digestibility of forages. Anim. Feed Sci. and Technol. 46:75-86.
DOWMAN, M.G. y COLLINS, F.C. 1982. The use of enzymes to predict the digestibility of animal feeds. J. Sci. Food Agric., 33:689-696.
DOWNEY, G. 1994. Qualitative Analysis in the Near-infrared Region. Analyst, 119:2367-2375.
DUMONT, J.C. 1994. Análisis y composición química de ensilajes. En: M. González y G. Bortolameolli (Eds.). II Seminario "Producción y Utilización de Ensilajes de Pradera para Agricultores de la Zona Sur". Instituto Investigaciones Agropecuarias, Est. Exp. Remehue, Serie Remehue No. 52, pp:27-37.
GABRIELSEN,B.C., K.P.VOGEL y D.KNUDSEN. 1988. Comparison of In Vitro Dry Matter Digestibility and Cellulase Digestion for Denving Near Infrared Reflectance Spectroscopy Calibration Equations Using Cool-Season Grasses. Crop Sci. 28:44-47.
GARRIDO, A., J.E.GUERRERO y A.GOMEZ CABRERA. 1993. Posibilidades y limitaciones de la aplicación de la técnica NIRS en la evaluación nutricional de alimentos para el ganado. En: A. Gómez Cabrera y E.J. de Pedro Sauz (Eds.), Nuevas Fuentes de Alimentos para la Producción Animal IV, Tunta de Andalucía, Consejería de Agricultura y Pesca, pp: 243-255.
GIVENS, D.I. 1986. New Methods for Predicting
the Nutritive Value of Silage.En: Stark, B y M. Wilkinson (Editors), Developments
in Silage, Chalcombe, pp: 66-75.
GIVENS, D.1.1993. Evaluating energy & protein in grass
& grass silage. Grass Farmer, 45:26-27.
GIVENS, D.I., J.M. EVERINGTON y A.H. ADAMSON. 1989. The Digestible and Metabolizable Energy Content of Grass Silage and their Prediction from Laboratory Measurements. Animal Feed Sci. and Technol., 24:27-43.
GIVENS, D.I., J.L. DE BOEVER y E.R. DEAVIEEE. 1997. The principies, practices and some future applications of near infrared spectroscopy for predicting the nutritive value of foods for animáis and humans. Nutrition Research Revs, 10:83-114.
GOERING, H.K. y P.J.VAN SOEST. 1970. Forage fiber analysis. USDA, ARS Agric. Handbook No 379. 20p., Washington D.C.
GONZALEZ, M. 1994. Métodos para mejorar la calidad de los ensila]es. En: M. González y G. Bortolameolli (Eds.). II Seminario "Producción y Utilización de Ensilajes de Pradera para Agricultores de la Zona Sur". Instituto Investigaciones Agropecuarias, Est. Exp. Remehue, Serie Remehue No. 52, pp:3-25.
HILDRUM, K.I., T. ISAKSSON, T. NAES, B.N. NILSEN, M. RODBOTTEN and P. LEA. 1995. Near infrared reflectance spectroscopy in the prediction of sensory properties of beef. J. Near Infrared Spectrosc..3:81-87.
HIRIART, M. 1981. Energía Digestible en Ensilajes. Agro Sur, 9:117-118.
HIRIART, M. 1994. Manual de Métodos Analíticos en Nutrición Animal. Instituto de Investigaciones Agropecuarias, CRI Carillanca, Temuco, 31 p.
HIRSCH-REINSHAGEN, P. 1992. Tablas de composición de alimentos para ganado de las zonas centro y centro sur de Chile. Ministerio de Agricultura (FIA)- Pontificia Universidad Católica de Chile, Departamento de Zootecnia, Santiago, 52p.
ISI. 1992. NIRS 3. Routine operation, Calibration and Network system Management S oftware for Near Infrared Instruments. Infrasoft International. PerstoipAnalytical Inc., Silver Spring, MD 20904, 328 p.
JIN, T.; E. LIU, X. TANG y H. CHEN. 1995. Differentiation of male, female and dead silkworms while in the cocoon by near infrared spectroscopy. J. Near Infrared Spectrosc., 3:89-95.
JONES, D.I.H. y HYWARD, MV. 1975. The effect of pepsin pretreatment of herbage on the prediction of dry matter digestibility from solubility in fungal cellulase solution. J. Sci. Food Agric., 26:711-718.
KENNEDY, C.A.; J.A. SHELFORD y P.C. WILLIAMS. 1996. Near infrared spectroscopy analysis of intact grass silage and fresh grass for dry matter, crude protein and acid detergent fiber. In: A.M.C. Davies y P. Wilhams (Eds.), Near Infrared Spectroscopy: The Future Waves. Proceedings of the 7th International Conference on Near Infrared Spectroscopy, Montreal, Canada, 6-11 August 1995. NIR Publications, Chichester, UK, pp:524-530.
LATRILLE, L. y D. ALOMAR. 1993. Experiencias en el uso de aditivos de ensilajes. Ciencia e Investigación Agrícola, 20:345-371.
LI, Y., G. LAYCOCK y W. FERNETS. 1996. Rapid assessment of potential malting quality of barley by near infrared diffuse reflectance spectroscopy. In: A.M.C. Davies y P. Williams (Eds.), Near Infrared Spectroscopy: The Future Waves. Proceedings of the 7th International Conference on Near Infrared Spectroscopy, Montreal, Canada, 6-11 August 1995. NIR Publications, Chichester, UK, pp:475-478.
MARTEN, G.C.; J.L. HALGERSON y J.H. CHERNEY. 1983. Quality Prediction of Small Grain Forages by Near Infrared Reílectance Spectroscopy. Crop Sci., 23:94-96.
MARTEN, G.C., J.S.SHENK y F.E. BARTON II (editors). 1989. Near Inrrared Reflectance Spectroscopy (NIRS): Analysis of Forage Quality. U.S. Department of Agriculture, Agriculture Handbook No.643 (revised with supplements), 110p.
MASOERO, G.; G. XICCATO, A. ZOTTE, R. PARIGI, G. BERGOGLIO y A. DALLE. 1994. Analysis of freeze-dried rabbit meat by NIRS. Zootecnia e Nutrizione Animale, 20:319-329.
MOSS, A.R., D.I. GIVENS y R.H. PHIPPS. 1992. Digestibility and energy value of combinations of forage mixtures. Animal Feed Sci. and Technol. 39:151-172.
MURRAY, I.1988. Aspects of the interpretation of Near Infrared Spectra. Food Science and Technology Today, 2:135-140.
MURRAY, I. 1993. Forage Analysis by Near Infra-Red Reflectance Spectroscopy. In: Davies, Baker, Grant and Laidlaw (Eds.), Sward Measurement Handbook, Second Ed., British Grassland Soc., pp:285-312.
NORRIS, K.H. 1989a. NIRS Instrumentation. En: MARTEN, G.C, J.S.SHENK y F.E.BARTON II (editors). Near Infrared Reflectance Spectroscopy (NIRS): Analysis of Forage Quality. U.S. Department of Agriculture, Agriculture Handbook No.643 (revised with supplements), pp: 12-17.
NORRIS, K.H. 1989b. Definition of NIRS Analysis. En: MARTEN, G.C., J.S. SHENK y F.E. BARTON II (editors). Near Infrared Reflectance Spectroscopy (NIRS): Analysis of Forage Quality. U.S. Department, of Agriculture, Agriculture Handbook No.643 (revised with supplements), p:6.
NORRIS, K.H., R.F. BARNES, J.E. MOORE y J.S. SHENK. 1976. Predicting forage quality by near infrared reflectance Spectroscopy. J. Anim. Sci., 43:889-897.
PASCUAL, J.J. y P. MOLINA. 1996. Automatic determination of protein fractions in manchega eweís milk by near infrared reflectance Spectroscopy. In: A.M.C. Davies y P. Williams (Eds.), Near Infrared Spectroscopy: The Future Waves. Proceedings of the 7th International Conference on Near Infrared Spectroscopy, Montreal, Cemada, 6-11 August 1995. NIR Publications, Chichester, UK, pp:559-564.
REEVES, J.B. 1994. Use of Near Infrared Reflectance Spectroscopy as a Tool for Screening Treated Forages and By-products. J. Dairy Sci., 77:1030-1037.
REEVES, J.B., T.H. BLOSSER y V.F. COLENBRANDER. 1989. Near Infrared Reflectance Spectroscopy for Analyzing Undried Silage. J. Dairy Sci. 72:79-88.
ROBERT, P., D. BERTRAND and C. DEMARQUILLY. 1986. Prediction of forage digestibility by principal components analysis of near infrared reflectance spectra. Anim. Feed Sci. And Technol., 16:215-224.
ROBERTS, C.A., R.E. JOOST and G.E. ROTTINGHAUS. 1997. Quantification of ergovaline in tall fescue by near infrared reflectance Spectroscopy. Crop Sci., 37(l):281-284.
SHENK, J. 1989. Public Software. In: Marten, G.C., J.S. Shenk y F.E. Barton II (Eds.), Near Infrared Reflectance Spectroscopy (NIRS): Analysis of Forage Quality. U.S. Department of Agriculture, Agric . Handbook N° 643 (revised with supplements), 110p.
SHENK, J. y M. WESTERHAUS. 1991. New standardization and calibration procedure for NIRS analytical systems. Crop Sci., 31:1694-1692.
SHENK, J. y M. WESTERHAUS. 1993. Analysis of Agriculture and Food Products by Near Infrared Reflectance Spectroscopy. Monograph. Dept. of Agronomy, Penn State University and Infrasoft. International, Port Matilda, PA, USA, 116 p.
SHENK, J. y M. WESTERHAUS. 1995. The application of near infrared reflectance Spectroscopy (NIRS) to forage analysis. In: Fahey, G.C. (ed.) Forage Quality, Evaluation, and Utilization. A.S.A., C.S.S.A., S.S.S.A., Madison, WI. pp:406- 449.
SOLSBERG, C. 1996. Use of near intrared transmittance in quality analysis of ñsh. In: A.M.C. Davies y P. Williams (Eds.), Near Infrared Spectroscopy: The Future Waves. Proceedings of the 7th International Conference on Near Infrared Spectroscopy, Montreal, Canada, 6-11 August 1995. NIR Publications, Chichester, IJK, pp:494-497.
TAKAHASHI, M., M. HAJIKA, K. IGITA y T. SATO. 1997. Rapid estimation of protein, oil and moisture contents in whole-grain soybean seeds by near infrared reflectance Spectroscopy. In: A.M.C. Davies y P. Williams (Eds.), Near Infrared Spectroscopy: TheFuture Waves. Proceedings of the 7th International Conference on Near Infrared Spectroscopy, Montreal, Canada, 6-11 August 1995. NIR Publications, Chichester, UK, pp:494-497.
THOMAS, C. y P.C.THOMAS. 1985. Factors Affecting the Nutritive Value of Grass Silage. In: Haresign,W. y JJ.Cole (Eds.), Recent. Advances in Animal Nutrition, Butterworths, London, p:223-256.
TILLEY, J.M.A. y TERRY, R.A. 1963. A two stage technique for in vitro digestion of forage crops. J. Br. Grassl. Soc. 18:104-111.
TODOROV, N.; S. ATANASSOVA, D. PAVLOV y R. GRIGOROV A. 1994. Prediction of dry matter degradability of forages by near infrared Spectroscopy. Livestock Production Science, 39:89-91.
TORRES, A. 1994. Praderas destinadas a ensilaje. En: M. González y G. Bortolameolli (Eds.). II Seminario "Producción y Utilización de Ensilajes de Pradera para Agricultores de la Zona Sur". Instituto Investigaciones Agropecuarias, Est. Exp. Remehue, Serie Remehue No. 52, pp:l 19-143.
TREMBLAY, G.F.; G.A. BRODERICK y S.M. ABRAMS. 1996. Estimating Ruminal Protein Degradability of Roasted Soybeans Using Near Infrared Reflectance Spectroscopy. J. Dairy Sci., 79:276-282.
UNIVERSIDAD AUSTRAL DE CHILE (INSTITUTO DE PRODUCCION ANIMAL). 1985. Composición de alimentos para el ganado en la zona sur. Boletín técnico, Valdivia, 45p.
VALDES, E.V., L.G.YOUNG, I. McMILLAN y J.E.WINCH. 1985. Analysis of hay, haylage and corn silage samples by near infrared reflectance. Can. J. Anim. Sci. 65:753-760.
WATERS, CJ. y D.I. GIVENS. 1992. Nitrogen degradability of fresh herbage: effect of maturity and growth type, and prediction from chemical composition and by near infrared reflectance Spectroscopy. Animal Feed Science and Technology, 38:335-349.
WERNLI, C. y A. HARGREAVES. 1988. Conservación de forrajes.En: I. Ruiz (Ed.), Praderas para Chile, INIA, Santiago, Chile, pp:635-677.
WESTERHAUS, M.O. 1989a. Equation Development. In: Marten, G.C., J.S. Shenk y F.E. Barton II (Eds.), Near Infrared Reflectance Spectroscopy (NIRS): Analysis of Forage Quality. U.S. Department of Agriculture, Agric. Handbook N° 643 (revised with supplements), pp: 38-39.
WESTERHAUS, M.O. 1989b. Validation. In: Marten,
G.C., J.S. Shenk y F.E. Barton II (Eds.), Near Infrared Reflectance Spectroscopy
(NIRS): Analysis of Forage Quality. U.S. Department of Agriculture, Agric. Handbook
N° 643 (revised with
supplements), pp: 40.
WILLIAMS, P.C., K.R. PRESTON, K.H. NORRIS y P.M. STARKEY. 1984. Determination of Amino Acids in Wheat and B arl ey by Near-Infrared Reflectance Spectroscopy. Journal of Food Science, 49:17-20.
WORKMAN, J. J. 1996. Interpretative Spectroscopy for near infrared. In: A.M.C. Davies y P. Williams (Eds.), Near Infrared Spectroscopy: TheFuture Waves. Proceedings of the 7th International Conference on Near Infrared Spectroscopy, Montreal, Canada, 6-11 August 1995. NIR Publications, Chichester, UK, pp:6-13.