Agro Sur 34(1-2): 7-9 2006
CONFERENCIAS
AVANCES EN LA MICROPROPAGACIÓN DE PLANTAS ORNAMENTALES
ADVANCES IN THE MICROPROPAGATION OF ORNAMENTAL PLANTS
Daquinta, M.
Laboratorio de Cultivo de Células y Tejidos. Centro de Bioplantas. Universidad de Ciego de Ávila. Carretera a Morón Km. 9. CP 69450. Cuba, e-mail: mdaquinta@bioplantas.cu.
La micropropagación de plantas ornamentales encontró una gran aplicación en el campo de la horticultura. La comercialización de plantas decorativas de follajes y flores es de cientos de millones de unidades, de los cuales alrededor del 80% se produce con el empleo de esta tecnología. Se prevé un crecimiento anual del consumo en el mercado mundial de productos florícolas, por lo que es necesario mejorar las metodologías de propagación in vitro para satisfacer estas crecientes demandas. La inmersión temporal es una técnica que ha permitido el incremento de los coeficientes de multiplicación con la disminución de los costos de producción. El uso del medio líquido para la propagación in vitro tiene algunas ventajas y se considera una técnica ideal para la propagación masiva de plantas, porque reduce la manipulación y es un requisito indispensable para la automatización del proceso (Aitken-Christie, 1991). Sin embargo, su principal desventaja es que provoca la hiperhidricidad de los tejidos de los brotes. Para evitar este desorden fisiológico, se han desarrollado diferentes procedimientos, entre los que se encuentran el cultivo en agitación, el empleo de soportes alternativos como puentes de papel de filtro, tapones de celulosa, la técnica de doble capa, el enfriamiento del fondo del frasco de cultivo, etc., así como el empleo de agentes químicos antivitrificantes.
Alvard et al. (1993) estudiaron cinco métodos diferentes de cultivo en comparación con el cultivo en medio sólido en la propagación de meristemos de bananos. A partir de estos resultados surgió un nuevo concepto para el cultivo in vitro en medio líquido: la inmersión temporal (Teisson y Alvard, 1995). Esta técnica se ha empleado exitosamente con Coffea, Hevea, Musa, Citrus ya sea mediante proliferación de meristemos, cultivo de microestacas, desarrollo de embriones a partir de callos, germinación y conversión de embriones somáticos. La calidad del desarrollo de los brotes es generalmente mejor a la que se obtiene con el empleo del medio líquido o semi-sólido. La micropropagación de plantas requiere la transferencia periódica del cultivo a medio fresco debido al agotamiento y/o alteración de los nutrientes, así como, crecimiento o proliferación del tejido, que sobrepasa la capacidad del frasco de cultivo. Generalmente los cultivos se mantienen en frascos individuales y se transfieren a medio fresco en un intervalo de cuatro a seis semanas. Algunos sistemas de micropropagación alternativos con el empleo de medio líquido se han desarrollado con el propósito de la automatización del proceso y la consiguiente reducción de los costos. Teisson y Alvard (1995) desarrollaron un aparato para la micropropagación de plantas a partir de la modificación de una unidad de filtración Nalgene de 250 mL de capacidad cuyo nombre comercial es RITA. En Israel, un grupo de investigadores han diseñado un biorreactor desechable para el cultivo de órganos que actualmente comercializa la firma OSMOTEK.
En Cuba, a partir del desarrollo del primer sistema semi-automatizado de inmersión temporal en 1997, se han realizado investigaciones sobre la aplicación de esta técnica en la proliferación de meristemos de caña de azúcar (Lorenzo et al., 1998), para el cultivo intensivo de microtubérculos de papas (Jiménez et al.. 1998), para la propagación in vitro de la pina (Escalona et al., 1999) y para la proliferación de bananos (Daquinta et al., 1999).
El sistema consiste de dos recipientes, mangueras, filtros hidrofóbicos de 0,2 µm, electroválvulas y un compresor de aire. Un frasco es el vaso de cultivo para los explantes y el otro, el recipiente para el medio de cultivo. Ambos frascos se comunican a través de mangueras. Las baterías de cultivo se colocan en estantes con condiciones ambientales controladas. La frecuencia y el tiempo de inmersión se controlan a través de un autómata, el cual hace que se abre una válvula y el aire impulsa el medio de cultivo hacia el frasco que contiene los explantes. Durante el período de inmersión, el aire permite el burbujeo del medio, remueve los explantes y cambia la atmósfera dentro del recipiente del cultivo. Pasado el tiempo de inmersión, se activa una segunda válvula y regresa el medio al recipiente de almacenamiento.
El SIT tiene dos posibilidades de aplicación: para la obtención de explantes y su ulterior proliferación en frascos convencionales de la micropropagación o para la obtención de brotes aptos para el enraizamiento ex vitro y la aclimatización.
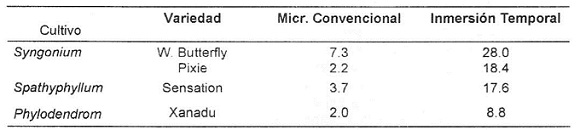
En el cuadro 1 se resumen los coeficientes de multiplicación que se han alcanzado en los diferentes cultivos ornamentales con el empleo del SIT.
 |
En todos los casos
el tiempo y la frecuencia de inmersión fueron de 2 minutos cada
tres horas. No se detallan las condiciones de cultivo en particular para
cada especie. |
BIBLIOGRAFIA
AITKEN-CHRISTIE, J. 1991. Automation. In: Debergh, P.C.; Zimmerman, R.H. (eds.). Micropropagation .Netherland, Kluwer Academic Publishers, pp 358-363.
AITKEN-CHRISTIE, J.; DAVIES, H. 1988. Development of a semi-automated micropropagation system. Acta Horticulturae 230: 81-87.
ALVARD, D,; COTE, F.; TEISSON, C. 1993. Comparison of methods of liquid medium culture for banana micropropagation. Effect of temporary immersion of explants. Plant Cell, Tissue and Organ Culture 32: 55-60.
DAQUINTA, M.; BARRERA, L.; LEZCANO, Y, MOSQUEDA, O.; ESCALONA, M.; BORROTO, C.G. 1999. Efecto de la oscuridad en la multiplicación in vitro del banano FHIA-18 en los sistemas 9 de inmersión temporal. Libro de Reportes Cortos. 5to Coloquio Internacional de Biotecnología Vegetal: pp 185-187.
ESCALONA. M.; LORENZO, J.C.; GONZALEZ, B.; DAQUINTA, M.; GONZALEZ, Y; ESJAR-DINS, J.L.; BORROTO, C.G. 1999. Pineapple (Ananas comosus L. Merr.) micropropagation in temporary immersion systems. Plant Cell Reports 18: 743-748. antivitrifying agents. Canadian Journal Plant Science 73: 231-235.
JIMENEZ, E.; PEREZ, N.; M DE FERIA, R.; BALBOA, R.; CAPOTE, A.; CHAVEZ, M.; QUIALA, E.; PEREZ, J.C. 1998. Improved production of potatoes (Solanum tuberosum L.) microtubers using temporary immersion systems. Plant Cell, Tissue and Organ Culture 54.
LORENZO, J.C.; GONZALEZ, B.; ESCALONA, M.; TEISSON. C.; ESPINOSA, P.; BORROTO, C.G. 1998. Sugar cane shoot formation in an improved Temporary Immersion System. Plant Cell, Tissue and Organ Culture. 54: 197-200.
TEISSON C.; ALVARD, D. 1995. A new concept of plant in vitro cultivation liquid medium: Temporary Immersion. In: Terzi, M.; Cella, R.; Falavigna, A. (eds.). Current Issues in Plant Molecular and Cellular Biology. Netherland, Kluwer Academic Publishers, pp. 105-109.