Cuadro
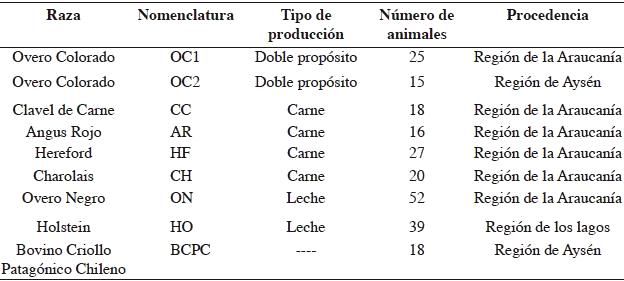
1. Número de animales muestreados por raza y zona geográfica.
Se indica el tipo de producción.
Table 1. Number of animals sampled by breed and geographical zone. The
type of production is indicated.
Agro Sur Vol. 39(1) 46-56 2011
DOI:10.4206/agrosur.2011.v39n1-05
ARTÍCULOS ORIGINALES
CARACTERIZACIÓN GENÉTICA DE UN REBAÑO DE BOVINO CRIOLLO PATAGÓNICO CHILENO
GENETIC CHARACTERIZATION OF A HERD OF CHILEAN PATAGONIAN CREOLE BOVINE
Jaime Piñeira V.(1), Fernando Mujica C.(2), Ricardo Felmer D.(1), Manuel Ortiz L.(4), Gabriela Pizarro I.(3), Marcela Aracena N.(2)
(1)
Laboratorio de Biotecnología Animal, INIA Carillanca,
(2) Facultad
de Ciencias Agrarias, Universidad Austral de Chile,
(3) Facultad de Recursos Naturales, Universidad
Católica de Temuco,
(4) Centro de Inseminación Artificial,
Universidad Austral de Chile.
ABSTRACT
The Criollo patagónico chileno (BCPC) (a type of Chilean creole that exist in the Patagonia) is a genetic resource that may have importance in the genetic improvement of extensive beef production systems both in the Aysen region as well as in other areas of Chile. Up to now there have been some studies designed to characterize phenotipically this type of animal but we are not aware of research aiming to determine its current conservation status and its population genetics, in comparison to other cattle breeds used in the country. The objective of this study was to characterize the genetic structure of a group of BCPC from a farm located in Mañihuales (Aysen); this structure was compared with that of other beef and dairy cattle breeds of common use in Chile. The analysis considered the use of 10 microsatellite markers recommended by FAO/ISAG that allowed to estimate several population genetic variables, perform Hardy and Weinberg proportions and identify groups genetically differentiated. Results indicate that the BCPC is an important source of bovine genetic variability, a characteristic that could be used along with its production characteristics and its adaptability to the Patagonian environment to further improve the genetics of cattle in the country.
Key words: creole bovine, genetic resources, diversity
RESUMEN
El bovino criollo patagónico chileno (BCPC) es un recurso genético que puede tener gran importancia en programas de mejoramiento genético de la ganadería tipo extensivo que se desarrolla tanto en la región de Aysén como en otras zonas del país. A pesar de esto, y aunque se han realizado estudios destinados a caracterizar fenotípicamente a dicho grupo de animales, a la fecha no se habían realizado estudios genéticos destinados a conocer su estado de conservación, y su estructura genética poblacional en comparación con la observada en otras razas bovinas utilizadas en Chile. Considerando lo anterior, el objetivo del presente estudio fue caracterizar la estructura genética de un grupo de BCPC existentes en un predio de la localidad de Mañihuales, Región de Aysén, la cual fue comparada con las estructuras genéticas de otras razas bovinas utilizadas comúnmente en Chile, para la producción de leche y carne. El análisis consideró la utilización de 10 marcadores microsatélites recomendados por FAO/ISAG, mediante los cuales fue posible estimar una serie de variables genético poblacionales, realizar pruebas de equilibrio de Hardy y Weinberg, y detectar la conformación de grupos genéticamente diferenciados. Los resultados indican que el BCPC es una importante fuente de variabilidad genética bovina, lo que junto con sus características productivas y su adaptabilidad al ambiente patagónico, podrían transformar a este grupo de animales en un importante recurso para la actividad ganadera nacional.
Palabras claves: bovinos criollos, recurso genético, diversidad.
INTRODUCCIÓN
Los recursos zoogenéticos para la alimentación y la agricultura, además de constituir la base esencial del proceso evolutivo de la vida en el planeta, son una parte fundamental de la base biológica de la seguridad alimentaria mundial y contribuyen a los medios de vida de más de 1.000 millones de personas (FAO, 2007).
La amplitud de concepto de recurso genético animal incluye tanto a especies terrestres como acuáticas, autóctonas o nativas, e incluso a especies exóticas asilvestradas, cuyo germoplasma transmitido de generación en generación, asegura la variabilidad genética de las poblaciones y su capacidad intrínseca para sobrevivir ante cambios medioambientales (Aranguren-Méndez et al., 2001).
Lamentablemente, a nivel productivo muchas veces no se ha logrado visualizar y valorizar dichos recursos y muy por el contrario, en sectores como el ganadero se tiende a menospreciar las características genéticas de funcionalidad y de adaptación de muchas razas nativas o criollas, en post de la selección de fenotipos más productivos capaces de dar respuestas más inmediatas a las demandas del mercado (Mujica 2008).
Como consecuencia de lo anterior, los recursos genéticos se están extinguiendo en el mundo en forma acelerada, hecho que ha sido informado por la Organización de las Naciones Unidas para la Agricultura y la Alimentación, la cual indica que en la actualidad el 20% de las razas de animales de granja se encuentran en peligro de extinción, a una tasa de desaparición de una raza por mes.
La realidad chilena no es distinta a lo planteado anteriormente, y estudios han demostrado que en Chile existe una utilización deficiente de recursos genéticos, como las razas criollas y nativas, en comparación con lo que se hace en otros países latinoamericanos como Brasil, Argentina, Colombia, Perú (Mujica, 2009), donde se ha avanzado en el levantamiento de información destinada a conocer la estructuración genética de las poblaciones (Martínez et al, 2007; Rivas et al, 2007; Armstrong et al., 2006; Martínez et al., 2003; Lirón et al., 2002; Zamorano et al., 1998; Bouzat et al., 1998), la variabilidad genética de los bovinos criollo con respecto a otros grupos de animales (Martínez et al., 2005), la búsqueda de alteraciones cromosómicas (Género et al., 1999), la estimación de heredabilidades para caracteres de interés productivo (Martínez et al., 2005) y evaluaciones inmunogenéticas (Quinteros et al., 1980).
La región de Aysén dispone de un recurso genético denominado Bovino Criollo Patagónico Chileno o bagual (en adelante BCPC), el cual ha sufrido considerables reducciones de su censo poblacional y que sobrevive únicamente gracias al esfuerzo de algunos ganaderos de la zona que han valorado su gran rusticidad y facilidad de parto, consecuencia del pequeño tamaño del ternero al nacer (Mujica, 2009). Debido a estas cualidades dichos productores los han conservado para cruzarlos con vaquillas especialmente de la raza Hereford, en sistemas extensivos de producción de carne (Aracena et al., 2008).
No existe plena certeza del origen de dicho ganado pero de acuerdo con antecedentes históricos, estos tendrían su origen en una corriente que comenzó en Venezuela y que luego llegó a Perú, Bolivia y Chile, desde donde posteriormente pasaron a Argentina y Paraguay (Rabasa, 1993), donde llegaron a ocupar enormes extensiones de territorio (Martínez, 2007).
Respecto del origen del BCPC se puede decir que no se tiene plena certeza de cómo llegaron los primeros animales a la patagonia chilena; sin embargo, existen dos documentos que sugieren que su llegada fue más bien tardía en comparación con otras regiones del continente, remontándose a mediados del siglo XIX. El primer registro que informa sobre la existencia de estos animales en la región de Aysén fue escrito por Santiago Marin Vicuña, ingeniero contratado por la Comisión Chilena de Límites, que en el año 1897 observó una gran cantidad de animales en el valle del río Mayer (actual Provincia Capitán Prat). Al respecto Marin-Vicuña informa que según relatos realizados por indios Tehuelches, dichos animales habrían acompañado la expedición que el año 1869 realizó el explorador británico George Chaworth Muster (Marin-Vicuña, 1901; Martinic, 2005).
Otro arribo importante de bovinos criollos habría sido el año 1906, cuando el explorador británico William Norris, contratado por la Compañía Explotadora del Baker, ingresó a la región de Aysén con 1.300 cabezas de ganado criollo comprado en la localidad de Tecka, Argentina, y que fueron trasladadas al sector de Bajo Pisagua, localizado al sur de dicha región (Ivanoff, 2000). Según las memorias escritas por Norris el año 1939, las cuales fueron parcialmente publicadas por Ivanoff (2000), "a pesar que dichos animales eran muy salvajes, no conocían al hombre y solo eran arriados unas cuantas veces al año, eran lo suficientemente buenos como para adaptarse a los valles protegidos, pastos y abundante agua existente en la Patagonia chilena".
En la actualidad la información existente acerca de las características, posibles ventajas y utilidades del BCPC es muy escasa. También se desconoce la situación actual en cuanto a los censos poblacionales, así como su nivel de "pureza" o cruzamientos con otras razas y su estado de conservación (Aracena et al, 2008).
De acuerdo con lo anterior, el objetivo del presente estudio fue caracterizar la estructura genética de un grupo de BCPC localizados en un predio de la localidad de Mañihuales, Región de Aysén del General Carlos Ibáñez del Campo, el cual fue comparado con las estructuras genéticas de otras razas bovinas utilizadas comúnmente en Chile, para la producción de leche y carne.
MATERIAL Y MÉTODOS
El estudio se realizó en la XI Región de Aysén del General Carlos Ibáñez del Campo, en un predio ubicado a 7 km de la ciudad de Mañihuales. En dicho lugar existe un rebaño de BCPC que cuenta con unos 60 animales, de los cuales fueron evaluados 18 que de acuerdo a la información entregada por el agricultor, poseen más de un 50% de criollo.
Toma de muestras
A los 18 animales evaluados les fueron tomadas muestras de pelo, las cuales fueron guardadas en bolsas de papel para posteriormente ser transportadas al laboratorio de biotecnología animal de INIA Carillanca Chile. Las muestras antes señaladas se contrastaron con otras muestras obtenidas de 212 animales, distribuidos en 8 razas bovinas productoras de leche y carne, localizadas en las regiones de la Araucanía, Los Lagos y Aysén (Cuadro 1).
Análisis de laboratorio
A partir de cada muestra, se seleccionaron 10 pelos que presentasen un folículo piloso visible. Dichos pelos se lavaron brevemente con agua destilada y se cortaron a 1 cm del bulbo. Estas muestras se dispusieron en un tubo eppendorf, al cual se le agregó 100μL de tampón de lisis de pelo (Tween 20 0,5%, NP-40 0,6%, MgCl2 5mM, Tris-HCl 10mM, pH 8,3, KCl 50mM) y 0,6 μL de proteinasa K (20 mg ml-1). Las muestras se incubaron a 60ºC por 1h en un termomixer (Eppendorf) con agitación de 800 r.p.m. y luego durante 15 min a 99ºC, para inactivar la proteasa. Antes de ser utilizada para su amplificación mediante PCR, se centrifugó la muestra por 2 min a 14.000 r.p.m., para separar las impurezas μ.
En el estudio se utilizaron 10 de los 20 marcadores microsatélite (Cuadro 2) recomendados FAO/ISAG, (2004), los cuales fueron analizados en el Centro de Inseminación Artificial, Universidad Austral de Chile, siguiendo un protocolo que consideró tres reacciones múltiplex en un termociclador Perkin Elmer modelo 9700. Cada reacción de PCR consideró un volumen de 20μ que contenía entre 20 y 100ng de ADN genómico, 100 μM de dNTP, 1,5 μM de MgCl2, entre 0,1 y 0,3 mM de partidor, tampón de PCR 1x y 1U de ampliTaqGold ADN polimerasa (Applied Biosystem). Las condiciones de reacción incluyeron una etapa inicial de desnaturalización del ADN por 5 min a 94ºC, seguida de 35 ciclos de amplificación consistentes en: desnaturalización por 1 min a 94ºC, hibridación por 1min a la temperatura adecuada para cada juego de primers y elongación por 1min a 72ºC, para terminar con una etapa de extensión de 10min a 72ºC.
Una vez realizada la amplificación de los loci microsatélites, éstos se separaron mediante electroforesis capilar. A tal efecto, las muestras se cargaron en un secuenciador automático ABI PrismTM – 310 Genetic Analyzer, utilizando un Módulo GSSTR POP4 (1ml) D. Md4, 5 segundos de tiempo de inyección, 15,0 Kv de voltaje de de inyección capilar, 15,0 kv de voltaje de electroforesis y una temperatura de 60º C. Finalmente, el genotipado se llevó a cabo mediante el programa GeneScan 3.7.
Análisis de datos
El análisis genético contempló la estimación de las variables poblacionales: número de alelos (na), riqueza alélicas (Ra), además de la heterocigosis observada (Ho) y esperada (He). De igual manera se realizó la prueba de equilibrio de Hardy y Weinberg (Falconer y MacKay 1996). Para tal efecto, se utilizaron los métodos de Weir y Cockerham (1984) y Robertson y Hill (1984), los que posteriormente fueron combinados mediante el método de Fisher's (1935). Posteriormente se estimó la distancia genética de Nei (Nei, 1987) y el índice de fijación FST (Wright, 1951). Los análisis se realizaron mediante los programas informáticos GenePop 4.0.10 (Raymond y Rousset, 1995) y FSTAT 2.9.3.2 (Goudet 1995). La visualización gráfica de los resultados se llevó a cabo mediante la confección de árboles filogenéticos mediante el método de Neighborjoining (Saitou y Nei, 1987). Para la confección de los árboles se utilizaron 1.000 juegos de datos (bootstraps); en su cómputo y visualización se utilizaron los programas Population 1.2.30 (Langella, 2002) y Treeview 1.6.6 (Page, 2001)
A continuación se realizó un análisis de cluster, el cual permite relacionar a los individuos más parecidos genéticamente. Dicho análisis utiliza un algoritmo bayesiano que emplea un modelo basado en el método de cadenas Markov de Monte Carlo, que estima la distribución a posteriori de cada coeficiente de mezcla de cada individuo (q). La media de esta distribución representa una estimación de la proporción que el genoma de un individuo tiene de las poblaciones parentales. Para el análisis se ha utilizado un periodo de burn-in de 100.000 repeticiones y 1.250.000 iteraciones y el programa Structure 2.3.3 (Pritchard et al., 2000).
Finalmente se realizó un Análisis Factorial de Correspondencia (AFC), el cual es equivalente al Análisis de Componentes Principales para variables cualitativas. Dicha evaluación intenta explicar una variable hipotética (factor), por medio de un modelo lineal en el que el factor (o varios factores) se encuentra en función de un conjunto grande de variables observables. En el presente estudio, se utilizó el programa Genetix v.4.05.2 (Belkhir et al., 2003), que elabora un gráfico 3D que corresponde a la codificación más conveniente para los datos de la genética de los organismos diploides, tal como fue propuesto por (She et al., 1987). En dicho gráfico los objetos analizados se ven como una nube de puntos en un hiperespacio que tiene tantas dimensiones como alelos. El algoritmo busca las direcciones independientes en este hiperespacio, la longitud de las cuales es la inercia. Estas direcciones, que son definidas por los vectores propios de la matriz, determinan una serie de ejes factoriales. Por convenio, el primer eje es el que tiene la contribución mayor a la inercia total.
|
Figura 1. Árbol filogenético
confeccionados a partir de las distancias genéticas interpoblacionales
de Nei, (1987) para las razas Overo Negro (ON), Holstein (HO), Angus Rojo
(AR), Overo Colorado de Vilcún, Overo Colorado de Coyhaique, Carolais
(CH) Hereford (HF) y Clavel de Carne (CC). Figure 1. Philogenetic trees made using the genetic distances inter-polulations of Nei (1987) for the reces Overo Colorado from Vilcún, Overo Colorado from Coyhaique, Carolais (CH) Hereford (HF) and Clavel de Carne (CC). |
RESULTADOS
El Cuadro 3 muestra las variables genético poblacionales, número de alelos (na), riqueza alélicas (Ra), heterocigosis observada (Ho) y heterocigosis esperada (He), obtenidas en cada una de las razas evaluadas, así como los resultados de los tests de equilibrio de Hardy y Weinberg agrupados mediante el método de Fisher's (1935).
En éste se puede observar que la raza con mayor número de alelos fue el BCPC (7.600±0,499), mientras que la raza con menor número de alelos fue Hereford (HF; 5,600±0,542). Lo mismo pudo observarse en la variable riqueza alélicas, donde BCPC y Hereford mostraron valores de 3,902±0,156 y 3,257±0,246 respectivamente.
En cuanto a Ho, se observó que esta variable alcanzó sus mayores niveles en la raza Overo Colorado muestreada en la región de Aysén (OC2; 0,827±0,118), mientras que los menores valores se observaron en Holstein (HO; 0,615±0,204). Lo anterior contrasta con los valores de He, que alcanzó su mayor y menor valor en BCPC (0,795±0,081) y Charolais (CH; 0,677±0,218).
Con respecto a la prueba de equilibrio de Hardy y Weinberg, se detectaron inconsistencias significativas (P<0,05) para las razas Clavel de Carne (CC) y Holstein (HO), las cuales mostraron déficit de heterocigotos (FIS 0,098±0,160 y 0,149±0,201 respectivamente). De igual manera, se detectó un desequilibrio altamente significativo en BCPC, el cual se traduce en un importante déficit de heterocigotos (FIS de 0,173±0,251).
La Figura 1 muestra un árbol filogenético en el que se aprecia una distancia bastante considerable entre BCPC y los clusters conformados por las razas productoras de leche (HO y ON) y las razas productoras de carne y doble propósito (AR, CH, HF, CC y OC). Este resultado es congruente con los resultados del análisis de clusters (Figura 2), donde se observa que los BCPC forman un cluster distinto a los conformados por las dos razas (HO y ON), (OC2, CC y CH), HF, OC1 y AR.
Por último, el Análisis Factorial de Correspondencia (Figura 3) muestra un resultado muy coherente con el análisis de clusters y el de distancias genéticas pues nuevamente se observan claros agrupamientos entre las razas productoras de leche y carne, mientras que los BCPC se sitúan a una distancia intermedia, con una ligera inclinación hacia los animales productores de carne y doble propósito.
DISCUSIÓN
Los resultados del presente trabajo indican que a pesar del reducido número de BCPC que fue posible incluir en el análisis (18 animales), estos presentaron un nivel de variabilidad genética comparable a los observados en otras razas utilizadas en Chile para la producción de leche y carne tales como Holstein, Angus Rojo, Charolais y Hereford. Al respecto es importante considerar que a diferencia de BCPC en la mayoría de estas razas se realiza inseminación artificial (IA) con semen importado, por lo que cuentan con un flujo constante de genes que explicarían la condición de equilibrio observada en la mayoría de los grupos raciales estudiados (Piñeira et al., 2012).
|
Figura 2. Análisis
individual de clusters. Cada barra representa a un individuo distinto,
los cuales han sido ubicados en las 6 poblaciones (6 colores) que mejor
explican el patrón genético presente en las 9 razas bovinas
evaluadas. Cada una de las barras verticales (individuos) se encuentra
en mayor o menor medida subdividida en segmentos de colores que representan
las fracciones (membresía) de cada individuo a cada una de las
6 poblaciones identificadas. En el eje de las abscisas se presentan los
valores del estadístico FST para cada una de las poblaciones; en
eje de las ordenadas se muestran los valores de las Q estimaciones; y
en la parte superior se muestra la distribución de los individuos
pertenecientes a los distintos grupos raciales. Figure 2. Clusters individual analysis. Each bar represents a different individual, which have been placed in the 6 populations (6 colors) that best explain the genetic pattern present in 9 breeds evaluated. Each of the vertical bars (individuals) is in more or less subdivided into segments of colors representing the fractions (membership) of each individual at each of the 6 identified populations. The x-axis shows the values of the FST statistic for each of the populations, in y-axis shows the values of Q estimates, and on top shows the distribution of individuals belonging to different racial groups. |
A pesar de los comparables niveles de variabilidad genética, los análisis de distancias genéticas, clusters y el Análisis Factorial de Correspondencias, revelan que los BCPC se distanciarían tanto de las razas productoras carne como de aquellas productoras de leche, lo que se debe a que en BCPC existen variantes alélicas de los microsatélites utilizados, distintas a las observadas en los otros grupos raciales.
Dicha condición, puede ser explicada por la acción del denominado efecto fundador y la deriva genética (Falconer y Mackay, 1996).
El efecto fundador, como su nombre lo indica, es un fenómeno que se origina cuando una población es constituida por un número de individuos (censo efectivo Ne) muy reducido respecto de la población original. Como consecuencia, en la nueva población será posible encontrar una mayor frecuencia de alelos raros o carecer de otros comúnmente encontrados en la población de origen. En relación con esto, existen antecedentes que indican que a mediados del siglo XIX, específicamente en 1850, la población de Bovinos Criollos Patagónicos en la zona pampera argentina variaba en torno a las 20.000.000 de cabezas (Lebedinsky, 1967), por lo que el número de individuos que constituyó las poblaciones de BCPC debió ser una muestra muy pequeña de la población original. Como consecuencia del pequeño tamaño de las poblaciones fundadoras, lo más probable es que también se haya gatillado un proceso de deriva génica, es decir que producto del azar, algunas varientes alélicas de genes neutros pudieron haberse fijado en las poblaciones (frecuencia = 1) o simplemente pudieron haber desaparecido (Ubilla y Altuna, 2009).
Aunque el presente estudio no realiza un barrido total del genoma, limitándose al uso de 20 marcadores microsatélites que por definición son neutros, es decir no se transfieren a ARN (Hamada et al., 1984), no es posible descartar que haya ocurrido un proceso de diferenciación en lo que respecta a las variantes alélicas de genes con valor adaptativo. Esto último, debido que una vez constituidas las poblaciones las cambios en las frecuencias génicas de dichos polimorfismos debieron haber dependido de los procesos de selección generadas de forma natural o por el hombre, en un prolongado período de adaptación a los entornos agroecológicos y de manejo en general. De esta manera, al igual que lo ocurrido con genes neutros, determinadas varientes alélicas asociadas a caracteres con valor adaptativo o productivo podrían haber visto aumentadas sus frecuencias génicas, mientras que otras pudieron desaparecer en un proceso de selección negativa (Ubilla y Altuna, 2009).
Al comparar las frecuencias genotípicas observadas con las frecuencias esperadas, la población de BCPC no presentó valores consistentes con una población en equilibrio de Hardy y Weinberg. De hecho, llama la atención la diferencia entre la heterocigosis observada (Ho) y la esperada (He) y el valor que alcanza en el estadístico FIS, los cuales sugieren que la población estudiada presenta un déficit de heterocigotos. La explicación más plausible para esta situación estaría dada por el hecho de que la mayoría de los criadores de BCPC no cuentan con registros genealógicos que permitan controlar la endogamia, lo que sin duda alguna está provocando pérdidas significativas de variabilidad genética y reducción de los censos efectivos poblacionales.
Finalmente, de cuerdo a los resultados del presente estudio y lo señalado por autores como Thao et al. (1998), Caballero y Toro (2002), Piyasatian y Kinghorn (2003) y Simianer 2005, el grado de diferenciación polimórfica observado en la población de BCPC estudiada combinado con el merito genético de este grupo de animales podría resultar en un importante indicativo de su valor como recurso genético. Sin embargo resulta urgente la realización de nuevos estudios que abarquen un número representativo de la población total de animales existentes en la Patagonia Chilena, la utilización de herramientas moleculares complementarias que permitan la realización de barridos geonómicos completos y estudios que permitan valorar productivamente a los animales.
|
Figura 3. Análisis
Factorial de Correspondecias Múltiples. El círculo color
azul agrupa a las razas productoras de leche Overo (ON) y Holstein (HO),
el círculo rojo a las razas productoras de carne Clavel de Carne
(CC), Angus Rojo (AR), Charolais (CH), Hereford (HF) y la raza de doble
propósito Overo Colorado (OC). El círculo verde agrupa a
los Bovinos Criollos Patagónicos Chilenos (BCPC). Puede observarse
que los factores 1 y 2 explican el mayor porcentaje de la variabilidad
observado, con valores de 30,20% y 21,38% respectivamente. Figure 3. Factorial analysis of multiple correspondences. The blue circle brings together the milk-producing breeds Holstein (OH) and Overo Negro (ON), the red circle to the meat-producing breeds Clavel de Carne (CC), Angus Rojo (AR), Charolais (CH), Hereford (HF) and the dual purpose breed Overo Colorado (OC). The green circle groups the Chilean Patagonian Creole Bovine (BCPC). The factors 1 and 2 explain the higer percentage of the observed variability, whith values of 30.20% and 21.38% respectively. |
CONCLUSIÓN
Conforme a los resultados del presente estudio el grado de diferenciación polimórfica observado en la población de BCPC estudiada es un importante indicador de su valor como recurso genético. Sin embargo el aislamiento de las poblaciones, la reducción de sus censos poblacionales, la inexistencia de programas de manejo y control de la endogamia, la pérdida de variabilidad genética y el inminente reemplazo por otras razas y especies ganaderas, tornan urgente la necesidad de destinar recursos materiales y humanos que permitan inventariar, caracterizar adecuadamente las poblaciones y conservar a este irreemplazable recurso genético.
BIBLIOGRAFÍA
ARACENA, M., MUJICA, F., ELIZALDE, F. 2008. Caracterización fenotípica del Bovino criollo patagónico. VIII Congreso de la Federación Iberoamericana de Razas Criollas y Autóctonas. Valdivia, Chile. Libro de Actas: pp. 75-82.
ARANGUREN-MÉNDEZ, J., JORDANA, J., GOMEZ, M. 2001. Genetic diversity in Spanish donkey breeds using microsatellite DNA markers. Genetics Selection and Evolution. 33: 433-442.
ARMSTRONG, E., POSTIGLIONI, A., MARTÍNEZ, A., RINCÓN, G., VEGA-PLA J. 2006. Microsatellite analysis of a sample of Uruguayan Creole bulls (Bos taurus). Genetics and Molecular Biology, 29: 267-272
BELKHIR, K., BORSA, P., CHIKHI, L., RAUFASTE, N., BONHOMME, F. 2002. GENETIX 4.04, logiciel sous Windows TM pour la génétique des populations. Laboratorio de Genética, poblaciones, Interacciones, CNRS UMR 5000, Universidad de Montpellier II, Montpellier, Francia.
BOUZAT, J. GIOVAMBATTISTA, G., GOLIJOW, C., LOJO, M., DULOUT, F. 1998. Genética de la Conservación de Razas Autóctonas: El Ganado criollo argentino. Interciencia, 23: 151-156.
CABALLERO, A., TORO M.A. 2002. Analysis of genetic diversity for the management of conserved subdivided populations. Conservation Genetics, 3: 289-299.
FALCONER, DS. Y MACKAY, T.F.C. 1996. Introduction to Quantitative Genetics. 4th ed. Longman Scientific and Technical, New York, NY, Pp. 49-83
FISHER, R.A. 1935. The logic of inductive inference (with discussion). J. R. Stat. Soc. 98: 39-82.
GENERO, E.R., RUMIANO, F.J.L., MORENO-MILLÁN, M. 1999. Estudio citogenético del ganado bovino criollo argentino biotipo patagónico. Archivos de Zootecnia, 48: 425-427.
GOUDET, J. 1995. FSTAT (Ver. 2.9.3.2): a computer program to calculate F-statistics. J. Heredity, 86: 485-486.
HAMADA, H., SEIDMAN, M., HOWARD, B.H., Y GORMAN, C.M. 1984. Enhanced gene expression by the poly(dT-dG)-poly(dC-dA) sequence. Mol. Cell. Biol., 4: 2622-2630.
IVANOF, DW. 2000. Caleta Tortel y su Isla de los Muertos. Editorial Terranova, Santiago de Chile. pp. 21-32.
KAUPE, B., WINTER, A. FRIES, R. ERHARDT, G. 2004. DGAT1 polymorphism in Bos indicus and Bos taurus cattle breeds. Journal of Dairy Research, 71: 182-187.
LANGELLA, O. 2002. Population 1.2.28. Logiciel de génétique des populations. Laboratoire Populations, génétique et évolution, CNRS UPR 9034, Gif-sur-Yvette.
EBEDINSKY, M. 1967. Estructura de la ganadería" Histórica y actual. 1ª. ed. Buenos Aires: Quipo. 1967.
LIRÓN, J.P., RIPOLI, M.V., DE LUCA, J.C., PERAL-GARCÍA, P., GIOVAMBATTISTA, G. 2002. Analysis of genetic diversity and populations structure in Argentine and Bolivian Creole cattle using five loci related to milk production. Genetics and Molecular Biology. 25: 413-419.
MARIN-VICUÑA, S. 1901. Al través de la Patagonia. Santiago de Chile, p. 99-100
MARTINEZ, R.D., GIOVAMBATTISTA, G., RIPOLI, M.V. 2003. Patagonian Argentine Creole cattle polymorphism: comparison with NorthWest populations of this breed. Veterinary science, 74: 287-290
MARTÍNEZ, R.D., FERNÁNDEZ, E. N., BRÓCCOLI A.M., MARTÍNEZ A., DELGADO, J.V. 2005. Variabilidad genética en el ganado bovino criollo argentino de origen patagónico. Archivos de Zootecnia, 54: 121-584.
MARTÍNEZ, R.A., D. GARCÍA, J. L. GALLEGO, G. ONOFRE, PÉREZ J., CAÑÓN, J. 2007. Genetic variability in Colombian Creole cattle populations estimated by pedigree information. Journal of Animal Science, 86: 545-552.
MARTINEZ, R.D. 2007. Caracterización zoométrica de bovinos criollos: patagónicos vs. Noroeste argentino. Rev. MVZ Córdoba 12: 1042-1049.
MARTINIC, M. 2005. De la Trapananda al Aysén. Pehuén Editores, Santiago, p. 93-95.
MUJICA. F. 2008. Recursos Genéticos Animales Nativos y Criollos en Chile. VIII Congreso de la Federación Iberoamericana de Razas Criollas y Autóctonas. Valdivia, Chile. Libro de Actas, p. 9-33.
MUJICA, F. 2009. Diversidad y Conservación de los recursos zoogenéticos del país. Agro Sur 37: 134-175.
NEI, M. 1987. Molecular Evolutionary Genetics. Columbia University Press, Nueva York.
ORGANIZACIÓN DE LAS NACIONES UNIDAS PARA LA ALIMENTACIÓN Y LA AGRICULTURA, SOCIEDAD INTERNACIONAL DE GENÉTICA ANIMAL (FAO/ISAG). 2004. Secondary Guidelines: Measurement of Domestic Animal Diversity (MoDAD): New Recommended Microsatellite Markers. (http://dad.fao.org/).
ORGANIZACIÓN DE LAS NACIONES UNIDAS PARA LA ALIMENTACIÓN Y LA AGRICULTURA (FAO). 2007. 11a Reunión Ordinaria, Comisión de Recursos Genéticos Para la Alimentación y la Agricultura. Roma, 11-15 de junio.
PAGE, RDM. 2001. TreeView (Win32) version 1.6.6. Available from http://taxonomy.zoology.gla.ac.uk/rod/rod.html.
PIÑEIRA J., RÍO J., FLOODY H., FELMER R. 2012. Distribución de polimorfismos asociados al grado de infiltración de grasa intramuscular en siete razas bovinas de carne utilizadas en la Región de la Araucanía, Chile. Arch Med Vet, 44: 43-52.
PIYASATIAN, N., KINGHORN, B.P. 2003. Balancing genetic diversity, genetic merit and population viability in conservation programmes. Journal of Animal Breeding Genetics 120: 137-149.
PRITCHARD, J.K., STEPHENS, M., DONNELLY, P. 2000. Inference of population structure using multilocus genotype data. Genetics, 155: 945-959.
QUINTEROS, I.R, MILLER, W.J, TEJEDOR, E.D., POLI, M.A., RUIZ, A.A. 1980. Investigaciones inmuno genéticas en el bovino criollo argentino marcadores genéticos. Analecta Veterinaria 12(1/2/3): 37-59.
RABASA, S. 1993. El bovino Criollo en los distintos países de América. En Ganado Bovino Criollo Tomo 3. Orientación Gráfica Editora SRL. 1ra Edición p. 1-13
ROBERTSON, A., HILL, WG. 1984. Deviations from Hardy-Weinberg proportions: sampling variances and use in estimation of inbreeding coefficients. Genetics 107: 703-718.
RAYMOND, M., ROUSSET, F. 1995. GENEPOP, Version 3.3: population for exact test ecumenism. J Heredity 86: 248-249.
RIVAS, E., VELI, E., AQUINO, Y., RIVAS, V., PASTOR, S., ESTRADA, R. 2007. Acciones para la caracterización y conservación del bovino criollo Peruano (Bos taurus). Agri, 40: 33-42.
SAITOU, N., NEI, M. 1987. The neighbor-joining method: a new method for reconstructing phylogenetic trees. Molecular Biology and Evolution 4: 406-425.
SHE, J.X., AUTEM, M., KOTOULAS ,G., PASTEUR, N., BONHOMME, F. 1987. Multivariate analysis of genetic exchanges between solea aegyptiaca and solea senegalensis (teleosts, soleidae). Biological Journal of the Linnean Society 32: 357-371.
SIMIANER, H. 2005. Decision making in livestock conservation. Ecological economics 53: 559-572.
THAON, D., ARNOLDI, C., FOULLEY, J.L., OLLIVIER, L. 1998. An overview of the Weitzman approach to diversity. Genetic selection and evolution 30: 149-161.
UBILLA, M. Y ALTUNA, C. 2009. El Prisma de la Evolución. Editorial DIRAC Facultad de Ciencias, Universidad la República, Montevideo Uruguay, 328 p.
WEIR, B.S. Y COCKERHAN, C.C. 1984. Estimating F-statistics for the analysis of population structure. Evolution, 38: 1358-1370.
WINTER, A., KRAMER, W., WERNER, F.A., KOLLERS, S., KATA, S., DURSTEWITZ, G., BUITKAMP, J., WOMACK, J.E., THALLER G., FRIES, R. 2002. Association of a lysine-232/alanine polymorphism in a bovine gene encoding acyl-CoA: diacylglycerol acyltransferase (DGAT1) with variation at a quantitative trait locus for milk fat content. Proc Natl Acad Sci USA 99: 9300-9305.
WRIGHT, S. 1951. The genetic structure of populations. Annals of Eugenics, 15: 323-354.
ZAMORANO, M.J., RUITER, J., RODERO, A, VEGA-PLA, J.L. 1998. Análisis genético de marcadores microsatélites en dos poblaciones de la raza bovina berrendo en negro. Archivos de zootecnia, 47: 195-200.
Fecha recepción antecedentes: 15 de octubre 2010