ARTICULOS ORIGINALES
Actividad sanguínea de glutatión peroxidasa en rebaños
lecheros a pastoreo: variación según edad y época del año*
A. Ceballos, M.V.Z., M. Sc.; F. Wittwer, M.V., M.V. Sc.; P.A. CONTRERAS, M.V., M. Phil.; H. Böhmwald, T.M.
Instituto Ciencias Clínicas Veterinarias, Universidad Austral
de Chile, Casilla 567, Valdivia, Chile.
SUMMARY
Glutathione peroxidase activity in grazing dairy cattle: age and seasonal variations
This study was designed to evaluate the nutritional status of selenium, measuring the blood GSH-Px activity in dairy herds from the South of Chile. Blood heparinized samples were taken from 5 groups (calves, rearing heifers, heifers, dry cows, and early lactating cows) of 7 animals each, from 8 dairy herds in the Province of Valdivia, Chile (39° S y 73° W) in the autumn of 1995. Groups of heifers and early lactating cows from the same herds were sampled during the spring of that same year.
A kinetic method was used to analyse blood GSH-Px activity. The mean and standard deviation of the values obtained were calculated. In order to compare the results among groups and between periods, the Kruskal-Wallis or Mann-Whitney statistical tests were used, as appropriate. The calves presented the highest values for blood GSH-Px activity while rearing heifers and heifers presented the lowest (P<0.01). In the rearing heifer and heifer groups there was an increase in the percentage of animals that presented low values of blood GSH-Px activity (30%). The blood GSH-Px activity of the dry period and early lactation groups was similar (P>0.01). A decrease in the GSH-Px activity was observed in heifers in spring, and the values were lower than those observed in autumn (P<0.01).
These results suggest that there are metabolic imbalances of selenium in dairy herds from the South of Chile; being grazing heifers the most affected.
Palabras claves: glutatión peroxidasa, selenio, estrés
oxidativo, bovinos.
Key words: glutathione peroxidase, selenium, oxidative stress, dairy cattle.
INTRODUCCION
La mayoría de las moléculas presentes en el organismo son químicamente
estables, es decir, tienen un número par de electrones en su orbital externo;
pero, existen otras cuyo número de electrones en el orbital externo es impar,
estas sustancias químicas altamente inestables y reactivas se conocen como radicales
libres (Barquinero, 1992). Cuando un radical interactúa con
una sustancia estable, toma de ella un electrón cargando positivamente la molécula;
así, el compuesto estable (no radical) se convierte en un radical libre altamente
agresivo, pudiendo generar más radicales, dando lugar a una reacción en cadena
(Halliwell, 1992).
El
oxígeno, aún siendo escencial para la vida, es también tóxico por ser una substancia
oxidante ya que puede aceptar electrones desestabilizando la molécula que lo
pierde; por lo tanto, en el metabolismo aerobio se producen oxidantes denominados
metabolitos oxigenados reactivos (MOR), entre los que se cuentan el anión superóxido
(O2•)1 , radicales hidroxilo
(OH•) y radicales alkoxy (RO•). Otras moléculas,
como el peróxido de hidrógeno (H2O2), no son radicales
libres; pero, químicamente se comportan como oxidantes (Barquinero,
1992); (Halliwell, 1992)). Existen otras fuentes de MOR
como las reacciones inflamatorias, la degradación de los ácidos grasos, la acción
del citocromo P-450 o en forma ocasional durante el metabolismo de ciertas sustancias
exógenas (Miller y col., 1993).
Bajo condiciones normales el organismo puede neutralizar la
capacidad reactiva de los MOR por la acción del sistema antioxidante; pero,
hay momentos en que se supera la capacidad antioxidante quedando el organismo
expuesto a la acción de los metabolitos oxigenados en lo que se conoce como
estrés oxidativo (Miller y col., 1993).
La glutatión peroxidasa (GSH-Px; EC 1.11.1.9) es una metaloenzima
que forma parte del sistema glutatión, señalado como el principal sistema antioxidante
del organismo. Hasta ahora se han identificado tres tipos de GSH-Px: celular,
extracelular (plasmática) y fosfolípido hidroperóxido glutatión peroxidasa.
La estructura de la enzima celular está conformada por cuatro subunidades de
22.000 daltons cada una donde cada subunidad contiene un residuo de selenio
(Se) en forma de selenocisteína (Burk y Hill, 1993).
La deficiencia de Se induce una baja actividad de GSH-Px, dejando
la célula expuesta a la acción nociva de los MOR, lo que produce alteraciones
en la estructura de los lípidos, proteínas, polisacáridos, DNA y otras macromoléculas
celulares (Miller y col., 1993). No sólo se altera la funcionalidad
celular sino también la estructura de organelos intracelulares como mitocondria,
lisosoma, pared y estructura celular (Combs y col., 1975).
Como producto de la deficiencia de Se, el estrés oxidativo se ha asociado con
la presentación de algunas patologías en el bovino como enfermedad del músculo
blanco, retención de placenta, inmunosupresión y mastitis, entre otras (Van
Saun, 1990; Eicken y col., 1992).
En Chile se han reportado casos de deficiencia de Se en equinos
(Contreras y col., 1991; Ceballos y col., 1996);
además, se han realizado algunos estudios para conocer la composición mineral
de forrajes (Haardt y col., 1976; Egaña y col.,
1987; Wittwer y col., 1988); pero no hay estudios acerca
de la concentración edáfica o forrajera de Se o de su balance nutricional en
bovinos.
En consideración a lo anterior, este trabajo tiene por objeto
conocer, caracterizar y evaluar, en diferentes épocas del año, el balance metabólico
nutricional de Se en bovinos de diferentes grupos etarios y productivos de rebaños
lecheros del sur de Chile.
MATERIAL Y METODOS
En el valle central de la provincia de Valdivia, Chile (39°
LS y 73° LO) fueron seleccionados ocho rebaños lecheros segun su ubicación geográfica,
actividad productiva, masa ganadera, tipo de alimentación del rebaño y que los
animales no estuvieran recibiendo una cantidad de Se adicional al consumido
en la pradera, el concentrado o la sal mineralizada.
La región presenta un clima oceánico con influencia mediterránea
húmeda y con una pluviosidad anual de ±1.800 mm. La distribución anual de lluvias
se caracteriza por presentar dos períodos definidos de baja y alta pluviosidad,
alternados con dos períodos de pluviosidad intermedia. El año 1995 el período
verano-otoño presentó una baja pluviosidad, concentrando el 35% del total anual,
mientras que el período invierno-primavera tuvo el 65% de las lluvias. La temperatura
en los períodos de alta pluviosidad disminuye alcanzando un promedio de 7° C,
mientras que en la época de baja pluviosidad es más elevada alcanzando un promedio
de 17° C (Goic y Siebald, 1987).
La superficie de los predios varió entre 100 y 700 hectáreas
aproximadamente. La topografía dominante es plana con pendientes simples a ondulada.
Los suelos son trumaos con una reacción ligera a fuertemente ácida, predominando
los pH fuertemente ácidos y el drenaje fluctúa entre moderado a excesivo. En
el área destinada a la ganadería predominaban las praderas mejoradas, en las
que se encuentran especies forrajeras como ballicas (Lolium sp.) y tréboles
(Trifolium sp.), en menor proporción pasto ovillo (Dactylis glomerata),
pasto miel (Holcus lanatus), pasto oloroso (Anthoxanthum odoratum),
pasto cebolla (Arrhenatherum elatius) y chépica (Agrostis capillaris).
La utilización de la pradera era con pastoreo directo y la conservación de excedentes
de forraje mediante ensilaje al final de la primavera o henificación en el verano.
El sistema de producción de leche correspondía a un modelo
con tendencia estacional, concentrando en primavera y otoño el mayor número
de partos, con una alimentación basada en la utilización de pradera, forrajes
conservados en la época invernal y alimentos concentrados como suplementación
para las vacas en producción. Las terneras estaban mantenidas en estabulación,
y su alimentación se basaba en el suministro de leche o sustituto lácteo hasta
los 60 días, más concentrado y heno a voluntad, en dos predios no recibían concentrado.
Después de los dos meses de edad se pasaban a pastoreo las terneras nacidas
en primavera, mientras que las nacidas en otoño iniciaban el pastoreo a los
seis meses, suspendiéndose el suministro de alimentos concentrados. Las vaquillas
y vacas preparto estaban en pradera; la suplementación con ensilaje o heno elaborados
en el mismo predio, era sólo en invierno.
La suplementación con sales minerales era principalmente para
las vacas en lactancia; sólo en cuatro predios se mantenía sal mineralizada
a voluntad para las vaquillas. En tres de los productos usados como suplemento
para las vacas, aparece el Se como componente de la mezcla mineral en una concentración
entre 5 y 13 ppm; de las sales utilizadas para las vaquillas sólo una contiene
Se como ingrediente.
Toma de muestras. En mayo de 1995 se seleccionaron en
cada rebaño 5 grupos de animales conformados por 7 terneras entre 15 y 60 días
de nacidas (terneras lactantes), 7 terneras entre 6 y 12 meses (terneras de
recría), 7 vaquillas entre 13 y 24 meses, 7 vacas preparto (no lactantes) y
7 vacas en el inicio de la lactancia. Se obtuvieron entre 5 y 10 ml de sangre
heparinizada mediante venopunción coccígea o yugular empleando el sistema de
tubos al vacío, los tubos se trataron previamente con una solución de ácido
nítrico (HNO3) al 15%. Las muestras se llevaron dentro de 24 horas al Laboratorio
de Patología Clínica Veterinaria de la Universidad Austral de Chile.
En noviembre de 1995 en los mismos rebaños se seleccionaron
dos grupos de animales igualmente elegidos al azar y conformados por 7 vaquillas
entre 13 y 24 meses y 7 vacas en el inicio de la lactancia.
Análisis. La concentración de hemoglobina se determinó
mediante el método de la cianometahemoglobina (Jain, 1986). Posteriormente se
preparó 1 ml de un hemolizado de la muestra de sangre conservándolo a –25° C
en envases plásticos debidamente identificados hasta su posterior análisis.
La actividad sanguínea de GSH-Px se analizó mediante la utilización de un juego
de reactivos comercial (Ransel®. Laboratorios Randox, Crumlin, Irlanda
del Norte) basado en una técnica cinética NADPH-dependiente según una modificación
del método descrito por Paglia y Valentine (1967). Los resultados
se expresan en U/g Hb.
Análisis estadístico. El tipo de distribución
de los datos se evaluó mediante la prueba de normalidad descrita por Pearson
y Stephens (1964). Se obtuvieron para cada grupo etario y estado productivo,
el rango de actividad y las estimadas promedio (x) y desviación estándar (DE)
(Domènech, 1980). Para establecer si las muestras procedían
de poblaciones diferentes se utilizó el método de Kruskal-Wallis para el análisis
de varianza por rangos; las diferencias entre los grupos fueron establecidas
utilizando la prueba de comparaciones múltiples de Dunn con una probabilidad
de error a = 0.01 (Daniel, 1978).
La comparación entre los períodos de otoño y primavera se realizó mediante la
prueba de Mann-Whitney con una probabilidad de error a
= 0.01(Daniel, 1978).
Para la técnica analítica se ha señalado una actividad enzimática
igual o menor a 60 U/g Hb (Randox, 1990) como límite bajo
el cual se considera que hay deficiencia nutricional de Se, por lo que se presenta
la frecuencia de individuos, rebaños y grupos de animales con valores de actividad
igual o inferior Se consideró que en el grupo había deficiencia de Se, al encontrar
una actividad de GSH-Px en promedio igual o inferior a la cifra señalada o cuando
tres o más individuos en el grupo presentaron valores bajos en la actividad
enzimática.
RESULTADOS
En el otoño, el promedio y la desviación estándar de la actividad
sanguínea de GSH-Px en los grupos estudiados fue 145 ± 90 U/g Hb, con un rango
de 26-426 U/g Hb. Las terneras lactantes presentaron la mayor actividad enzimática,
mientras que las terneras de recría y las vaquillas tuvieron una actividad enzimática
menor, encontrándose diferencias entre los grupos (P<0.01). Las vacas preparto
y en el inicio de la lactancia presentaron una actividad enzimática similar
(P>0.01) con valores que se ubicaron entre los encontrados para los grupos
anteriores (cuadro 1). Igualmente, se encontraron diferencias
(P<0.01) en la actividad sanguínea de GSH-Px entre los grupos de cada rebaño,
situación que fue similar en los ocho rebaños estudiados.
|
Cuadro 1
Promedio, desviación estándar y rango de la actividad
sanguínea de glutatión
peroxidasa en grupos de animales de rebaños lecheros.
Mean, standard deviation and range of blood glutathione
peroxidase activity in groups
of animals from dairy herds.
|
|
| |
Edad -
|
Actividad de GSH-Px
|
| Animales |
estado
|
(U/g Hb)
|
| |
productivo
|
|
| |
|
 ± DE* ± DE*
|
Rango
|
|
|
|
Terneras
|
15-60 días
|
209 ± 96 |
37 - 426
|
a |
|
Terneras
|
6-12 meses
|
119 ± 78 |
26 - 342
|
b, c |
|
Vaquillas
|
13-24 meses
|
99 ± 42 |
26 - 190
|
b |
|
Vacas
|
Preparto
|
161 ± 82 |
46 - 409
|
a, d |
|
Vacas
|
Inicio de lactancia
|
143 ± 65 |
35 - 404
|
c, d |
|
| * Promedio de 8 rebaños con 7 observaciones
por grupo. |
| Letras diferentes (P<0.01). |
En las terneras lactantes se observó el menor número de individuos
con una actividad enzimática inferior al valor señalado como marginal, encontrándose
sólo 3 (5.5%) animales con valores bajo 60 U/g Hb. En el grupo de las terneras
de recría se encontraron 20 (36.4%) individuos y en el grupo de las vaquillas
13 (23.6%) con una actividad de GSH-Px en sangre inferior al valor marginal.
En las vacas sólo se observaron 4 (7.3%) hembras preparto y 8 (14.5%) en el
inicio de la lactancia con una actividad enzimática disminuida.
En el rebaño 2 se encontraron todos los grupos de animales
con una actividad enzimática promedio menor al valor marginal. En el rebaño
6 se encontraron todos los grupos, excepto las terneras lactantes, con un bajo
valor promedio en la actividad enzimática. En los rebaños 1 y 3 sólo se encontraban
afectados los grupos de terneras de recría y las vaquillas con una actividad
enzimática promedio más baja, siendo su valor inferior al reportado como marginal
(figura 1). En los rebaños 4, 5, 7 y 8 la actividad enzimática
promedio en los grupos analizados se encontraba mayor a 60 U/g Hb.
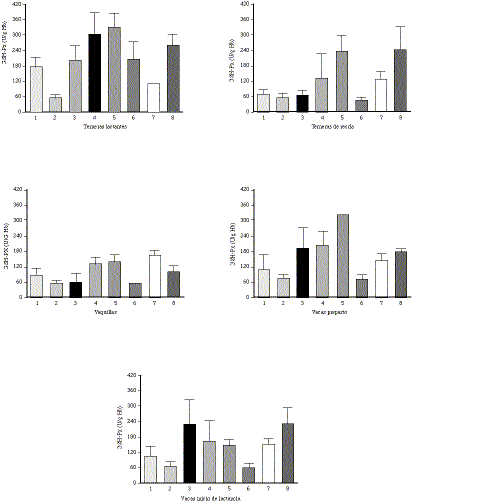
Figura 1. Actividad sanguínea de glutatión peroxidasa
en otoño en bovinos de cinco categorías etarias productivas de ocho rebaños
lecheros. Cada columna corresponde al 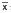 ± DE
(n=7).
± DE
(n=7).
Blood glutathione peroxidase activity during autumn, in five categories of animals
from dairy herds. Each column represents 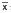 ± SD
(n=7).
± SD
(n=7).
En la primavera, la actividad enzimática observada en las vaquillas
fue significativamente menor que la observada en otoño (P<0.01). Contrariamente,
la actividad sanguínea de GSH-Px en las vacas en el inicio de la lactancia no
presentó diferencias (P>0.01) entre períodos (cuadro 2).
Asimismo, en la primavera aumentó la frecuencia de individuos en el grupo de
las vaquillas con una actividad enzimática inferior a 60 U/g Hb, las que se
encontraban en los rebaños 1, 3 y 6. En el grupo de las vacas en el inicio de
la lactancia, en primavera aumentó la frecuencia de individuos con una actividad
enzimática bajo el valor marginal en los rebaños 2 y 6 (figura
2).
|
Cuadro 2
Promedio, desviación estándar y rango de la actividad
sanguínea de glutatión
peroxidasa en vaquillas y vacas en el inicio de lactancia en otoño y primavera
en ocho rebaños lecheros.
Mean, standard deviation and range of blood glutathione
peroxidase activity in groups
of heifers and early lactating cows from dairy herds.
|
|
| |
Actividad de GSH-Px
|
| |
(U/g Hb)
|
|
Grupo
|
|
| |
Otoño
|
Primavera
|
| |
|
|
| |
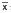
± DE* |
Rango
|
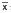
± DE* |
Rango
|
|
|
Vaquillas
|
99 ± 42 a
|
26 – 190
|
70 ± 24 b
|
15 – 128
|
|
13-24 meses
|
|
|
|
|
| |
|
|
|
|
|
Vacas
|
143 ± 65 c
|
35 – 404
|
125 ± 80 c
|
18 – 407
|
|
Inicio de lactancia
|
|
|
|
|
|
* Promedio de 8 rebaños con 7 observaciones
por grupo.
Letras diferentes (P<0.01) . |
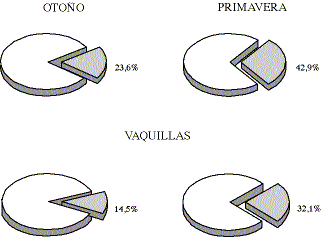
VACAS EN EL INICIO DE LA LACTANCIA
Figura 2. Frecuencia de vaquillas y vacas en
el inicio de la lactancia con actividad sanguínea de GSH-Px menor a 60 U/g Hb
en otoño y primavera en ocho rebaños lecheros.
Frequency of heifers and early lactating cows with low blood
glutathione peroxidase activity during autumn and spring in dairy herds.
El número de grupos de vaquillas y vacas en el inicio de la lactancia que presentaron
valores promedio bajos en la actividad sanguínea de GSH-Px, se mantuvo igual
tanto en otoño como en primavera. encontrándose en ambos períodos 3 de los 8
grupos de vaquillas y 2 de los 8 grupos de vacas en el inicio de la lactancia,
con una baja actividad sanguínea de GSH-Px.
DISCUSION
La mayor actividad sanguínea de GSH-Px se observó en el grupo
de las terneras lactantes, mientras que en las terneras de recría y las vaquillas
la actividad enzimática fue menor (cuadro 1), observándose
diferencias entre los grupos (P<0.01).
Una concentración de Se adecuada en los primeros días de vida
refleja la transferencia materna del mineral durante la gestación. En el feto
se ha comprobado que el hígado almacena el Se transferido por la madre; así,
este órgano tiene una reserva que puede ser movilizada rápidamente permitiendo
una actividad enzimática alta en las primeras semanas de vida (House
y Bell, 1994; Kirk y col., 1995). En los grupos de terneras
de recría y vaquillas se observaron desbalances nutricionales de Se en 6 de
los 16 grupos estudiados, al encontrarse una actividad enzimática inferior a
60 U/g Hb (figura 1). En estos grupos se encontró una disminución
en la actividad enzi-mática en la mayoría de los individuos muestreados, lo
que estaría indicando que el desbalance nutricional de Se obedece a un problema
de grupo más que a la afección de individuos en forma aislada.
Resultados similares se han observado en Nueva Zelanda, encontrándose
una baja actividad enzimática en vaquillas, con una disminución entre el 35
y 65% respecto al valor mínimo de referencia (Wichtel y col.,
1994). En Uruguay. se encontró en vaquillas un valor promedio de 26 U/g
Hb, considerando como valor marginal una actividad de GSH-Px inferior a 30 U/g
Hb (Ricciardino y col., 1991).
Una vez producida la depleción de la reserva de Se almacenada
durante la gestación y después del destete, las terneras de recría y las vaquillas
dependen únicamente del forraje y otros suplementos nutricionales para satisfacer
su requerimiento de minerales. Por lo anterior, si la suplementación con Se
en este período no es adecuada disminuye su concentración en la sangre trayendo
como consecuencia una actividad sanguínea de GSH-Px disminuida (Weiss
y col., 1984). Los forrajes que crecen en suelos deficitarios en Se presentan
un bajo contenido de este mineral; así, el consumo de estos forrajes y la falta
de una suplementación mineral, según el requerimiento, producirían una disminución
en la actividad sanguínea de GSH-Px (Jukola, 1994).
En consideración a lo anterior, es posible observar en los
animales a pastoreo una disminución de la actividad sanguínea de GSH-Px, siendo
las terneras de recría y las vaquillas los grupos más afectados (figura
1), ya que éstos dependen del consumo de forrajes para satisfacer no sólo
su requerimiento de minerales sino de otros nutrientes.
Las vacas preparto y en el inicio de la lactancia no presentaron
diferencias en la actividad enzimática (P>0.01), y sus valores se ubicaron
entre los observados para las terneras lactantes y las vaquillas (cuadro
1). En el preparto no se observaron grupos de vacas con desbalances nutricionales
de Se; mientras que en las vacas en lactancia se encontraron dos grupos con
valores disminuidos (figura 1). En otros estudios igualmente
se ha señalado que en las vacas la actividad de GSH-Px en sangre es adecuada,
habiéndose reportado valores superiores al que los autores consideraron bajo
o marginal (Backall y Scholz, 1979; Calamari y
col., 1989).
En los predios estudiados se observaron cambios en la alimentación
de las vacas con respecto a los demás grupos de animales. El uso de alimentos
concentrados de origen industrial contribuye a aumentar el contenido de Se en
la ración; así, se elevaría la concentración del mineral en el hígado, la sangre
y otros tejidos, como también en la leche (Binnerts y col., 1993).
Como respuesta biológica frente a un mayor aporte de selenio, se producirá un
aumento en la actividad sanguínea de glutatión peroxidasa (McDowell,
1992).
El aumento de Se en la ración producirá una elevación de la
actividad sanguínea de GSH-Px en un lapso entre l a 4 semanas después de la
suplementación (Knight y Sunde, 1988). Así, un cambio en la
alimentación entre el período seco y el inicio de la lactancia no tendría un
efecto inmediato sobre la actividad sanguínea de GSH-Px, lo que explicaría por
qué entre las vacas preparto y las vacas en el inicio de la lactancia no se
observaron diferencias (cuadro l) en la actividad enzimática
(P>0.01). Además, en las vacas preparto la actividad sanguínea de GSH-Px
se mantendría elevada gracias a la alimentación recibida al final de la lactancia,
la que es similar a la alimentación en el inicio de la lactancia, presentando
diferencias sólo en la cantidad de alimentos consumidos.
La disminución en la actividad sanguínea de GSH-Px que se observó
en algunos grupos de vacas en el inicio de la lactancia (figura
1), estaría dada por el consumo de un forraje con un bajo contenido de Se
y no recibir una suplementación adecuada durante el preparto, situación similar
a la encontrada en las terneras de recría y las vaquillas.
Sólo en las vaquillas se observaron diferencias en la actividad
sanguínea de GSH-Px entre otoño y primavera (P<0.01) encontrándose en primavera
los valores más bajos (cuadro 2) En primavera aumentó la frecuencia
de animales, tanto vaquillas como vacas al inicio de lactancia, con valores
bajos en la actividad enzimática (figura 2). Resultados
similares se han observado en otros estudios donde al final de primavera se
presentó una disminución en la actividad sanguínea de GSH-Px (Clark
y col., 1992; Mee y col., 1994; Wichtel
y col., 1996).
Anteriormente se había señalado que la concentración de Se
en la ración es el principal factor para inducir cambios en la actividad de
GSH-Px; así, cualquier variación estacional que se presente en la actividad
enzimática será una consecuencia de las variaciones en la concentración de Se
en la pradera, las que igualmente son estacionales y dependerían del régimen
de lluvias en cada período del año donde una alta pluviosidad produce una disminución
del contenido de Se (Grant y Sheppard, 1983; Clark
y col, 1992).
La actividad de GSH-Px refleja el estado metabólico de Se en
el organismo, que a su vez depende del consumo del mineral en los dos o tres
meses anteriores al análisis (Whitaker y Kelly, 1994); así,
se encontrarían en primavera valores bajos en la actividad enzimática por un
bajo consumo de Se en invierno. En vaquillas se ha observado una disminución
en la actividad enzimática cuando el animal retorna al pastoreo después de la
época invernal. Esta baja actividad sería una consecuencia del aporte deficitario
de Se durante la estabulación invernal (Hakkarainen y col., 1987).
En la provincia de Valdivia se concentra el 65% de la pluviosidad
anual en el período invierno e inicio de primavera, lo que induciría una disminución
en la concentración de Se en el forraje en esta época. Asimismo, el crecimiento
abundante del forraje, característico del inicio de primavera, guarda una relación
inversa con la concentración de Se, contribuyendo a disminuir el aporte del
mineral en la ración (Grant y Sheppard, 1983).
Por otra parte, el crecimiento del forraje en primavera presenta
un aumento en el contenido de ácidos grasos poliinsaturados, nitrógeno, oxalatos
y potasio, siendo éstos algunos factores que pueden inducir un aumento en el
requerimiento de antioxidantes, entre ellos el Se (Ardüser
y col., 1985; Wichtel y col., 1994; Wichtel
y col., 1996). El aumento en la demanda de Se va a contribuir a acrecentar
la deficiencia del mineral en primavera, y por ende la disminución en la actividad
de glutatión peroxidasa.
Al analizar los resultados obtenidos y bajo las condiciones
de este estudio, es posible concluir que en el sur de Chile se presentan valores
disminuidos en la actividad sanguínea de glutatión peroxidasa, compatibles con
la deficiencia de Se. Además, existen diferencias en la actividad sanguínea
de GSH-Px según el grupo de animales y la época del año, encontrándose en las
terneras de recría y en las vaquillas, al igual que en primavera, la mayor frecuencia
de individuos y grupos con valores de actividad enzimática disminuidos; diferencias
que obedecen principalmente a cambios en la alimentación.
RESUMEN
Con el objeto de estudiar en rebaños lecheros a pastoreo el
estado nutricional de selenio (Se) mediante el análisis de la actividad sanguínea
de glutatión peroxidasa (GSH-Px), se tomaron muestras de sangre en el otoño
de 1995 a diferentes grupos de bovinos en 8 rebaños de la provincia de Valdivia,
Chile (39° LS y 73° LO). En los mismos rebaños, en primavera, se repitió el
muestreo sólo en dos grupos.
La actividad enzimática fue analizada mediante una técnica
cinética enzimática (Ransel®, Randox Lab., Crumlin, UK). Los resultados
fueron descritos empleando estadística descriptiva y las comparaciones se hicieron
mediante análisis estadísticos no paramétricos.
Las terneras lactantes presentaron la mayor actividad enzimática
y el menor número de animales con actividad disminuida (5.5%), mientras que
las terneras de recría y las vaquillas presentaron los valores más bajos (P<0.01),
así como un mayor número de animales afectados (30%). Las vacas preparto y en
el inicio de lactancia presentaron una actividad enzimática similar (P>0.01),
con valores ubicados entre los observados para los grupos anteriores. En primavera
se hallaron valores de actividad enzimática más bajos que en otoño, aumentando
la frecuencia de individuos afectados (P<0.01).
Por lo anterior, es posible concluir que rebaños lecheros de
la provincia de Valdivia presentan deficiencias nutricionales de Se, siendo
más afectados los animales en crecimiento que son mantenidos en pastoreo y con
mayor intensidad en primavera.
Aceptado: 13.08.97.
* Proyecto FONDECYT-Chile 195 1062.
1 Los MOR se simbolizan con • (Halliwell, 1992).
BIBLIOGRAFIA
ARDÜSER, F., S. WOLFFRAM,
E. SCHARRER. 1985. Active absorption of selenate by rat ileum, J. Nutr. 115:
1203-1208.
BACKALL, K.A., R.W. SCHOLZ. 1979. Reference
values for a field test to estimate inadequate glutathione peroxidase activity
and selenium status in the blood of cattle. Am. J. Vet. Res. 40: 733-
738.
BARQUINERO, J. 1992. Los radicales libres:
una amenaza para la salud. En: CRYSTAL, R.G. y J.R. RAMON. 1992. Sistema GSH.
Glutatión: eje de la defensa antioxidante. Excerpta Medica. Medical Communications
B.V., Amsterdam.
BINNERTS. W.T., D. C. VIETS, H.A. DAS, C.F.
MILLS. 1993. Liver and milk: analysis for the selenium status of milk cows.
En: ANKE, M. y D. MEISSNER. 1993. Trace elements in man and animals. Proceedings
of the 8th. International Symposium on Trace Elements in Man and Animals. Gersdorf,
Germany.
BURK, R.F., K.E. HILL. 1993. Regulation of
selenoproteins, Annu. Rev. Nutr. 13: 65-81.
CALAMARI, L., G. BERTONI, M.G. MAIANTI, V.
CAPPA. 1989. Sull' utilità di nuovi parametri ematochimici nella valutazione
del profilo metabolico delle lattifere Zoot. Nutr. Anim., l5: 191-210.
CEBALLOS, A., O. ARAYA, E. PAREDES. 1996. Aspectos
clínico-patológicos de la esteatosis en el equino: descripción de un caso Arch.
Med Vet. 28: 125-130.
CONTRERAS, P.A., V. CUBILLOS, O ARAYA. 1991.
Enfermedad del músculo blanco en equinos: descripción de dos casos clínicos,
Patología Animal 5: 27-31.
CLARK, L.J., A.S. FAMILTON, A.B. WRIGHT, P.
ISHERWOOD, E. BAAS. 1992. Selenium field trials in dairy cattle, Vet. Cont.
Ed. Massey Univ., 145: 27-31.
COMBS Jr., G.F., T. NOGUCHI, M.L. SCOTT. 1975.
Mechanisms of action of selenium and vitamin E in protection of biological membranes,
Fed. Proc. 34: 2090-2095.
DANIEL, W.W. 1978. Applied nonparametric statistics.
Houghton Mifflin Company, Boston.
DOMÈNECH, J.M. 1980. Bioestadística. 3a. ed.,
Editorial Herder, Barcelona.
EGAÑA, J.I., H.E. VICENT, F. SQUELLA, M. MAINO,
R. BRAVO. 1987. Evaluación nutricional mineral de vacas Hereford alimentadas
con praderas naturales del secano costero central de Chile, Avances en Ciencias
Veterinarias 2: 13-19.
EICKEN, K., H. SCHOLZ, N. STOCKHOFE-ZURWlEDEN.
1992. Mangelhafte Selen- und Vitamin-E- Versorgung als Ursache für bestandsweise
auftretende Peritarsitiden beim Rind, Tierärztl. Umschau. 47: 843-847.
GRANT, A.B., A.D. SHEPPARD. 1983. Selenium
in New Zealand pasture, N. Z. Vet. J. 31:131-136.
HAARDT, E., J. POTOCNJAK, A. LOPEZ, S. CORNEJO.
1976. Survey model applied to mineral study in forages for a country (Chile)
with a great versatility of ecological systems. En: 1st. International Symposium
Feed Composition, Animal Nutrient requirements and Computerization of Diets.
Logan, Utah, USA.
HAKKARAINEN, J., B. PEHRSON, J. TYÖPPÖ-NEN.
1987. Blood vitamin E, selenium and glutathione peroxidase concentrations in
heifers fed either on grass or on winter feed, J. Vet. Med. A. 34: 508-514.
HALLIWELL, B. 1992. Especies reactivas de
oxígeno en los sistemas vivos: procedencia, bioquímica y papel patógeno en el
hombre. En: CRYSTAL, R.G. y J.R. RAMON, 1992. Sistema GSH. Glutatión: eje de
la defensa antioxidante. Excerpta Medica. Medical Communications B.V., Amsterdam.
HOUSE, W.A., A.W. BELL. 1994. Sulfur and selenium
accretion in the gravid uterus during late gestation in Holstein cows, J.
Dairy Sci 77: 1860-1869.
JAIN, N. C. 1986. Schalm's Veterinary hematology.
4th. ed., Lea & Febiger, Philadelphia.
JUKOLA, E. 1994. Selenium, vitamin E, vitamin
A and beta-carotene status of cattle in Finland, with special reference to epidemiological
udder health and reproduction data. Academic Dissertation. College of Veterinary
Medicine, Section of Animal Hygiene. Helsinki, Finland. Swedish University of
Agricultural Sciences, Faculty of Veterinary Medicine, Uppsala, Sweden.
KIRK, J.H., R.L. TERRA, I.A. GARDNER, J.C.
WRIGHT, J.T. CASE, J. MAAS. 1995. Comparison of maternal blood and foetal liver
selenium concentrations in cattle in California, Am. J. Vet. Res. 56:1460-1464
KNIGHT, S.A., R.A. SUNDE. 1988. Effect of
selenium repletion on glutathione peroxidase protein level in rat liver, J.
Nutr. 118: 853-858.
McDOWELL, L.R. 1992. Minerals in human and
animal nutrition. Academic Press, Inc., San Diego.
MEE J.F., K.J. OFARRELL, P.A.M. ROGERS. 1994.
Base-line survey of blood trace element status of 50 dairy herds in the South
of Ireland in the spring and autumn of 1991, Irish Vet. J. 47: 115-122.
MILLER, J.K., E. BRZEZINSKA-SLEBODZINSKA,
F.C. MADSEN. 1993. Oxidative stress, antioxidants and animal function, J
Dairy Sci 76: 2812-2823.
PAGLIA, D.E., W.N. VALENTINE. 1967. Studies
on the quantitative and qualitative characterisation of erythrocyte glutathione
peroxidase, J. Lab. and Clin. Med. 70: 158-169.
PEARSON, E.S., M.A. STEPHENS. 1964. The ratio
of range to standard deviation in the same normal sample, Biometrika
51: 484-487.
RANDOX. 1990. Ransel: Glutathione peroxidase.
Technical brief. Randox Laboratories. Ltd., Crumlin, U.K.
RICCIARDINO, M.Z., P.D. MEDUS, M. GOMEZ, B.E.
RUKSAN. 1991. Deficiencia de cobre y selenio en vaquillonas sobre pastura natural.
I. Causas y efectos inherentes a la pastura, Prod. Anim. 3: 213-221.
VAN SAUN, R.J. 1990. Rational approach to
selenium supplementation essential, Feedstuffs 15: 15-17.
WEISS, W.P., V.F. COLENBRANDER, M.D. CUN-NINGHAM.
1984. Maternal transfer and retention of supplemental selenium in neonatal calves,
J. Dairy Sci. 67: 416-420.
WHITAKER, D.A., J.M. KELLY. 1994. Use and
interpretation of metabolic profiles in dairy cows En: I Curso de Divulgación
en Técnicas de RIA y Evaluación de metabolitos Sanguíneos y Cinéticas Digestivas
Relacionadas en la Nutrición y Reproducción de Bovinos. Maracay, Venezuela.
WICHTEL, J.J., A.L. CRAIGIE, H. VARELA-ALVAREZ,
N.B. WILLIAMSON. 1994. The effect of intra-ruminal selenium pellets on growth
rate, lactation and reproductive efficiency in dairy cattle, N. Z. Vet. J.
42: 205-210.
WICHTEL, J.J., D.A. FREEMAN, A.L. CRAIGIE,
H. VARELA-ALVAREZ, N.B. WILLIAMSON. 1996. Alpha-tocopherol, selenium and polyunsaturated
fatty acid concentrations in the serum and feed of spring-calving dairy heifers,
N. Z. Vet. J. 44: 15-21.
WITTWER, F.G., P.A. CONTRERAS, H. BÖHMWALD,
R. ANRIQUE, R. FUCHSLOCHER. 1988. Concentraciones de zinc y cobre en forrajes
y suero sanguíneo de 40 predios lecheros de la X Región, Chile, Arch. Med.
Vet. 20: 118-125.
![]() ± DE*
± DE*
