G. VALENZUELA1, M. V., M. V. Sc.; I. QUINTANA1, T.M., Prof. Biol. y Quím.
1Instituto de Patología Animal, Facultad
de Ciencias Veterinarias, Universidad Austral de Chile, Casilla 567,
Fax: 56 63 218918, Valdivia, Chile.
SUMMARY
Development of Fasciola hepaticaeggs in outdoor temperatures in Temuco, southern Chile
A two-year study on the development of Fasciola hepatica eggs under outdoor conditions was carried out in Temuco, southern Chile (38-41S, 72-25W). Eggs obtained from bile of infected cattle were placed in buckets in a medium of distilled water once a month, and examined at monthly intervals, until 50% had hatched. The shortest period of development was 37 days in eggs placed outside in January, 1990. The longest period required for development was 249 days for eggs placed outside in April 1988. Eggs placed outside in March failed to hatch in autumn and remained viable throughout the winter; most of them hatched in October or November. It was proved that liver fluke eggs do not have a parallel development and that the time taken to hatch vary within each sample. The hatching stage only occurred when the mean temperature was more than 10° C. It can be concluded that in outdoor conditions, the development time is influenced by environmental temperature, latitude of the habitat and that no hatching occurs below an average temperature of 10° C.
Palabras claves: Fasciola hepatica, huevos, evolución, medio ambiente.
Key words: Fasciola hepatica, eggs, development, outdoor conditions.
INTRODUCCION
De acuerdo a la única información disponible respecto de las principales enfermedades parasitarias diagnosticadas en las plantas faenadoras de carne de Chile, la fasciolosis hepatica presenta los siguientes porcentajes de decomiso a nivel nacional: Bovinos, 32.4%, ovinos, 3.4%, porcinos, 2.0%, caprinos, 14.2% y equinos, 16.3% (Chile, 1989). De acuerdo a esta misma fuente de información, se considera la enfermedad parasitaria de mayor prevalencia con una tasa a nivel nacional para todas las especies de un 11.8%, superando a la hidatidosis, cisticercosis y triquinosis. El mismo informe señala que la fasciolosis se extiende en Chile desde la Primera hasta la Decimoprimera Región, siendo las zonas de mayor prevalencia las comprendidas entre la Cuarta y Novena Regiones.
A las pérdidas representadas por el decomiso de hígados, se deben agregar las provocadas por baja productividad tanto en leche como en carne (Chirinos y De Chirinos, 1991; Acosta y col., 1991; Spence y col., 1992; Echevarría y col., 1992). Esta baja productividad en carne se ha observado también en bovinos menores de un año (Acosta y col., 1991). Por su parte, en Chile se registran, además, infecciones en el hombre (Apt y col., 1988).
En el Frigorífico de Temuco S.A. de la IX Región (Chile, 1996), se beneficiaron en el período 1985-1994, 440.520 bovinos. De éstos, a 153.662, es decir, 34.7%, se les decomisó el hígado por fasciolosis. Tomando como ejemplo un bovino de 13 meses de edad, cuyo hígado pesa aproximadamente 5.3 kg, de acuerdo a Gallo (1990), significa una pérdida de 814.409 kg que no llegaron a consumo humano.
A pesar de la alta disponibilidad en nuestro país de un amplio número de antiparasitarios (Valenzuela, 1994), la infección en el bovino no parece disminuir, esto porque el control, además, debe considerar estudios de factores biológicos, climáticos, topográficos, que de acuerdo a Boray y col. (1969) favorecen la presentación de esta parasitosis. Estos antecedentes demuestran la necesidad del estudio de la biología del parásito en las diversas regiones del país para llevar a cabo planes de control. Estos estudios deben ser regionales, sobre todo en nuestro país, cuya longitud permite la presentación de una amplia variedad de climas.
Chile de norte a sur se divide en zonas con diversos regímenes hídricos y de temperatura, correspondiendo al lugar de la investigación un clima mediterráneo (Chile, 1989). Según Pantelouris (1965) y Ollerenshaw (1971), la temperatura es un factor importante en la evolución de los huevos de Fasciola hepatica.
Estudios de desarrollo de huevos de F. hepatica en el medio ambiente
en Chile corresponden a los realizados por Valenzuela
(1979). Dicho autor observó en la X Región prolongación
del tiempo de desarrollo en huevos colocados en el medio ambiente en el mes
de abril y comienzo de la eclosión de ellos en el mes de septiembre.
La eclosión de los huevos siempre se observó en meses con temperaturas
medias mensuales sobre 10° C, siendo masiva en el mes de septiembre. Por
su parte, Rubilar (1990), en la VIII Región
y Alcaíno y col. (1993)
en la VII Región observaron los primeros huevos eclosionados en el mes
de junio y agosto, respectivamente.
El propósito del presente trabajo fue determinar el tiempo de desarrollo
de huevos de F. hepa-tica en el medio ambiente de la IX Región
de Chile.
MATERIAL Y METODOS
Los huevos de F. hepatica se obtuvieron de bilis de bovinos. El contenido de 4 a 5 vesículas se pasó a través de un embudo con filtro de 60 hilos por pulgada hacia una probeta de 2.000 ml. Se agitó la bilis con una bagueta y se completa con agua hasta los 2.000 ml. Se dejó sedimentar por 3 horas y se eliminó un litro de sobrenadante. Se completó nuevamente la probeta con agua hasta los 2.000 ml y se dejó sedimentar nuevamente por 3 horas. Este procedimiento se repitió por 4 a 5 veces, hasta obtener un sedimento lo más claro posible.
El sedimento se colocó cada vez en dos vasos de 200 ml, con el objeto de tener un duplicado para resolver problemas de ruptura, pérdidas, etc., de alguno de ellos.
Los vasos fueron colocados en un sistema de flotación de acuerdo a Valenzuela y Sievers (1978).
Con el objeto de hacer más estrecha la relación huevo-hábitat, el sistema se mantuvo en canales determinados como hábitat de caracoles de la especie Limnaea viatrix.
Los huevos se examinaron mensualmente al microscopio, y el período de
observación de cada muestra se consideró el período comprendido
entre la colocación de los huevos en el medio ambiente hasta que se observó
el 50% de los huevos eclosionados. Las observaciones se realizaron entre abril
de 1988 y febrero de 1990.
Datos climáticos de temperatura media mensual fueron proporcionados por
la estación meteorológica INIA Carillanca.
RESULTADOS
El tiempo de desarrollo para las diferentes muestras se presenta en el cuadro 1 y figura. 1.
En el primer año la muestra colocada en el ambiente en el mes de abril prolongó su desarrollo, siendo éste de 249 días. Sin embargo, el segundo año en que las observaciones se iniciaron en el mes de enero, prolongó su desarrollo la muestra colocada en el mes de marzo, siendo su período de evolución de 216 días.
El período más corto de desarrollo fue de 37 días y correspondió a la muestra colocada en el mes de enero de 1990, y de 54 días, a la muestra colocada en enero de 1989.
Se observa que los tiempos más largos de desarrollo corresponden a las muestras colocadas en otoño e invierno y los más cortos a los meses de primavera y verano.
Tiempo de desarrollo de huevos de Fasciola hepatica, temperatura media
mensual y pluviosidad para
Temuco, IX Región. Período 1988-1990.
Development time of Fasciola hepatica eggs, average of temperature
and rainfall for Temuco, IX Region of Chile.
From 1988-1990.
|
|
||||
|
Desarrollo (días)
|
T.M.M. (°C)
|
Pluviosidad (mm)
|
||
|
|
||||
|
|
Enero Febrero Marzo Abril Mayo Junio Julio Agosto Septiembre Octubre Noviembre Diciembre |
|
18.5 14.6 11.9 8.7 7.1 5.5 7.7 9.2 10.4 13.3 15.0 |
0.0 114.5 29.8 106.1 214.7 124.0 181.9 55.1 145.6 32.6 47.3 |
|
|
Enero Febrero Marzo Abril Mayo Junio Julio Agosto Septiembre Octubre Noviembre Diciembre |
58 216 178 146 144 120 119 58 96 61 70 |
17.4 13.9 11.3 8.8 8.1 7.2 7.9 9.3 11.2 13.6 15.5 |
21.0 56.0 28.4 77.5 273.0 236.3 207.7 60.4 51.8 21.8 171.7 |
|
|
Enero Febrero Marzo Abril |
56
|
17.3 14.2 10.9 |
55.1 130.6 106.3 |
|
|
||||
DISCUSION
El efecto de la temperatura sobre el desarrollo de los huevos de F. hepatica fue observado primero por Thomas 1883 (citado por Pantelouris, 1965), quien concluyó que ciertas temperaturas eran más favorables para el desarrollo de los huevos. En investigaciones posteriores se demostró que a temperaturas inferiores a 10° C no se producía desarrollo ni eclosión de los huevos (Ross y McKay, 1929; Rowan, 1956), como tampoco desarrollo de estados larvarios en el caracol, huésped intermediario, ni la emergencia de las cerca-rias desde los mismos (Ollerenshaw, 1971a).
En la presente investigación se comprobó que los huevos colocados en el mes de abril prolongaron su desarrollo durante los meses de invierno, esto se debió a que recibieron la influencia de un solo mes con temperaturas adecuadas para la eclosión, abril 1988, por lo tanto insuficiente (cuadro 1).
Ollerenshaw (1971a), en Inglaterra, observó eclosión antes del período de invierno en huevos colocados en septiembre, lo que estacionalmente correspondería al mes de marzo en el hemisferio sur; lo mismo fue observado por Valenzuela (1979) en Valdivia.

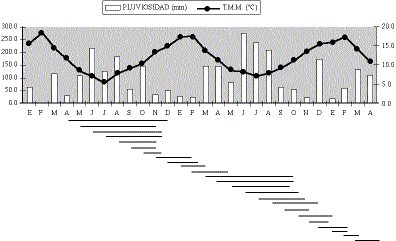
Figura 1. Evolución de huevos de Fasciola hepatica. Temuco, IX Región. 1988-1990.
Development of Fasciola hepatica eggs. Temuco, IX Región. 1988-1990.
En la figura 1 se observa el desarrollo de los huevos a fines de otoño y durante el invierno. Se aprecia una lenta variación en el desarrollo. En todas las muestras colocadas en este período el desarrollo se prolongó en los meses fríos y se fue acortando gradualmente a medida que se fue acercando el período de primavera.
Rowcliffe y Ollerenshaw (1959) observaron desarrollo en el ambiente a temperaturas inferiores a 10° C, por ello señalan que 10° C es más inadecuado para la eclosión de los huevos, que para el desarrollo mismo; además, Borchert (1964) señala que la segmentación del huevo se inicia ya a temperaturas que fluctúan entre 8 y 12° C.
Esto ha sido observado en Chile por Rubilar (1990), en Chillán, y por Alcaíno y col. (1993) en Teno, en que hubo desarrollo en los meses de invierno. Esto se explica porque en dichos meses hubo temperaturas superiores a 10° C en algunos días.
El tiempo de desarrollo fue mayor en Temuco, IX Región, de 250 días comparados con 154 obtenidos en Teno, VII Región, por Alcaíno y col. (1993).
En el segundo año, los huevos colocados en el mes de marzo prolongaron su desarrollo. Esto fue observado también en Teno, VII Región, por Alcaíno y col. (1993). Los registros climáticos indican dos meses con temperaturas favorables para la eclosión, pero insuficientes para completar el desarrollo marzo y abril del segundo año (cuadro 1).
Luego, en el período de bajas temperaturas, el desarrollo se prolonga, siendo de 250 días en Temuco y 154 días en Teno, debido a que el promedio mensual de temperatura en este período fue de 10° C.
Ollerenshaw (1971b), en condiciones de laboratorio a temperatura constante, observó que a 10° C no se produce desarrollo en los huevos. Por su parte, Rowcliffe y Ollerenshaw (1959) señalan que en el medio ambiente se puede considerar como temperatura crítica el valor de 9.05 ± 0.5° C. Valenzuela y col. (1979) observaron en Valdivia, X Región, desarrollo de huevos bajo la temperatura de 10° C, pero eclosión de huevos sólo sobre ella.
En lo que respecta a la eclosión de los huevos, ésta comenzó en aquellos meses con temperaturas sobre 10° C o cercanas a ellas (figura 1).
La eclosión de los huevos que se desarrollan durante el invierno se concentra principalmente en octubre y noviembre en la IX Región. Alcaíno y col. (1993) lo observaron en septiembre en la VII Región.
En el trabajo de Rowcliffe y Ollerenshaw (1959), el comienzo de la eclosión ocurrió en junio, lo que estacionalmente corresponde a diciembre en el hemisferio sur, es decir, en el período más tardío, esto, debido a que las temperaturas en el hemisferio norte, durante la experiencia, fueron más bajas que las registradas en la presente investigación.
En Valdivia, X Región, Valenzuela (1979) observó eclosión en septiembre y en otro trabajo en octubre y noviembre (Valenzuela y col., 1979).
Luego se observa, en ambos años, que el tiempo de desarrollo se acorta gradualmente al acercarse la estación de primavera.
Esto fue observado por Rowcliffe y Ollerenshaw (1959), en Inglaterra. Se debe destacar que el período más corto de desarrollo se observó en los huevos colocados en el mes de enero de ambos años, siendo de 37 días a 15.9° C en enero de 1990, lo cual coincide con lo observado por Valenzuela (1979), en Valdivia, X Región, Alcaíno y col. (1993), en Teno, VII Región, y Rubilar (1990), en Chillán, VIII Región. A fines de verano y comienzos de otoño, el tiempo de desarrollo se alarga. Los huevos colocados hasta el mes de marzo producen miracidios antes de otoño e invierno. Esto coincide con lo observado por Valenzuela (1979), Alcaíno y col. (1993) y Rubilar (1990). Cabe hacer notar que este último autor observó que el tiempo de desarrollo en invierno fue menor que lo observado por los otros autores.
RESUMEN
Se realizó un estudio de desarrollo de huevos de Fasciola hepatica en el medio ambiente en Temuco, Novena Región de Chile (38-41S y 72-25W). Las observaciones se realizaron desde abril de 1988 hasta junio de 1990. Los huevos obtenidos de vesículas de bovinos infectados con el parásito fueron colocados una vez al mes en vasos con agua destilada, en un sistema flotante. El sistema flotante se mantuvo en canales, en hábitat del parásito. Las muestras fueron examinadas una vez al mes hasta obtener el 50% de los huevos eclosionados. El tiempo de desarrollo más largo fue de 249 días en las muestras colocadas en abril de 1988 y el más corto, de 37 días, en las colocadas en enero de 1990. Los huevos colocados en el ambiente en marzo no eclosionaron hasta después del invierno, en octubre o noviembre. Se comprobó que los huevos no tienen un desarrollo paralelo. Se concluye que el desarrollo en el medio ambiente es influenciado por la temperatura ambiental, que varía de acuerdo a la latitud geográfica del hábitat, y que no hay eclosión de huevos a temperaturas medias inferiores a 10° C.
AGRADECIMIENTOS
Al Fondo de Investigaciones Agropecuarias, FIA; por proporcionar financiamiento
para esta investigación, al Sr. Euclides Aravena por permitir el desarrollo
de este trabajo en su predio agrícola, al Sr. Mario Olivares G., Médico
Veterinario, por su coordinación en actividades prediales, a INIA Carillanca,
por proporcionar los datos del clima.
______________________________________________
Aceptado: 08.01.98.
* Financiado por el Fondo de Investigaciones
Agrope-
cuarias, FIA, Proyecto 064/85.
BIBLIOGRAFIA
ACOSTA, D., H. CARDOZO, A. NARI, J. ETCHEBARNE. 1991. Impacto en el incremento de peso en los terneros infectados experimentalmente al destete con Fasciola hepatica. X Congreso Latinoamericano de Parasitología. I Congreso Uruguayo de Parasitología. 17-22 noviembre, Montevideo, Uruguay.
ALCAINO, H., F. VEGA, T. GORMAN. 1993. Epidemiología de la Fasciolasis hepatica en la VII Región, Chile, Parasitol. al Día 17: 99-106.
APT, W., P. KLEIN, F. VEGA, H. ALCAINO, C. RETAMAL. 1988. Fasciolasis humana en la población rural de la provincia de Curicó (VII Región). Chile, Parasitol. al Día 12: 155-164.
BORAY, J.C., F.A. HAPPICH, J.C. ANDREWS. 1969. The epidemiology of fasciolasis in two representative endemic regions in Australia, Aust. Vet. J. 45: 549-553.
BORCHERT, A. 1964. Parasitología Veterinaria. 3ª edición, Acribia, Zaragoza.
CHILE. MINISTERIO DE SALUD PUBLICA. 1989. Información estadística de las principales enfermedades registradas en los animales beneficiados en los mataderos del país durante el año 1988. Ordinario 5877.
CHILE. 1989. Mapa Agroclimático de Chile. Instituto de Investigaciones Agropecuarias, INIA, Ministerio de Agricultura.
CHILE. 1996. Frigorífico Temuco S.A. Informe de decomisos causados por algunas zoonosis parasitarias más frecuentes en bovinos, durante los años 1984-1994.
CHIRINOS, A.R., N.I. DE CHIRINOS. 1991. Evaluación de los efectos de la distomatosis hepatica sobre la eficiencia reproductiva y producción lechera. X Congreso Latinoamericano de Parasitología. Montevideo, Uruguay. 17-22, noviembre.
ECHEVARRIA, F.A., M.B. CORREA, R.D. WEHRLE, I.F. CORREA. 1992. Experiments on anthelmintic control of Fasciola hepatica in Brazil, Vet. Parasitol. 43 (3-4): 211-222.
GALLO, C., J.A. DE LA VEGA, M. PARRA. 1990. Antecedentes sobre el valor cárnico de diferentes especies en Chile. Informativo sobre carne y productos cárnicos. Instituto de la Carne, UACH 19: 1-54.
OLLERENSHAW, C.B. 1971a. Forecasting liver fluke disease in England and Wales 1958-1968 with a comment on the influence of climate on the incidence of the disease in some other countries, Vet. Med. Rev. 2/3: 289-312.
OLLERENSHAW, C.B. 1971b. Some observation on the epidemiology of Fasciolasis in relation to the timing of Molluscicide applications in the control of the disease, Vet. Rec. 88 (6): 152-164.
PANTELOURIS, E.M. 1965. The common liver fluke. Pergamon Press, London.
ROSS, I.C., A.C. McKAY. 1929. The bionomics of Fasciola hepatica in New South Wales and the intermediate host Limnaea brazieri, Bull. Coun. Sci. Industs. Res. Aust. 5: 1-63 (citado por Pantelouris, 1965).
ROWAN, W.B. 1956. The mode of hatching of the egg of Fasciola hepatica, Exp. Parasit. 5: 118-137.
ROWCLIFFE, S.A., C.B. OLLERENSHAW. 1959. Observations on the bionomics of the eggs of Fasciola hepatica, Ann. Trop. Med. Parasit. 54: 172-181.
RUBILAR, L. 1990. Estudio de un sistema predictivo de infestaciones por Distomatosis 1987-1990. Proyecto FIA, 064/85. Informe Técnico Final.
SPENCE, S.A., G.C. FRASER, E.B. DETTMANN, D.F. BATTESE. 1992. Production responses to internal parasite control in dairy cattle, Aust. Vet. J. 69 (9): 217-220.
VALENZUELA, G. 1979. Estudio epidemiológico acerca del desarrollo de huevos de Fasciola hepatica en el medio ambiente en Valdivia, Chile, Bol. Chile Parasit. Vol. 34 (1-2): 31-35.
VALENZUELA, G. 1994. Terapéutica de Distoma-tosis. Seminario Terapéutica Antiparasitaria. Colegio Médico Veterinario, Consejo Regional Valdivia, Valdivia, julio, 1994.
VALENZUELA, G., G. SIEVERS. 1978. Un sistema práctico para cultivo de huevos de Fasciola hepatica, Bol. Chile Parasit. 32 (3 y 4): 84.
VALENZUELA,
G., I. FUENTEALBA, O. HENRI-QUEZ. 1979. Acción de la temperatura ambiente
sobre el desarrollo de huevos de Fasciola hepatica en Valdivia, período
invierno-primavera, Arch. Med. Vet. Suplemento 1: 134-139.