COMUNICACIONES
RATTO, M., MV, MSc; M. BERLAND, Prof. Biol; M. WOLTER, Lic. MV; R. MATAMOROS, MV, MSc, PhD.
Escuela de Medicina Veterinaria, Universidad Católica de Temuco, Casilla 15-D, Temuco, Chile.
The in vitro development of matured and fertilized bovine oocytes was compared between two culture systems. Oocytes were collected by aspiration of follicles of 3-8 mm in diameter using an 18g needle. After morphological selection the oocytes were incubated at 39 0C, 5 % C02 y 95 % relative humidity, during 22 hours. Afterwards, oocytes were incubated with spermatozoa selected by Percoll gradient system. The rate of nuclear maturation and fertilization was 93,7 % (74/79) and 76,9 % (50/65), respectively. A total of 252 zygotes were cultured, 102 with oviductal cells and 150 in conditioned medium. The in vitro development on day 2 of culture (4- or 8-cell embryos) was 62,7 % (64/102) for the zygotes co-cultured with oviductal cells and 66,7 % (100/150) for the zygotes cultured in conditioned medium. The development to the morula stage was 17,6 % (18/102) for the zygotes co-cultured with oviductal cells and 13,3 % (20/150) for the zygotes cultured in conditioned medium. A statiscally significant difference was not found in the development of 4, 8-cell embryos or morula. The development of embryos up to the blastocyst stage was 15,7 % (16/102) for the zygotes co-cultured with oviductal cells. Two blastocysts were transferred to the uterine horn ipsilateral to the CL in two recipients by non-surgical embryo transfer. Pregnancy was confirmed by ultrasonography at 42 and 57 days detecting the presence of one conceptus in each animal. This work has shown that in vitro inseminated of bovine oocytes with espermatozoa prepared with modified BO and co-cultured with oviductal cells, can develop to the blastocysts stage, unlike those that were cultured with conditioned medium. Finally, it is important to mention that this is the first communication in Chile of pregnancy after in vitro fertilization of bovine oocytes.
Palabras claves: preñez, fecundación in vitro, bovinos
Key words: pregnancy, in vitro fertilization, bovine
INTRODUCCION
La fecundación in vitro es de gran apoyo en el desarrollo de técnicas que tienen un potencial importante en la reproducción animal, tales como la micromanipulación de embriones, producción de quimeras y animales transgénicos. El desarrollo de esta biotecnología permite la producción de embriones hasta estadíos avanzados compatibles con la transferencia a hembras receptoras (First y Parrish, 1987). En los últimos años con el desarrollo de métodos que facilitan la colección de ovocitos directamente de animales vivos, la producción de embriones in vitro ha sido introducida en los programas de selección. (Kruip, 1991). Es importante destacar que esta técnica es la única opción disponible para producir crías de hembras valiosas que por causas no genéticas son estériles y por lo tanto son eliminadas de los sistemas productivos.
Desde el punto de vista biológico, el establecimiento de la fecundación in vitro es una alternativa valiosa para la investigación de los mecanismos celulares y moleculares involucrados en las interacciones gaméticas, fecundación y desarrollo embrionario temprano (Barros y Leal, 1982).
Es bien conocido que los cigotos pueden ser co-cultivados in vitro con células oviductales o en el medio previamente condicionado por estas células desarrollando hasta un 30% a blastocistos (Eyestone y First, 1989; Eyestone y col., 1990), no obstante, la capacidad de implantación de los mismos es variable luego de la transferencia en vacas receptoras (Bavister, 1995).
En Chile, son escasos los antecedentes relacionados con las tasas de desarrollo embrionario obtenidos a partir de ovocitos recolectados de vacas que van al sacrificio. Risopatron y col. (1989), obtuvieron una tasa de desarrollo de 42,6% de embriones de 4-8 células mientras que De los Reyes y col. (1996) comunicaron la obtención de embriones de 2-4 células a las 48 horas y blastocistos a los 7 días pero no mencionan el porcentaje de desarrollo obtenido.
El objetivo del presente trabajo fue comparar las tasas de desarrollo in vitro de ovocitos bovinos co-cultivados con células oviductales o medio condicionado, luego de ser madurados y fecundados in vitro.
MATERIAL Y METODOS
Colección de ovarios y maduración in vitro de ovocitos. Los ovarios fueron obtenidos en el matadero y transportados dentro de una hora posterior al sacrificio de los animales, en un termo a 35°C con una solución salina fisiológica al 0,85 %, suplementada con 100 UI/ml de penicilina y 100 µg/ml de estreptomicina. Los ovocitos fueron aspirados mediante punción de folículos de 3 a 8 mm de diámetro por medio de una aguja 18-g acoplada a una jeringa de 10 ml. El contenido de la aspiración fue colectado en tubos plásticos de 15 ml, el cual se dejó decantar por 5 minutos mantenido en un baño de agua a 39 °C. Luego con pipeta Pasteur se aspiró el fondo del tubo colocando el material en placas Petri plásticas Falcon 10071. Se procedió a la búsqueda y selección de los complejos cúmulo-ovocito (CCO) por medio de un microscopio estereoscópico a un aumento de 15x. Solamente ovocitos rodeados por un cúmulo compacto y citoplasma homogéneo fueron utilizados para el cultivo (Leibfried y First, 1979). Previo a la maduración, los ovocitos fueron lavados manualmente con pipeta Pasteur 3 veces en 2 ml de fosfato buffer salino (FBS2) suplementado con 100 UI/ml penicilina-100 µg/ml de estreptomicina y albúmina bovina sérica 0,3 % (BSA fracción V2) y 3 veces con 2 ml de medio de maduración constituido por TCM 199 (M1992) suplementado con suero fetal bovino inactivado 10 % (SFB2), hormona folículo estimulante3 0,08 m g/ml (NIH-FSH-P1); estradiol 1µg/ml; piruvato de sodio4 0,2 mM; sulfato de gentamicina4 50 µg/ml (Saeki y Col. 1991).
De 10 a 12 ovocitos fueron colocados en gotas de 50µl de medio depositadas en una placa de Petri plástica Falcon 10071, las cuales fueron cubiertas con aceite mineral y finalmente incubadas a 39 °C, CO2 al 5 % y humedad relativa de 95 % durante 22 horas. Luego de este período, una muestra de los ovocitos fue teñida con orceína acética al 1 % para verificar maduración nuclear (metafase y primer corpúsculo polar).
Preparación del semen para la fecundación. El semen fue procesado de manera similar a lo descrito por Takahashi y First (1992). Se utilizó semen de un mismo toro, el cual fue descongelado y centrifugado durante 30 minutos a 700g utilizando una gradiente discontinua de Percoll4 (45/90%) preparada con medio BO modificado (Brakett y Oliphant, 1975). Posteriormente, se extrajo el sobrenadante y el pellet se suspendió con medio BO modificado a una concentración de 5x106 espermatozoides/ml.
Inseminación in vitro. Luego de 22 horas de cultivo, los ovocitos fueron lavados 3 veces en una solución de BO modificada que contenía 12 mg/ml de albúmina bovina sérica, libre de ácidos grasos (BSA Fatty-Acid-free4) y 10 mM de cafeína4 (medio de fecundación). Con este mismo medio se depositaron gotas de 45 µl (gotas de fecundación) en una placa de Petri plástica Falcon 10071, las cuales fueron cubiertas con aceite mineral. Posterior al lavado de los CCO, se tomaron 15 ovocitos en un volumen de 5 µl y fueron colocados en las gotas de fecundación. Finalmente, se agregó a la gota 50 µl del semen procesado alcanzando un volumen final de 100 µl, una concentración espermática de 2,5x106 espermatozoides/ml, una concentración final de 6mg/ml de BSA F-Acid-free y 5mM de cafeína. Los CCO con espermatozoides fueron co-cultivados a 39°C, CO2 al 5% y una humedad relativa de 95 % durante 18 horas. Luego de este período, una muestra de estos ovocitos fue teñida con orceína acética al 1 % con el fin de determinar las tasas fecundación de acuerdo a la presencia de 2 pronúcleos y cola de espermatozoide ( Sirard y col., 1989).
Preparación de las células oviductales. El mismo día que se obtuvieron los CCO, se prepararon las células oviductales a partir de oviductos transportados en bolsas plásticas sobre hielo desde el matadero, la técnica fue similar a la utilizada por Carvalho y col. (1996). En el laboratorio, los oviductos fueron lavados con solución salina fisiológica, eliminando los ligamentos y la grasa que los rodeaba. El oviducto fue colocado sobre una placa de Petri y con un portaobjeto estéril se ejerció presión desde la unión útero-tubárica hasta el infundíbulum, obteniéndose un material de aspecto cremoso-amarillento, éste fue introducido en un tubo plástico Falcon 20951. Este material fue lavado 4 veces por decantación con TCM 199, enriquecido con 1 % de SFB y 50 µg/ml de gentamicina. Finalmente, fue suspendido en 10 ml del mismo medio, pero suplementado al 10 % de SFB en un frasco plástico5 para cultivo e incubado durante 48 horas a 39°C, CO2 al 5 % y Humedad relativa de 95%. Luego del período de incubación, se realizaron 2 lavados adicionales y se introdujo 1µl de esta suspensión a gotas de 100 µl de medio de cultivo, incubándose bajo las condiciones descritas. La presencia de motilidad en un 70 % o más de las vesículas de células oviductales fue considerada como un signo de viabilidad y aptas para el cultivo.
El medio en el cual habían sido cultivadas las células oviductales durante 48 horas fue centrifugado, filtrado y utilizado para el cultivo de los ovocitos fecundados (medio condicionado).
Cultivo in vitro. Finalizado el período de fecundación, los CCO fueron colocados en un tubo de 1ml agitándolo por 3 minutos con el fin de sacarles las células foliculares y finalmente se cultivaron, en las gotas con las células oviductales o en las gotas del medio condicionado, a 39°C, 5 % de CO2 y humedad relativa de 95 % durante 8 días. Se evaluó la división celular a los dos días después de la inseminación (día 0: inseminación in vitro) y al día 6, 7 y 8 de cultivo.
Evaluación de la viabilidad de los embriones in vivo. Cuatro blastocistos obtenidos in vitro el día 7 fueron transferidos, mediante técnica no quirúrgica a dos vacas sincronizadas con una dosis de 33,5 mg de Dinoprost Trometamina, análogo de Prostaglandina F2 a , considerando la detección del estro como día 0. De acuerdo a lo descrito por Goto y col. (1989), cada animal recibió 2 embriones en el cuerno ipsilateral al ovario que presentaba un cuerpo lúteo. El diagnóstico de gestación fue realizado mediante ecografía a los 42 y 57 días post-trasferencia. Se consideró como signo de gestación la presencia fetal.
Análisis estadístico. Los resultados del desarrollo embrionario in vitro fueron comparados por un análisis de Chi-cuadrado (tabla de contingencia) con la corrección de Yates por continuidad (Zar, 1996).
RESULTADOS Y DISCUSION
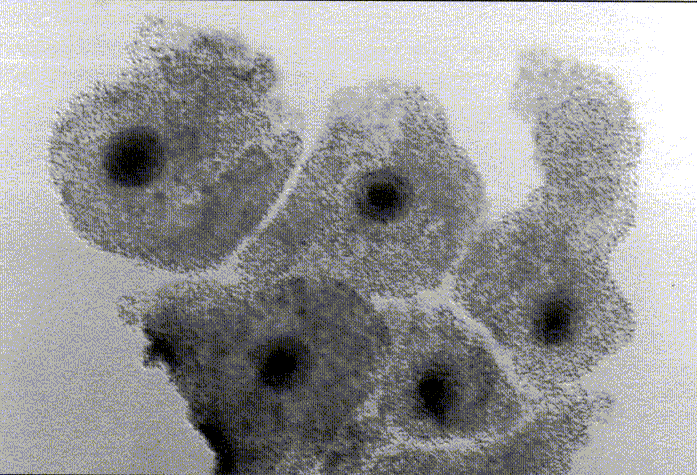
El porcentaje de maduración de ovocitos luego de 22 horas de cultivo fue 93,7 % (74/79; figura 1). El porcentaje de fecundación normal encontrado luego de las 18 horas de inseminación fue 76,9 % (50/65).

| Figura 1. Ovocitos con cúmulus expandidos 22 horas
post cultivo. Oocytes with cumulus after 22 hours of culture. |
|
Cultivo in vitro
|
|
N° de embriones (%)
|
||
|
Día 2
4-8 células |
Día 6
Mórulas |
Día 7-8 Blastocisto
|
||
|
Células Oviductales
Medio Condicionado
|
|
64 (62.7)
100 (66.7)
|
18 (17.6)
20 (13.3)
|
16 (15.7)
----
|
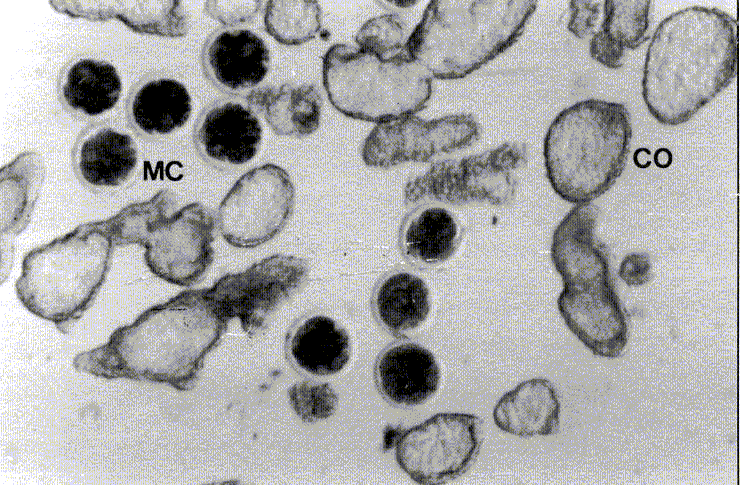
| Figura 2. Mórulas compactas (MC) de 5 días
co-cultivadas con células oviductales (CO). Five days-compact morulae (MC) co-cultured with oviductal cells (CO). |
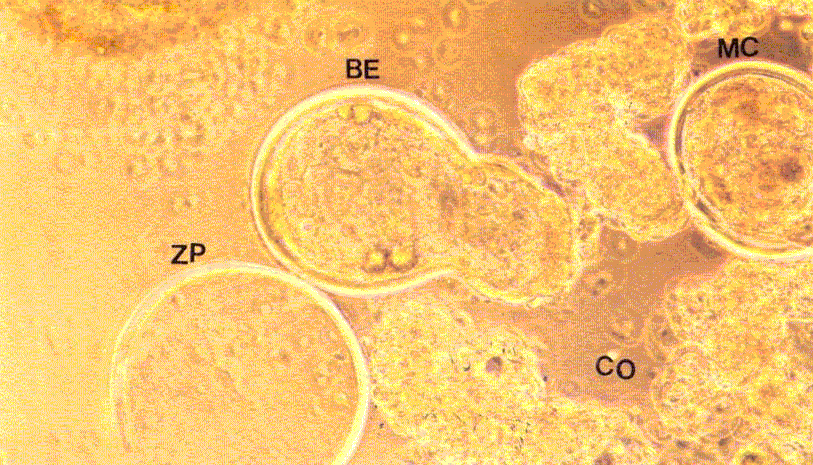
| Figura 3.Blastocisto en eclosión (BE) al día
8 de cultivo. Zona pelúcida (ZP). Mórula Compácta
(MC). Célula Oviductal (CO). Hatching blastocyst (BE) at 8 days of culture. Pellucidae zonae (ZP). Compact Morulae. Oviductal cell (CO) |
La ecografía reveló la presencia de un sólo feto en cada hembra con signos normales de desarrollo (figura 4).
Los resultados de este estudio confirman lo establecido por otros investigadores quienes indican que factores provenientes tanto de células somáticas, como de medio condicionado, pueden evitar el bloqueo in vitro del embrión bovino al estadío de 8-16 células (Eyestone y First, 1989). Se ha planteado que estas células actuarían en el desarrollo secretando factores de crecimiento (factores embriotróficos) y produciendo una detoxificación del medio de cultivo (Bavister, 1995). En el presente estudio las tasas de maduración y fecundación in vitro de ovocitos de bovinos fueron similares a las descritas por Parrish y col. (1995), Avery y Greve (1995) y más elevadas al compararlas con las obtenidas por Risopatrón y col. (1991) y De los Reyes y col. (1996).
Asimismo el porcentaje de desarrollo a los 2 días post-inseminación (embriones de 4-8 células) fue similar al descrito por Parrish y col. (1995), superando el valor obtenido por Risopatrón y col. (1991). Sin embargo, el desarrollo del 15,7 % de blastocistos sobre el total de ovocitos cultivados con células oviductales, fue más bajo al compararlo con los resultados obtenidos en otros estudios (Takahashi y First, 1992; Avery y Greve, 1995, Carvalho y col. 1995).
Para la realización de los cultivos oviductales no se tomó en cuenta el estado fisiológico del animal al momento de extraer los oviductos, tal como presencia en el ovario ipsilateral de un folículo preovulatorio o cuerpo lúteo hemorrágico; no obstante, se consideró como signo de viabilidad la motilidad de las células oviductales, la que se mantuvo durante los 10 días de cultivo. Por otra parte, otros autores utilizan células oviductales sin tomar en cuenta el estado fisiológico del animal logrando tasas de desarrollo de blastocistos mayores a 25 % (Sirard y Blondin, 1996).
La baja tasa de desarrollo obtenida podría atribuirse a la selección de los complejos cúmulos-ovocitos previo a la maduración, etapa en la cual se debería ejercer una estricta evaluación sobre la calidad morfología tanto de las células de los cúmulos como en el ovoplasma (Sirard y Blondin, 1996). Se observó que las tasas de desarrollo tanto para embriones de 4 a 8 células cómo para mórulas fueron similares en ambos sistemas de cultivo, pero sólo se obtuvieron blastocistos a partir de ovocitos cultivados con células oviductales. Las razones para este fenómeno son por ahora desconocidas, no obstante en la literatura se encuentran resultados contradictorios que indican entre un 3 y 30 % de blastocistos producidos en cultivo con medio condicionado de células oviductales (Eyestone y Col., 1990; Pinyopummintr y Bavister, 1991). Además, en esos estudios se empleó una solución Tyrode modificada para el procesamiento y capacitación del semen bovino. En este contexto, resultados obtenidos por Jaakma y col. (1997), demuestran menores tasas de blastocistos cuando se utiliza el medio BO modificado para la preparación de los espermatozoides, en comparación a solución Tyrode modificado.
| Figura 4. Gestación en bovino 42 días post
transferencia. Utero (U), feto (F). Forty two days pregnancy in bovine after embryo transfer. Uterus (U), fetus (F). |
A pesar de haber transferido dos embriones por hembra, la preñez de ambas con un sólo feto coincide con lo descrito por otros autores utilizando la misma metodología (Goto y col., 1989; McMillan, 1996). Por otra parte confirma la viabilidad de los embriones obtenidos.
Es importante destacar que en Chile no hemos encontrado antecedentes de gestaciones
en bovinos logradas por la transferencia directa de embriones producidos in
vitro, por lo que este trabajo sería la primera comunicación
al respecto.
En conclusión, este estudio demuestra que la tasa de desarrollo para
embriones hasta el estadío de mórula, no varía por el sistema
de cultivo utilizado y solamente los cigotos cultivados con células oviductales
desarrollan hasta el estadío de blastocistos , siendo estos viables al
ser transferidos a hembras receptoras.
RESUMEN
Se comparó el desarrollo in vitro de ovocitos obtenidos
de ovarios de vaca de matadero, madurados, fecundados y cultivados in
vitro bajo dos sistemas. Los ovocitos fueron cultivados en un medio
de maduración a 39 °C, 5 % de CO2 y humedad relativa
de 95 % durante 22 horas. Posteriormente, fueron incubados con espermatozoides
seleccionados a través de una gradiente discontinua de Percoll.
La tasa de maduración nuclear y fecundación fueron de 93,7
% (74/79) y 76,9 % (50/65) respectivamente. Un total de 252
ovocitos fecundados fueron cultivados in vitro. El porcentaje de
desarrollo in vitro a las 2 días post-inseminación
(embriones de 4-8 células) fue de 62,7 % (64/102) para los cigotos
cultivados con células oviductales y de 67 % (100/150) para los
cultivados en medio condicionado (P>0,05). El porcentaje de desarrollo
de mórulas fue de 17,6 % (18/102) para los cigotos cultivados con
células oviductales y de 13,3 % (20/150) para los cultivados con
medio condicionado (P>0,05). Se obtuvo una tasa de desarrollo del 15,7
% (16/102) de blastocistos para aquellos cigotos cultivados con células
oviductales. No se obtuvo blastocistos a partir de cigotos cultivados en
medio condicionado. Cuatro blastocistos fueron transferidos a dos hembras
receptoras. A los 42 y 57 días se encontró la presencia de
un feto en cada hembra.
______________________________
Aceptado: 29.12.98
Fuente Financiamiento: DIUC 98-33-04
AGRADECIMIENTOS
Se agradece la colaboración brindada por el matadero de Temuco,
especialmente al Sr. Noe Riquelme y su personal, también se agradece
la asistencia técnica del Dr. Eduardo Angarita G y del Sr. Sebastián
Ratto V, y de los estudiantes de Medicina Veterinaria de la Universidad
Católica de Temuco, Rodrigo Rubilar y Maximiliano Bello.
________________________________________
1 Becton Dickinson, Nueva York, USA.
2 Gibco-BRL, Grand Island, NY, USA.
3 Vetepharm, London, Ontario, Canadá.
4 Sigma, St. Louis, ST, USA.
5 Nunc Inter Med, Dinamarca
BIBLIOGRAFIA
AVERY, B. T. GREVE. 1995. Impact of Percoll on bovine spermatozoa used for in vitro insemination. Theriogenology. 44: 871-878.
BARROS, C. J. LEAL. 1982. In vitro fertilization and its use to study gametes interactions, in vitro fertilization and embryo transfer. En: HAFEZ, E.S. y SEMM, K. 1982. International Medical Publishers. pp. 37-49.
BAVISTER, B.D. 1995. Culture of preimplantation embryos: facts and artifacts. Hum. Repr. Update. 1: 91-148.
BRACKETT, B.G. y G. OLIPHANT. 1975. Capacitation of rabbit spermatozoa in vitro. Biol. Reprod. 12: 260-274.
CARVALHO, R.V., M.R. DEL CAMPO, A.T. PALASZ, Y. PLANTE R.J. MAPLETOFT. 1996. Survival rates and sex of bovine ivf embryos frozen at different development stages on day 7. Theriogenology. 45: 489-498.
DE LOS REYES, M., C. ALMENDRA, M. BERLAND, H. DEL CAMPO C. BARROS. 1996. Selección de espermatozoides de toro para fecundación in vitro. Arch. Med. Vet. 1: 31-38.
EYESTONE, W.H. N.L. FIRST. 1989. Co-culture of early cattle embryos to the blastocyst stage with oviductal tissue or in conditioned medium. J. Reprod. Fertil. 85: 715-720.
EYESTONE, W.H., J.M. JONES N.L. FIRST. 1990. The use of oviduct-conditioned medium for culture of bovine oocytes to the blastocyst stage. Theriogenology. 33: 226.
FIRST, N.L. J.J. PARRISH. 1987. In vitro fertilization of ruminants. J. Reprod. Fertil. 34 (Suppl.): 151-170.
GANDOLFI, F., L. BREVINI R.M. MOOR. 1989. Effect of oviduct environment on embryonic development. J. Reprod. Fertil. 38 (Suppl.): 107-115.
GOTO, K., Y. KAJIHARA, S. KOSAKA, M. KOBA, Y. NAKANISHI K. OGAWA. 1988. Pregnancies after co-culture of cummulus cells with bovine embryos derived from in-vitro fertilization of in-vitro matured follicular oocytes. J. Reprod. Fertil. 83: 753-758.
JAAKMA, U., B.R. ZHANG, B. LARSSON, K. NIWA H. RODRIGUEZ-MARTINEZ. 1997. Effects of sperm treatments on the in vitro development of bovine oocytes in semidefined and defined media. Theriogenology 48: 711-720.
McMILLAN, W.H. 1996. Potential survival rates to term for transferred in vitro and in vivo derived bovine embryos. Theriogenolgy 45: 233.
KRUIP, T.A.M., R. BONI, Y.A. WURTH, M.W.M. ROELOFSEN M.C. PIETERSE. 1994. Potencial use of ovum pick-up for embryo production and breeding cattle. Theriogenology 42: 675-684.
LEIBFRIED, L. NL FIRST. 1979. Characterization of bovine follicular oocytes and their ability to mature in vitro. J. Anim. Sci. 48: 76-86.
PARRISH, J.J., A. KROGENAES J.L. SUSKO-PARRISH. 1995. Effect of bovine sperm separation by either Swin-up or Percoll method on succes of in vitro fertilization on early embryonic development. Theriogenology. 44: 859-869.
PINYOPUMMINTR, T., B. D. BAVISTER. 1991. In vitro-matured/in vitro-fertilized bovine oocytes can develop into morulae/blastocysts in chemically defined, protein-free culture media. Biol. Reprod. 45: 736-742.
RISOPATRON, J.M., M.R. DEL CAMPO, C.H. DEL CAMPO. 1991. Efecto de la temperatura de mantención de los ovarios sobre la maduración, fecundación y desarrollo de ovocitos de bovino. Arch. Med. Vet. 2: 143-149.
SAEKI, K., M. HOSHI, M.L. LEIBFRIED-RUTLEDGE, N.L. FIRST. 1990. In vitro fertilization and development of bovine oocytes matured with commercially available follicle stimulating hormone. Theriogenology. 34: 1035-1039.
SIRARD, M.A. P. BLONDIN. 1996. Oocyte maturation and IVF in cattle. Anim. Reprod. Sci. 42: 417-426.
SIRARD, M.A., J.J. PARRISH, C.B. WARE, M.L. LEIBFRIED-RUTLEDGE, N.L. FIRST. 1988. The culture of bovine oocytes to obtain developmentally competent embryos. Biol. Reprod. 39: 546-552.
TAKAHASHI, Y., N.L. FIRST. 1992. In vitro development of bovine one-cell embryos: influence of glucose, lactate, pyruvate, amino acids and vitamins. Theriogenology. 37: 963-978.
ZAR, J.H. 1996. Biostatistical analysis. Prentice Hall. Upper Saddle River, USA.