ARTICULOS ORIGINALES
F. OBLITAS1, M.V., M.Sc.; P. A.
CONTRERAS2, M.V., M. Phil.; H. BÖHMWALD2,
T. M.;
F. WITTWER2, M.V., M.V. Sc*1.
1 Facultad de Ciencias Veterinarias,
Universidad Nacional de Cajamarca, Casilla 16, Cajamarca, Perú.
2 Instituto de Ciencias Clínicas Veterinarias,
Universidad Austral de Chile, Casilla 567, Valdivia, Chile.
*Autor para correspondencia (fwittwer@uach.cl)
SUMMARY
An experiment was designed to study the effects of a selenium (Se) supplementation with sodium selenite on the blood activity of glutathione peroxidase (GSH-Px; EC 1.11.1.9) and live weight gain of selenium deficient grazing dairy heifers from two dairy farms from the south of Chile.
A total of 80 Friesian heifers (40 growing heifers, 287 kg b:w; and 40 mating heifers, 358 kg b:w) managed at grazing on permanent pastures belonging to two selenium deficient herds (40 animals from each herd), were used. Animals were allotted in similar groups, treated and control. The animals from the treated groups were administered with sodium selenite at 1.67% i.m., in a single dose of 5 mg of Se/100 kg body weight. Body weight change and GSH-Px blood activity were determined previous to supplementation and every three months.
The initial blood activity of GSH-Px was 34 U/g Hb in one herd and 116 U/g Hb in the other (Ref. value = > 130 U/g Hb). A significant increase in the GSH-Px activity up to 3 months after supplementation with selenium (P<0.05) was observed and the highest values were found at the 2nd month of the experiment. The percentage of increase of GSH-Px at the second month in the treated animals, in comparison with both the initial values and the values of the control animals, was of 300% in one herd and 179% in the other herd.
The live weight gain up the third month was slightly greater in the treated group than in the control (P<0.05) with a mean of 234 and 220 g/d in the growing and mating treated heifers, respectively in comparison with 169 and 148 g/d in the control groups.
It was concluded that, under the conditions of this study, selenium supplementation increases the blood activity of the enzyme GSH-Px for a period of at least three months and there is also evidence suggesting an increase in weight gain in selenium deficient grazing dairy heifers.
Palabras claves: selenio, suplementación, vaquillas, Glutatión-peroxidasa (GSH-Px).
Key words: trace element, selenium, cattle, Glutathione peroxidase (GSH-Px).
INTRODUCCION
El selenio (Se) es uno de los minerales esenciales para el mantenimiento y desarrollo de las funciones del organismo animal (McDowell, 1992), debiendo estar presente en la dieta de los animales domésticos en concentraciones que varían entre 0,1 y 0,3 ppm (N.R.C., 1983). Forma parte de la enzima glutatión peroxidasa (GSH-Px; EC 1.11.1.9), encargada de catalizar la reducción de los peróxidos para proteger a las células del daño oxidativo (Sandholm, 1980). La presencia de Se en la estructura de la enzima permite que exista una alta relación entre la concentración sanguínea o tisular de Se y la actividad de GSH-Px (Thompson y col., 1980); es así como en bovinos a pastoreo se ha establecido una correlación de 0,97 entre su actividad en los eritrocitos y la concentración sanguínea de Se (Ceballos y col., 1999).
La deficiencia metabólica de Se provoca una disminución en la actividad de GSH-Px, que se asocia a mayor susceptibilidad al estrés oxidativo y consecuentemente a diversos síndromes asociados a su déficit nutricional, como la enfermedad del músculo blanco, debilidad neonatal, miopatía cardíaca, retención de placenta, abortos, degeneración testicular, inmunosupresión y mastitis (Ceballos y Wittwer, 1996).
El Se cumple diversos roles en los animales, más allá de su actividad antioxidante citosólica que se señaló inicialmente, es así como actualmente se han descrito 10 selenoproteínas, además de GSH-Px, en tejidos de animales, cuya función no está aún claramente demostrada (Arthur y col., 1990). Entre éstas se ha descrito una deiodinasa que interviene en la conversión de T4 a la forma activa de T3, por lo cual frente a una deficiencia de Se se observa un incremento de TSH y T4 con una disminución de T3 plasmático (Arthur y col., 1993); antecedente que podría señalar un menor crecimiento en animales selenodeficientes.
Con el objeto de asegurar un aporte adecuado o controlar problemas de deficiencia de Se se utiliza la suplementación con sales inorgánicas o compuestos orgánicos de Se. Dentro de ellos, el selenito de sodio constituye el producto más utilizado, ya sea en conjunto con fertilizantes, esparcido sobre la pradera, por vía oral junto a una mezcla mineral, como bolos intraruminales o también por vía parenteral (McDowell, 1992; Rogers y Gately, 1992).
En Chile existen antecedentes que indican la presencia de forrajes con concentraciones de Se inferiores a los requerimientos para bovinos a pastoreo (Wittwer y col., 1997), así como también con actividad deficitaria de GSH-Px en la X Región (Ceballos y col., 1998). Por ello, este trabajo tuvo por objeto estudiar el efecto de una suplementación con selenito de sodio, sobre el balance metabólico de Se y el desarrollo en vaquillas a pastoreo, medidos por los cambios de la actividad de la glutatión peroxidasa (GSH-Px) y del peso corporal, respectivamente.
MATERIAL Y METODOS
Ubicación y selección de los predios. En Valdivia, sur de Chile (39° LS y 73° LO), fueron seleccionados al final de otoño, dos predios lecheros en consideración a su masa ganadera, tipo de alimentación, uso de praderas con antecedentes de concentraciones de Se menores a los límites requeridos (< 0,1 ppm) y la presencia de animales con baja actividad enzimática de GSH-Px (< 130 U/g Hb).
En ambos predios predominaban las praderas naturales mejoradas, de calidad regular y con una baja producción de materia seca, correspondiente al período invernal. En ellas se encontraban especies forrajeras como ballicas (Lolium sp.) y tréboles (Trifolium sp.), en menor proporción pasto ovillo (Dactylis glomerata), pasto miel (Holcus lanatus), pasto oloroso (Anthoxanthum odoratum), pasto cebolla (Arrhenatherum elatius) y chépica (Agrostis capillaris). Las fertilizaciones eran realizadas a fines de verano o en primavera sobre la base de nitrógeno, fósforo y potasio (NPK).
Animales experimentales. Para la experiencia se utilizaron 2 rebaños de 40 animales en cada uno (Rebaño 1 y Rebaños 2), con un total de 80 vaquillas de la raza Frisón Negro. Cada rebaño estaba constituido por 20 vaquillas en crecimiento, de 12 - 14 meses de edad con un peso promedio de 287 ± 29 kg y 20 vaquillas en encaste, de 18 - 20 meses de edad, con un peso promedio de 358 ± 36 kg. Cada grupo de 20 animales se dividió en dos bloques al azar de 10 animales, en tratamiento y control, respectivamente.
Los animales fueron identificados individual-mente con autocrotales plásticos y mantenidos conjuntamente con el resto del rebaño en condiciones de pastoreo directo de la pradera. Además, durante el período experimental se adicionó heno durante algunos días críticos, el cual había sido obtenido de las mismas praderas en el verano.
Suplementación con selenio. Un grupo fue tratado mediante una suplementación con selenito de sodio (Na2SeO3.5H2O) en solución acuosa al 1,67 %, por vía intramuscular, en dosis de 5 mg de Se/100 kg de peso vivo. El otro grupo no fue tratado y constituyó el grupo control. En ambos grupos se consideró a este momento como el tiempo experimental cero.
Obtención y manejo de las muestras. De cada animal se obtuvieron muestras de 10 ml de sangre, al tiempo 0 y posteriormente cada 30 días, en 3 oportunidades. Las muestras fueron obtenidas por venopunción coccígea, empleando tubos al vacío con heparina y transportadas dentro de 12 horas a temperatura de refrigeración al Laboratorio de Patología Clínica Veterinaria de la Universidad Austral de Chile.
Análisis de laboratorio. En las muestras de sangre se determinó la concentración de hemoglobina mediante el método de la cianometahemoglobina (Jain, 1986) y se preparó 1 ml de hemolizado, conservándolo a -25°C hasta su análisis.
La actividad sanguínea de glutatión peroxidasa (GSH-Px; EC 1.11.1.9) se analizó en el hemolizado mediante un kit comercial* según la metodología desarrollada por Paglia y Valentine (1967) y ejecutada según lo descrito por Ceballos y col. (1999). La exactitud de la prueba se controló mediante un hemolizado con actividad conocida y la precisión mediante el coeficiente de variación que fue de 3,2%.
Registro de pesos corporales. Los pesos vivos de cada animal, sin destare, se registraron mensualmente desde el tiempo 0 y en 4 oportunidades empleando una balanza ALLFLEX,, (F 600, Electronic Weighing System). La ganancia o pérdida de peso se determinó en gramos por día (g/día), mediante la diferencia de pesos entre dos pesajes dividida por el número de días transcurridos.
Análisis de los resultados. Los resultados se describen para cada grupo (tratado y control) y período (0, 0 a 30, 0 a 60 y 0 a 90 días) mediante el promedio (x) y error estándar (EE). La significancia (P<0,05) de las diferencias entre períodos y tratamientos, para las variables GSH-Px y ganancia de peso, se estableció mediante el ANDEVA de bloques al azar repetidos en el espacio y tiempo. Además, se determinó los factores que influyen en las variables mencionadas mediante el uso del método de regresión polinomial. La variación porcentual real de la actividad de GSH-Px en los grupos de animales tratados, ajustada según la variación del grupo control, se calculó para los períodos experimentales de 30, 60 y 90 días basándose en:
Variación porcentual real
| = (Xp(30-60 ó 90)T-XOT*100) - (Xp(30, 60 ó 90)C-XOC* 100) | |
|
---------XOT |
---------XOC |
Donde:
Xp (30,60 ó 90)T = Valor promedio a los 30, 60 ó 90 días en el grupo tratado.
XOT = Valor promedio al tiempo 0 en el grupo tratado.
Xp (30, 60 ó 90)C = Valor promedio a los 30, 60 ó 90 días en el grupo control.
XOC = Valor promedio al tiempo 0 en el grupo control.
Evaluación de pesos corporales. Los promedios iniciales de los pesos corporales en los animales de los grupos tratados y control fueron similares (P>0,05), tanto en las vaquillas en crecimiento (286±9 y 287±11,4 kg), como en las en encaste (360±9,4 y 357±11,2 kg respectivamente). Con posterioridad a ello, se observó un incremento leve, pero sostenido, en todos los grupos hasta los 60 días de la experiencia y luego una pérdida leve de peso entre los 60 y 90 días, excepto en las vaquillas en crecimiento tratadas (P>0,05) (cuadro 2). Así, para los 90 días del período experimental se obtuvo un promedio de ganancia de peso de 270 y 216 g/d en las vaquillas tratadas y de 169 y 143 g/d en las vaquillas controles (P<0,05).
En las vaquillas en crecimiento tratadas se obtuvo una diferencia, respecto de la controles, de 59 y 73 g/d para los rebaños 1 y 2 respectivamente, mientras que en las vaquillas en encaste la diferencia a favor de los animales tratados fue de 82 y 73 g/d (gráfico 2).
El incremento de peso de los animales de ambos grupos tuvo una amplia variabilidad (192%), deduciéndose que hubo otros factores que influyeron en los resultados obtenidos; este incremento de peso fue mayor en el grupo de los animales tratados, tanto en crecimiento como en encaste, con respecto al grupo control (P<0,05), aunque existió una fuerte influencia del tiempo con relación al incremento de peso en todos los parámetros, siendo éste inversamente proporcional y cuya ecuación de regresión dio como resultado: R2=0,97.
RESULTADOS
Actividad enzimática sanguínea de glutatión peroxidasa. Los valores iniciales de GSH-Px (promedio ± EE) para las vaquillas del rebaño 1 fueron de 34 ± 2,8 U/g Hb, y para el segundo rebaño de 116 ± 5,3 U/g Hb, con valores similares en los animales de los grupos tratados y controles (P>0,05). La suplementación intramuscular con selenito de sodio en los grupos tratados de los dos rebaños provocó un incremento significativo (P<0,01) de la actividad de la enzima sanguínea de GSH-Px con relación a los grupos controles (cuadro 1). En el grupo tratado existe un incremento de la actividad enzimática sanguínea de GSH-Px hasta los 60 días para luego disminuir hacia los 90 días; aunque los valores de los períodos entre 30 y 90 días son mayores (P<0,05) con relación a los valores de GSH-Px obtenidos en la etapa pre-experimental.
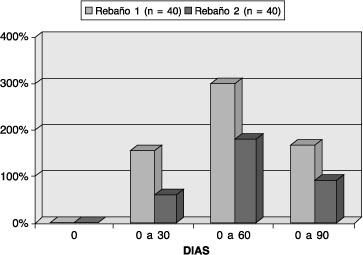
La actividad de GSH-Px aumentó significati-vamente en los grupos tratados (P<0,01). Se apreció un incremento a los 30 días, alcanzando su mayor actividad a los 60 días, en que se presentó un incremento real sobre el grupo control de 300% en el rebaño 1 (R2 = 0,73) y de 179% en el rebaño 2 (R2 = 0,85), para luego disminuir progresivamente hacia los 90 días (gráfico 1). Los valores de confiabilidad en ambos grupos controles fueron de R2=0,43 para el rebaño 1 y R2=0,42 para el rebaño 2.

|
Gráfico 1. Variación porcentual real del promedio de la actividad enzimática sanguínea de GSH-Px a los 30, 60 y 90 días respecto al día 0 en vaquillas Frisón Negro de dos rebaños tratadas con selenito de sodio el día 0 (5 mg / 100 kg. p.v.). Gluthatione peroxidase activity change in two herds of grazing Friesian heifers treated with sodium selenite (Se = 5 mg/100 kg b.w.), at 30, 60 and 90 days post-treatment, Values are expresed as percentage of variation in relation to control animals. |
| Rebaño 1 |
Rebaño 2 |
|||
| Período (días) |
Tratadas (n=20) |
Controles (n=20) |
Tratadas (n=20) |
Controles (n=20) |
| 0 30 60 90 |
35± 4a 114 ± 5b 173 ± 9c 106 ± 5b |
34 ± 4 58 ± 3 66 ± 4b 46 ± 3a |
109 ± 7a 151 ± 7b 340 ± 11c 166 ± 9b |
122 ± 8 96 ± 7a 162 ± 12b 73 ± 7a |
| Promedio (30 - 90 días) |
131 ± 5* | 56 ± 2 | 219 ± 12* | 107 ± 7 |
|
Letras diferentes = P< 0,05 entre períodos
para cada rebaño. * = P<0,05 con grupo control. |
DISCUSION
Actividad enzimática sanguínea de glutatión peroxidasa. La actividad enzimática de GSH-Px inicial de las vaquillas de ambos rebaños fue inferior a los valores considerados adecuados (<130 U/g Hb), clasificándose el rebaño 1 con 34 U/g Hb, como deficiente, y el rebaño 2 con 116 U/g Hb como marginal (Ceballos y Wittwer, 1996). Estos valores indican que había desbalances metabólicos de Se, sin la presentación de signos clínicos relacionados con la deficiencia de este elemento.
La deficiencia de Se sería causada por un bajo contenido del mineral en la pradera, puesto que las vaquillas sólo consumían pasto. Al respecto se ha señalado que un 60% de las praderas de la zona presentan concentraciones de este elemento <0,1 ppm (Wittwer y col., 1997), valor considerado como mínimo en la dieta para bovinos (NRC, 1983). La concentración de Se en la pradera está influenciada por muchos factores como: tipo y pH del suelo, pluviosidad, época del año, composición botánica, entre otros (Sandholm, 1980; Langlands y col., 1981; Ekermans y Schneider, 1982); como consecuencia, el contenido y disponibilidad de Se en el suelo determinará su concentración en el forraje y éste a su vez regula la concentración sanguínea y tisular de Se en el animal a pastoreo (Langlands y col., 1981; Gissel-Nielsen y col., 1984).
La suplementación mediante inyección intramuscular de selenito de sodio, produjo un aumento de la actividad sanguínea de GSH-Px en los animales tratados de ambos rebaños, alcanzándose la mayor actividad a los 60 días después del tratamiento (cuadro 1). El aumento en la actividad sanguínea de GSH-Px ocurre en un lapso de 1 a 4 semanas (Levander, 1986; McDowell, 1992), ya que el aumento de la concentración orgánica de Se no conduce a la síntesis inmediata de la enzima, sino que está asociada a su incorporación a los eritrocitos en el proceso de eritropoyesis (Knight y Sunde, 1988).
El aumento en la actividad enzimática a los 30 días después de la aplicación intramuscular de selenito de sodio en las vaquillas tratadas, nos indica que la dosis empleada fue adecuada para superar la deficiencia de Se por un período de al menos dos meses, posterior al período de latencia requerido para la incorporación del Se como GSH-Px en los eritrocitos. No se observó similar incremento en las vaquillas controles, a pesar de mantenerse junto a las del grupo tratado con idéntica alimentación y manejo, corroborando que el aumento significativo de la actividad de GSH-Px obtenida en los grupos tratados estuvo determinada por el tratamiento con selenito de sodio.
Evaluación de la ganancia de peso. Las variaciones de peso observadas durante los 90 días de experimentación en ambos grupos de animales fueron pequeñas e incluso con pérdida de peso en el período final (cuadro 2). Este comportamiento está asociado a las características del manejo y alimentación de los animales durante el período experimental, correspondiente a fines de otoño e invierno. En este período, las praderas de la zona presentan leves variaciones en su composición nutricional, pero su crecimiento es mínimo y el contenido de materia seca es bajo, alrededor de 15% a 21%, lo que lleva a una baja disponibilidad de forraje (Anrique y col., 1995; Teuber y Dumont, 1996)
Las ganancias de peso en los 90 días de ensayo fueron mayores en los animales tratados respecto de los controles, tanto en las vaquillas en crecimiento como en encaste (cuadro 2) y en los 2 rebaños, vale decir, con valores deficientes (rebaño 1) y marginales (rebaño 2) de GSH-Px (gráfico 2). La alta variabilidad individual observada, asociada a factores externos propios del manejo y alimentación en ensayos o experiencias a nivel de campo, limitan la sensibilidad para medir los efectos de una suplementación en este tipo.
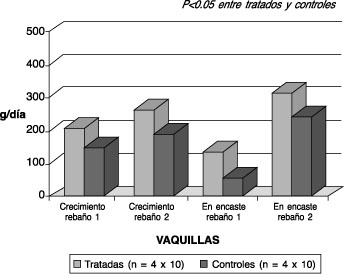
| Gráfico 2. Promedio de la diferencia de pesos (g/día)
a los 90 días en vaquillas Frisón Negro en crianza y en
encaste de dos rebaños, tratadas con selenito de sodio (Se = 5
mg/100 kg p.v.) y controles.
Mean body weight change (g/d) in control and growing and mating grazing Friesian heifers at 90 days following treatment with sodium selenite (Se = 5 mg/100 kg b.w.). |
| Vaquillas | En crecimiento |
En encaste |
||
|
Período |
Tratadas (n=20) |
Controles (n=20) |
Tratadas (n=20) |
Controles (n=20) |
| 0 30 30 60 60 90 |
560 ± 61 130 ± 109 111 ± 83 |
431 ± 41 180 ± 113 -104 ± 86 |
381 ± 72 425 ± 73 -145 ± 60 |
258 ± 50 353 ± 85 -153 ± 65 |
| Promedio | 270 ± 57* | 169 ± 55 | 216 ± 51* | 143 ± 49 |
| * = P< 0,05 con grupo control. |
Wichtel y col. (1994), sostienen que aún no está completamente establecida la razón por la que la deficiencia de Se en los animales a pastoreo provoca un retardo en el crecimiento de los animales, aunque no se observen signos de Enfermedad del Músculo Blanco. Por otra parte, la tasa de crecimiento de estos animales aumenta al suplementar con Se, lo cual sugiere la existencia de un mecanismo en el cual no estaría involucrado un metabolismo anormal de peróxidos y por lo tanto es independiente de la enzima GSH-Px. Wichtel y col. (1996), sugieren que los efectos adversos en los animales Se-deficientes a pastoreo pueden ser producidos por una alteración del metabolismo de las hormonas tiroídeas y no por una alteración en las concentraciones periféricas de la hormona del crecimiento. Al respecto, se ha descrito que la iodotironina-5-deiodinasa tipo I, es una enzima Se-dependiente responsable de la deiodinización de la tiroxina (T4), convirtiéndola en su forma más activa Triyodotironina (T3) (Berry y col., 1991).
Los resultados del presente trabajo permiten concluir que la suplementación de Se como selenito de sodio en solución acuosa al 1,67% en dosis de 5 mg de Se/100 kg de peso vivo, vía intramuscular, produce un incremento de la actividad de glutatión peroxidasa desde los 30 a 90 días de su aplicación, permitiendo obtener una mayor ganancia de peso (g/día) en vaquillas selenio deficiente a pastoreo.
RESUMEN
Con el propósito de evaluar los efectos de una suplementación con selenio (Se) en el comportamiento metabólico y productivo de bovinos mantenidos a pastoreo con antecedentes de deficiencia de este mineral, se realizó una experiencia evaluando la respuesta a una suplementación con selenito de sodio sobre la actividad de glutatión peroxidasa eritrocítica (GSH-Px; EC 1.11.1.9) y ganancia de peso.
En dos rebaños del sur de Chile, con historia de deficiencia de Se en el pasto y de GSH-Px en los animales, se seleccionaron 80 vaquillas Frisón Negro, 40 en crecimiento de 287 kg de peso y 40 en encaste de 358 kg de peso. En los animales de cada rebaño (n=40) se constituyeron dos grupos similares, tratados (n=20) y control (n=20), manteniéndose juntos a pastoreo en praderas naturales. Los animales tratados recibieron una inyección de selenito de sodio al 1,67% (Se = 5 mg/100 kg de peso i.m.). Previo a la suplementación y luego cada mes durante 3 meses, se determinó la actividad sanguínea de GSH-Px y el peso corporal.
La actividad sanguínea inicial de GSH-Px de los dos rebaños fue de 34 y 116 U/g Hb (valor de referencia > 130 U/g Hb). La suplementación provocó un aumento (P<0,05) de la actividad de la enzima hasta los 3 meses, con los valores más altos a los 2 meses, con un incremento real sobre los controles (P<0,05) de 300% y 179% en los rebaños 1 y 2 respectivamente.
Los pesos a los 90 días fueron mayores en los grupos tratados que en los controles (P<0,05), siendo los promedios de 234 y 220 g/día para los animales en crecimiento y en encaste respectivamente y de 169 y 148 g/día para las vaquillas controles.
Se concluye que la suplementación en vaquillas selenio deficiente a pastoreo, bajo las condiciones del estudio, incrementa la actividad sanguínea de GSH-Px por un período de al menos tres meses y evidencia un efecto favorable sobre la ganancia de peso.
_____________________________
Aceptado: 11.04.2000.
* Proyecto FONDECYT - CHILE 199-0993 y DID UACH S98-18.
* Ransel, y Ransel Control® lotes N 099 RS y 129 RS. Randox Laboratories Lts. Crumlin, Irlanda del Norte.
BIBLIOGRAFIA
ARTHUR, J.R., F. NICOL, G.J. RECHETTE. 1990. Hepolic iodothyronine 5'-deiodinasa: The role of selenium. Biochem. J. 272273.
ARTHUR, J.R., 1993. The biochemical functions of selenium relationships to thyroid metabolism and antioxidant systems. Rowett Research Institute Annual Report. Backsburn, Aberdeen, UK.
ANRIQUE, G.R., X. VALDERRAMA, R. FUCHSLOCHER. 1995. Composición de alimentos para el ganado en la zona sur. Ed. Fundación Fondo de Investigación Agropecuaria, FIA, Ministerio de Agricultura. Universidad Austral de Chile. Uniprint S. A. Imprenta Universitaria. Valdivia, Chile.
BERRY. M.J., L. BANU, P.R. LARSEN. 1991. Type I iodothyronine deiodinasa is a selenocysteine-containing enzyme. Nature (Lond.) 348: 349.
CEBALLOS, A., F. WITTWER. 1996. Metabolismo del selenio en rumiantes. Arch. Med. Vet. 28. 5-18.
CEBALLOS, A., F. WITTWER, P.A. CONTRERAS, H. BÖHMWALD. 1998. Actividad sanguínea de glutatión peroxidasa en rebaños lecheros a pastoreo: variación según edad y época del año. Arch. Med. Vet. 30: 13-22.
CEBALLOS, A., F.G. WITTWER, P.A. CONTRERAS, E. QUIROZ, H. BÖHMWALD. 1999. Actividad de glutatión peroxidasa en bovinos a pastoreo correlacionada con la concentración sanguínea y plasmática de selenio. Pesq. Agrop. 34. 2331-2338.
DOMÈNECH, J. M. 1980. Bioestadística. 3 ed. Editorial Herder, Barcelona, España.
EKERMANS, L.G., J.V. SCHNEIDER. 1982. Selenium in livestock production: a review. J. South Afr. Vet. Ass. 53: 223-228.
GISSEL-NIELSEN, G., U.C. GUPTA, M. LAMOND, T. WESTERMACK. 1984. Selenium in soils and plants, and its importance in livestock and human nutrition. Adv. Agr. 37: 397-460.
JAIN, N.C. 1986. Schalm's Veterinary Hematology. 4th. ed., Lea & Febiger, Philadelphia.
KNIGHT, S.A., R.A. SUNDE. 1988. Effect of selenium repletion on glutathione peroxidase protein level in rat liver. J. Nutr. 118: 853-858.
LANGLANDS, J.P., J.E. BOWLES, A.J. SMITH, G.E. DONALD. 1981. Selenium concentration in the blood of ruminants grazing in Northern New South Wales. I. Analysis of samples collected in the National Brucellosis Erradication scheme. Austr. J. Agric. Res. 32: 511-521.
LEVANDER. O.A. 1986. Selenium. En: MERTZ, W. 1986. Trace elements in human and animal nutrition. Vol. 2. 5th. ed., Academic Press, Inc. Orlando, USA.
McDOWELL, L.R. 1992. Minerals in Animal and Human Nutrition. Academic Press, Inc., San Diego, California, U.S.A.
McDOWELL, L.R., J.H. CONRAD, F.G. HEMBRY. 1993. Selenio. Minerales para Rumiantes en Pastoreo en Regiones Tropicales. 2 ed., Departamento de Zootecnia, Universidad de Florida, Gainesville. (Boletín): 37-40.
NATIONAL RESEARCH COUNCIL (N.R.C.), SUBCOMITTEE ON SELENIUM. 1983. Selenium in Nutrition. Revised Edition. National Academic Press, Washington, D.C.
NICHOLSON, J.W.G., R.E. McQUEEN, R.S. BUSH. 1991. Response of growing cattle to supplementation with organically bound or inorganic sources of selenium or yeast cultures. Can. J. Anim. Sci. 71: 803-811.
PAGLIA, D.E., W.N. VALENTINE. 1967. Studies on the quantitative and qualitative characterization of erythrocyte gluthatione peroxidase. J. Lab. Clin. Med. 70: 158-169.
PEHRSON B., S. JOHNSSON. 1985. Selenium and glutathione peroxidase in blood and tissues and growth and feed efficiency in young bulls at different dietary selenium levels. Zbl. Vet. Med. A. 332: 492-501.
ROGERS, P.A. M., T.F. GATELY. 1992. Control of mineral imbalances in cattle and sheep. Edit. Teagasac, Dublin, Ireland.
SANDHOLM, M. 1980. Biological and clinical aspects of selenium. En: IV International Conference on Production Disease in Farm Animals. München, Germany, pp. 247-253.
TEUBER, K.T., J.C. DUMONT. 1996. Atributos de la pradera para la alimentación del rebaño lechero. En: III Seminario Aspectos Técnicos y Perspectivas de la Producción de Leche. Eds. F. Lanuza y G. Bortolameolli. Serie Remehue N° 64. Osorno, Chile. pp.3-21.
THOMPSON, K.G., A.J. FRASER, B.M. HARROP, J. A. KIRK. 1980. Glutatione peroxidase activity in bovine serum and erythrocites in relation to selenium concentrations of blood, serum and liver. Res. Vet. Sci. 28: 3-6.
WICHTEL, J.J., A.L. CRAIGIE, H. VARELA-ALVAREZ, N.B. WILLIAMSON. 1994. The effect of intra-ruminal selenium pellets on growth rate, lactation and reproductive efficiency in dairy cattle. N. Z. Vet. J. 42: 205-210.
WICHTEL, J.J., A.L. CRAIGIE, D.A. FREEAN, H. VARELA-ALVAREZ, N.B. WILLIAMSON. 1996. Effect of selenium and iodine supplementation on growth rate and somatotropic function in dairy calves at pasture. J. Dairy Sci. 79: 1865-1872.
WITTWER, F.G., A. CEBALLOS, P.A. CONTRERAS, H. BÖHMWALD. 1997. Actividad sanguínea de glutatión peroxidasa en bovinos a pastoreo y correlación con la concentración sanguínea y plasmática de selenio. XXII Reunión Anual. Sociedad Chilena de Producción Animal, Valdivia, Chile, pp. 183-184.