ARTÍCULOS ORIGINALES
Comparación entre dos técnicas de diagnóstico para diarrea viral bovina (dvb) en 50 predios de la X región, Chile. Seroneutralización y enzimoinmunoensayo indirecto (ELISA-I)*
Comparison of two diagnostic techniques to bovine viral diarrhea disease (BVD) in 50 dairy herds from the Xth Region, Chile. Seroneutralization test and indirect immunosorbent assay (I-ELISA)
G. REINHARDT 1, M.V., Dr. med.vet ; L. CARRASCO 1, M.V.; N. TADICH 2, M.V., Ph.D.; S. RIEDEMANN 1, T.M., M.V.
1 Instituto de Microbiología, Facultad de Ciencias. 2 Instituto de Ciencias Clínicas Veterinarias, Facultad de Ciencias Veterinarias, Universidad Austral de Chile, Casilla 567, Valdivia, Chile. e-mail: greinhar@uach.cl
SUMMARY
Bovine viral diarrhea/Mucosal
disease (BVD/MD) is a highly spread virosis worldwide and has a great impact
in bovine reproduction and production. In Chile, the disease has been reported
with over 60% of prevalence and it demands adecuate diagnostic methods.
Curently the official serologic diagnostic test in Chile is the serum neutralization
test (SNT), this method detects the presence of antibodies against the BVD virus
and it is considered to have good specificity and sensitivity, althought, it
presents some disadvantages in its interpretation and in its execution.
The aim of this investigation was to compare de SNT as gold standard, with a
commercial immunosorbent assay (ELISA), in terms of specificity and sensitivity
in the detection of antibodies against BVD antigens. A set of 500 bovine sera
drawn from 50 milk herds from the Xth Region of Chile were analized.
The results showed that the SNT detected 278 serum samples as positives and
the ELISA detected 347 serum samples as positives, these represents for ELISA
test a relative sensitivity and specificity of 91% and 57%, respectively. Statistically
significant differences of the serodiagnosis obtained in both tests were established
through the McNemar test (<0.05), and a median concordance between them through
the Kappa test. When the SNT titers were related with the optical densities
(OD) of ELISA, a positive association was detected between this values.
It was concluded that ELISA provides good results in comparison with SNT, having
the former a higher number of detections because its dignostic higher sensitivity.
Therefore, ELISA is an appropiate diagnostic method for large populations of
cattle.
Palabras claves: Diarrea Viral Bovina, comparación métodos diagnóstico.
Key words: Bovine viral diarrhea, comparison of diagnostic methods.
INTRODUCCIÓN
El complejo Diarrea Viral Bovina/Enfermedad de las Mucosas (DVB/EM), es una enfermedad infecciosa de alta prevalencia en bovinos de cualquier edad y en diversos lugares del mundo, que provoca un importante impacto económico debido principalmente a pérdidas de tipo reproductivo que se manifiestan por abortos, defectos congénitos, mortalidad neonatal y problemas de fertilidad, entre otros (Blood y Radostitis, 1992).
DVB/EM de diagnosticó en nuestro país en 1986, por medio de hallazgos anatomopatológicos en terneros de la X Región (Fidler y col., 1986), lo que fue confirmado por técnicas de Inmunofluorescencia directa (IFD), seroneutralización (SN) y aislamiento viral en cultivo celular (Reinhardt y col., 1986). Posteriormente el agente se ha aislado repetidamente, como por ejemplo en fetos abortados en la Región Metropolitana (Celedón y col., 1997).
Lo que más llama la atención en el comportamiento biológico del virus DVB es la existencia de dos biotipos, el citopático (cp) y el no citopático (ncp) (Coria y col., 1984). Su diferencia radica en la particularidad del primero de producir efecto citopático (ecp) en un cultivo celular susceptible, el que se traduce en vacuolización citoplasmática y muerte celular (Gillespie y col., 1960). El otro biotipo (ncp), no causa ningún efecto manifiesto en la monocapa celular que infecta y donde se multiplica adecuadamente (Baker, 1987). Cabe señalar que este biotipo es el más común en la naturaleza (Brownlie y col., 1987), y que el biotipo cp deriva de cambios genéticos del anterior (Corapi y col., 1988).
Una posterior clasificación del virus DVB, basada en diferencias encontradas en la secuencia genética de una región del genoma, conocida como región 5'UTR, determina la existencia de los genogrupos I y II, existiendo diferncias a nivel molecular y en cuanto a severidad de los signos clínicos que se producen (Ridpath y col., 1992). Se pudo determinar que el genogrupo II reune las cepas más virulentas (Ellis y col., 1998; Fulton y col., 2000). En Chile, Pizarro y col., (1999), demostraron la presencia de ambos serogrupos en el ganado bovino nacional.
Existen variadas técnicas de diagnóstico útiles en la detección de la enfermedad y ellas pueden ser divididas en dos grandes grupos, el método directo y el método indirecto. El primero se basa en la detección del virus o antígeno viral, en contraste, el segundo determina la respuesta inmune de tipo humoral del huésped frente a la acción del agente.
En general, la totalidad de los métodos de diagnóstico utilizados en el laboratorio para el estudio de DVB requieren, para un resultado satisfactorio, de una recolección apropiada de muestras, buen material de trabajo, transporte y procesamiento adecuados (Ministry of Agriculture, Fisheries and Food, England, 1978).
La ténica de seroneutralización (SN), consiste en una prueba punto final seroneutralizante, que permite identificar y cuantificar la capacidad de los anticuerpos séricos para inhibir o neutralizar el efecto citopático de una cepa dada. Los anticuerpos neutralizantes son responsables del efecto protector del suero y están dirigidos contra determinates antigénicos específicos de la superficie del virus (FAO, 1985). Según Duffel y Harkness (1985), esta prueba diagnóstica presenta la limitante de no detectar bajas tasas de anticuerpos como en el caso de animales virémicos inmunocompetentes.
El método inmunoenzimático (ELISA) para la detección de anticuerpos, se utiliza para la cuantificación de muy pequeñas cantidades de éstos, que habitualmente no son detectables por los métodos convencionales; además esta técnica presenta la carcterística de una alta especificidad y sensibilidad, así como rapidez, lo que posibilita el estudio de grandes poblaciones en corto tiempo, en forma rutinaria y sencilla (Dinter, 1989). Por otra parte, su cuantificación se basa en la reacción enzima-sustrato que produce un cambio de coloración que se evalúa mediante un espectrofotómetro lo que evita resultados subjetivos, además resultan ser pocos los errores que esdta técnica presenta en caso del uso de "kits" comerciales, puesto que las variables han sido estandarizadas de modo que los parámetros medidos no sean alterados (Dubovi, 1990).
Este estudio pretende comparar el diagnóstico serológico de la infección por el virus DVB utilizando un método de ELISA indirecto y la prueba de SN en muestras de suero sanguíneo obtenidas de ganado bovino de predios lecheros de la X Región de Chile con el propósito de evaluar la técnica de ELISA en relación con la SN, según sensibilidad y especificidad, comparando los resultados obtenidos y estudiando la correlación existente entre ambos métodos utilizados.
MATERIAL Y MÉTODOS
Este estudio utilizó un total de 50 predios lecheros, ubicados en las provincias de Llanquihue, Osorno y Valdivia de la X Región de Chile, los que fueron seleccionados por conveniencia, de acuerdo a tamaño del rebaño, ausencia de vacunación contra la enfermedad e interés del propietario en participar. Se recolectaron 500 muestras de sangre, a partir de 10 animales de cada predio, de edades que fluctuaron entre los 6 y 18 meses. Todas las muestras se obtuvieron por extracción de 5-10 ml de sangre desde la vena yugular mediante la utilización de tubos Venojet que fueron transportados al Instituto de Microbiología donde se obtuvo el suero por centrifugación de cada muestra a 700 x g por 15 min. Los sueros así obtenidos se almacenaron en tubos Eppendorf, rotulados con números correlativos y congelados a -30° C. Previo a su análisis se inactivaron por 30 min. a 56° C, con la finalidad de destruir los inhibidores inespecíficos que pudieren alterar los resultados de la SN.
La prueba de SN, dilución punto final seroneutralizante, se realizó diluyendo los sueros problema, el suero control positivo y el suero control negativo en logaritmo de base 2, en medio mínimo esencial en sales de Earle (MEM-E), en volúmenes de 50m l y se enfrentaron a 100 dosis infectantes cultivo de tejido 50% (DICT50) de la cepa viral München del virus DVB, también en volúmenes de 50 m l. Luego de una incubación por 60 min. a temperatura ambiente, se adicionó 100 m l de células embrionarias de pulmón bovino de segundo pasaje (1x106 cél/ml),en MEM-E más 10 % de suero fetal bovino irradiado (SFB). Finalmente las microplacas se llevaron a incubación en estufa de cultivo con cámara húmeda a 37° C y adicionada de un 5% de CO2 por 5 días, para luego proceder a su lectura mediante observación microscópica.
Para la interpretación de la prueba de SN se observó la presencia de cpe en los diferentes pocillos de cada microplaca. Se revisaron los sueros controles positivo y negativo, los pocillos de control de células y los de control de citotoxicidad de los sueros problema y luego se procedió a la lectura de los pocillos correspondientes a cada dilución sérica. Toda muestra que presentó a lo menos un pocillo sin cpe se consideró positiva y el título neutralizante de cada suero se calculó de acuerdo al método de Behrens y Kärber (Mayr y col, 1974).
El método de ELISA-I utilizado fue un "kit" comercial basado en la detección de IgG en los sueros analizados, denominado CHEKIT-BVD-SERO*, el que básicamente está compuesto de microplacas de 96 posillos sensibilizados con antígenos, de modo que los pacillos pares presentan un antígeno control (que corresponde a las células donde se cultiva el virus DVB), y los impares con antígeno viral DVB inactivado. Cada suero problema , un suero control negativo y otro positivo se diluyeron 1:10 y esa dilución se colocó en duplicado en pocillos pares e impares de la microplaca sensibilizada. Las microplacas se incubaron por 90 min. a temperatura ambiente y en cámara húmeda. Posteriormente se procedió a la eliminación del contenido de cada microplaca y se realizó un lavado en triplicado. A continuación se procedió a la colocación en cada pocillo de una dilución al 1:200 del conjugado (200 m l), incubándose nuevamente a temperatura ambiente por 60 min. y en cámara húmeda a fin de que se produjera su unión con los probables anticuerpos presentes en los pocillos. Transcurrido el tiempo de incubación se realizó nuevamente la eliminación del contenido de cada placa y su posterior lavado en triplicado. Con el fin de evidenciar la unión del conjugado al complejo antígeno-anticuerpo, se adicionó a cada pocillo, 200 m l de cromógeno que actúa como sustrato de la enzima presente en el conjugado y que en el caso de reacciones positivas genera una coloración que puede observarse a simple vista. Luego de 10 a 15 min. de incubación se agregó 50 m l de una solución de detención de la reacción para proceder a la lectura, la que se realizó con un fotómetro lector (MULTISKAN MK II), a una longitud de onda de 405 nm, lo que permite determinar la densidad óptica (DO) de la reacción colorimétrica. Para la interpretación de los resultados se siguieron las intrucciones del laboratorio productor del "kit". Para ello, de cada muestra hecha en duplicado se obtuvo el valor promedio de DO, como también de los controles positivo y negativo. Los valores de las DO de cada muestra y el valor de la DO del suero positivo fueron corregidos, sustrayéndoles el valor de DO del control negativo. Para la interpretación del rtesultado de cad muestra se utilizó la siguiente fórmula:
% muestra = DO muestra _- DO C negativo x
100
DO C positivo - DO C negativo
Valores menores de 30% se consideran negativos; valores entre 30 y 40% se consideran dudosos y valores mayores de 40% se consideran positivos. Todas las muestras que se consideran dudosas se vuelven a analizar con el fin de clasificarlas como positivas o negativas en forma definitiva.
Para el análisis de los resultados se utilizaron parámetros estadísticos de sensibilidad (Se) y especificidad (Es), mediante una tabla de 2x2, donde el sistema de referncia fue la prueba de SN.
Cuadro 1. Clasificación
cruzada de las pruebas de SN y ELISA
Specificity and sensitivity of ELISA compared
with SNT.
|
Seroneutralización |
|||
|
ELISA |
Positivo |
Negativo |
Total |
| Positivo |
A |
B |
A+B |
| Negativo |
C |
D |
C+D |
| Total |
A+C |
B+D |
(N) |
Descripción :
A: Positivos verdaderos
B: Falsos positivos
C: Falsos negativos
D: Negativos verdaderos
(N): Número total de muestras comparadas
Además, se utilizaron gráficos tipo Box-Plot, que muestran medidas de resúmen para ambas técnicas, realizados mediante el programa computacional Statistica 4.0; se usó la prueba de McNemar para muestras relacionadas y detección de muestras positivas (Daniel, 1978), con el fin de comprobar la hipótesis nula planteada, esto es igual proporción de seroreaccionantes positivos a las dos técnicas. Se utilizó el método estadístico de Kappa (K), con un nivel de confianza de 95%, para determinar el grado de concordancia entre ambas pruebas, descartando el azar (Whimster, 1997), y se ocupó el coeficiente de Spearman para determinar la correlación existente entre títulos de anticuerpos medidos por la SN y los porcentales de DO obtenidos por ELISA (Nie y col., 1975).
RESULTADOS
Para el análisis de los resultados obtenidos con las dos pruebas diagnósticas utilizadas, se establecieron dos categorías de muestras, positivas o negativas respecto a la presencia o ausencia de anticuerpos frente al antígeno del virus DVB. Mediante la técnica de SN se titularon los sueros positivos y por la técnica de ELISA, tras la repetición de las muestras que resultaron dudosas, se categorizó la totalidad de ellas.
El resultado de las pruebas de informa en los cuadros 2 y 3 para cada prueba respectivamente, en los que se agruparon los diversos planteles analizados según el número de sueros positivos y el porcentaje respecto de las 10 muestras por plantel.
Cuadro 2. Distribución
en número y porcentaje de los sueros positivos a SN para DVB en los 50
planteles lecheros de la X Región , Chile.
Distribution of positive dera for BVD tested by SNT in 50 dairy herds from the
X Region, Chile.
|
SERONEUTRALIZACIÓN |
||
| N° Predios |
N° Muestras |
Porcentajes |
| 3 |
0 |
0 |
| 3 |
3 |
10 |
| 4 |
8 |
20 |
| 2 |
6 |
30 |
| 6 |
24 |
40 |
| 6 |
30 |
50 |
| 6 |
36 |
60 |
| 5 |
35 |
70 |
| 4 |
32 |
80 |
| 6 |
54 |
90 |
| 5 |
50 |
100 |
| 50 |
278 |
TOTAL |
El cuadro N° 2 indica que, de los 50 planteles analizados, el 94% (48) de ellos presentaron al menos un suero reaccionante al virus DVB y que la prueba de SN detectó 278 sueros positivos del total de 500, lo que representa un 55,6
Cuadro 3. Distribución
y porcentaje de sueros reaccionantes a ELISA frente a DVB en 50 planteles analizados
en la X Región, Chile.
Distribution of positive sera for BVD tested by
ELISA in 50 dairy herds from the X Region, Chile.
|
ELISA |
||
| N° Predios |
N° Muestras |
Porcentaje |
| 2 |
0 |
0 |
| 1 |
1 |
10 |
| 1 |
2 |
20 |
| 5 |
15 |
30 |
| 2 |
8 |
40 |
| 4 |
20 |
50 |
| 7 |
42 |
60 |
| 5 |
35 |
70 |
| 2 |
16 |
80 |
| 2 |
18 |
90 |
| 19 |
190 |
100 |
| 50 |
347 |
TOTAL |
De los resultados presentados en el cuadro N° 3 se desprende que el 96% de los los 50 predios analizados tenían a lo menos un animal reaccionante y la prueba de ELISA detectó 347 muestras como positivas, lo que corresponde al 69,4% de las 500 muestras estudiadas.
Cuadro 4. Resultados
comparados del total de sueros analizados tanto por ELISA como por SN frente
al virus DVB.
Comparison of ELISA and SNT results for BVDV.
|
Seroneutralización |
|||
|
ELISA |
Positivo |
Negativo |
Total |
| Positivo |
252 (A) |
95 (B) |
347 (A+B) |
| Negativo |
26 (C) |
127 (D) |
153 (C+D) |
|
Total |
278 (A+C) |
222 (B+D) |
500 (N) |
Cálculo de Sensibilidad
y Especificidad relativas:
Sensibilidad relativa: (A/ (A+C) x 100 = 91%
Especificidad relativa: (D/ (B+D) x 100 = 57%
Los datos entregados en el cuadro N° 4 muestran que la sensibilidad relativa de ELISA detecta el 91% del total de positivos diagnosticados por SN y la especificidad relativa de ELISA detecta el 57% del total de negativos dignosticados por SN.
De los resultados obtenidos se desprende que existen diferencias en la detección de muestras reaccionantes entre ambas pruebas diagnósticas, dado por aquéllas seropositivas para una técnica pero negativas para la otra.
La prueba de McNemar para muestras relacionadas con c 2 = 39,3 determinó una p<0,05, lo que rechazó la hipótesis nula planteada, lo que indica en la detección de anticuerpos por ELISA y por SN hubo diferencias significativas.
De acuerdo al método estadístico de Kappa, se determinó un valor moderado de concordancia (K = 0,49), entre las técnicas utilizadas, lo que resultó ser estadísticamente significativo (p<0,05).
Cuadro 5.
Promedios y desviación estándar (DS) de los resultados de la totalidad
de las muestras séricas analizadas tanto por ELISA como por SN.
Means and standard deviatin (SD) resuts of positive and negative serum samples
tested by ELISA and SNT.
| Seroneutralización |
ELISA |
|
| Promedio |
33* |
77** |
| Desviación Estandar |
69,1 |
55,1 |
* Expresado en título de anticuerpos
** Expresado en porcentaje de DO.
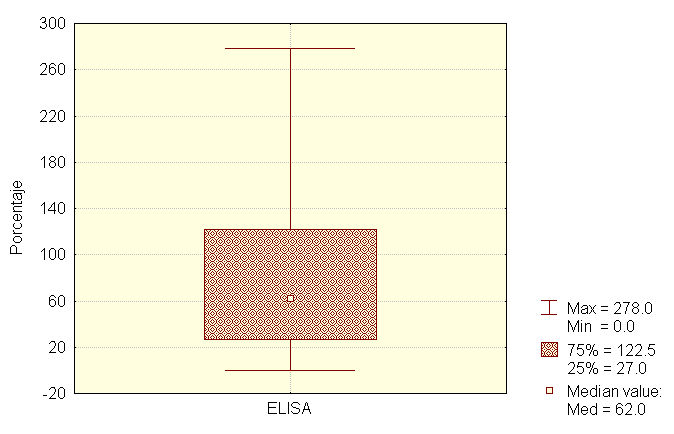
En el gráfico N° 1 se observan los valores límites obtenidos por la técnica de ELISA, del total de muestras analizadas, cuyos valores fluctuaron entre 0 y 278. El vcalor mediano estableció que el 50% de las observaciones se encontraron sobre 62, así mismo el área achurada se delimitó por los valores de los percentiles (25 y 75) y concentró el 50% del total de las observaciones.
Distribución de frecuencias para ELISA y SN.

Gráfico
1: Medidas de resumen de sueros analizados por ELISA, según porcentajes
de DO (n=500).
Sumary of values tested by ELISA according
OD porcentages.
En el gráfico N° 2 se observan los valores límites obtenidos mediante la prueba de SN del total de las pruebas analizadas, cuyos valores fluctuaron entre 0 y 447. El valor mediano estableció que el 50% de las observaciones se encontró sobre 7 y al igual que en el gráfico N° 1, el área achurada se delimitó por los valores de los percentiles (25 y 75), concentrando el 50% del total de las observaciones.
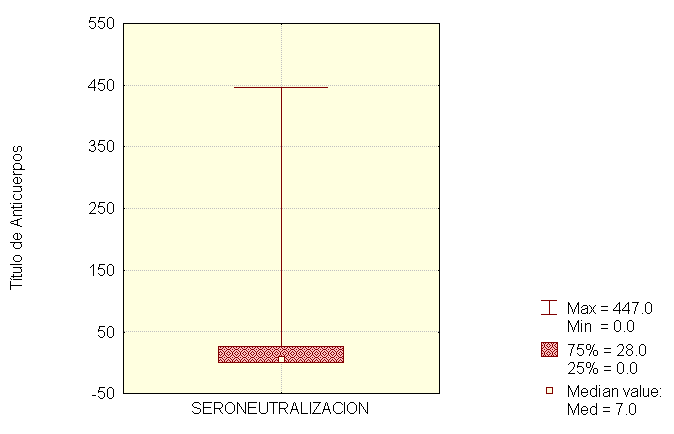
Gráfico
2: Medidas de resumen de sueros analizados por SN, según título
de anticuerpos (n=500).
Sumary of values analized by SNT according antibody titles.
Determinación del coeficiente de Correlación.
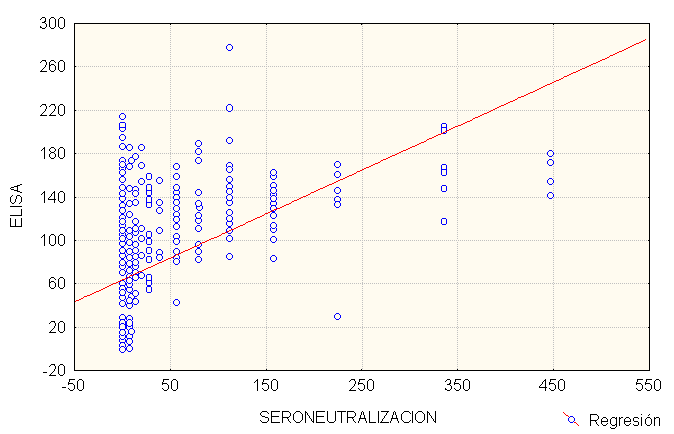
En el gráfico N° 3 se presenta la dispersión de los sueros analizados y revela la existencia de asociación entre ambas variables, en este caso, los valores obtenidos mediante las pruebas de ELISA y SN, respectivamente. Por medio de la orientación que muestra la nube de puntos de este diagrama, se establece una asociación de tipo positiva.
Sobre la base de lo anteriormente descrito, se calculó el coeficiente de correlación de Spearman que asocia los porcentajes de DO ontenidos por ELISA y los títulos alcanzados por SN. Para la totalidad de los sueros (n=500), resultó ser r=0,61 con p<0,05, lo que estableció una mediana asociación entre ambas técnicas, teniendo en cuenta que este coeficiente presenta un rango de -1 a +1.
Este mismo coeficiente, aplicado solo a los sueros diagnosticados positivos por ambas pruebas (n=252), resultó con un valor de r=0,69 con p<0,05.
DISCUSIÓN
La prueba de SN es la más comunmente utilizada en todo el mundo para la determinación de niveles de anticuerpos frente al virus de DVB y el Servicio Agrícola y Ganadero de Chile (SAG), la considera como prueba oficial en el país; sin embargo, no existe ninguna cepa de virus DVB universalmente aceptada como cepa de referencia para ser usada por esta técnica. Las más comunmente utilizadas son las cepas citopáticas NADL, Singer y Oregon C24V (Edwards, 1990). Esto último es relevante puesto que los títulos de anticuerpos obtenidos con una u otra cepa pueden diferir de un laboratorio a otro. En todo caso ella se considera como una prueba altamente específica, que se basa en la detección de anticuerpos neutralizantes que surgen como respuesta protectora del animal frente a una infección viral. Las limitantes que posee no son pocas, principalmente referente a la gran subjetividad en la lectura de la prueba, disponibilidad de tiempo, altos costos en la obtención y mantención de cultivos celulares y posibles contaminaciones no deseadas de ellos (Dinter, 1989). Muchas razones, además de las mencionadas anteriormente pueden provocar diferencias en los resultados, entre ellas la diversidad antigénica de los aislados del virus DVB (Bolin y col., 1992), que genera diferencias radicales en el título de anticuerpos obtenido de un mismo animal al utilizar 2 cepas diferentes, por lo que algunos laboratorios han instaurado el uso de un "pool" de antígenos virales, lo que obviaría esa situación. Existen otras diferencias producto de la variación en la realización de la técnica, como son el tipo de células utilizado y el nivel del pasaje celular empleado (Edwards, 1990).
La prueba de ELISA ha demostrado ser una herramienta efectiva en el diagnóstico de la enfermedad, dadas sus múltiples ventajas, entre las cuales cabe destacar su automatización, estabilidad de sus reactivos, medición de los resultados en forma objetiva mediante instrumentos, utilización de pequeñas cantidades de reactivos y bajo nivel de peligro biológico (Meléndez y col., 1987). Además resulta ser una prueba de diagnóstico rápida sobre un gran número de muestras y muy versátil pues puede utilizarse indistintamente en suero sanguíneo, plasma o leche (Dinter, 1989).
Las desventajas que se le atribuyen a la prueba de ELISA se refieren principalmente a la posibilidad de reacciones inespecíficas, reactividad cruzada y sensibilidad a inhibidores de la actividad enzimática, todo lo cual se reduce notoriamente al utilizar una prueba de ELISA comercial (Meléndez y col., 1987), como lo fue en este estudio.
Se demostraron diferencias en cuanto a los resultados serológicos obtenidos en cada una de las dos pruebas utilizadas, de modo que se obtuvo sueros positivos o negativos en ambas muestras, sueros positivos para ELISA y negativos para SN y sueros negativos para ELISA y positivos para SN (Cuadro N° 4). En relación a los sueros que resultaron positivos a ELISA y negativos a SN, se podría explicar porque el método puede detectar antígenos heterólogos del virus que infectó a los animales y que producen una respuesta inmune baja, traducida en pequeñas concentraciones de anticuerpos sólo detectadas por la gran sensibilidad que posee la prueba de ELISA (Donis y Dubovi, 1987b).
Los resultados negativos a la detección de anticuerpos frente a DVB, por la prueba de SN, se pueden apoyar también en los estudios de Xue y col., (1990) que establecen que la glicoproteína viral gp53 es la principal responsable de la neutralización viral y sólo unos pocos epítopes de ella contribuyen a la neutralización. Además, las variaciones genéticas que sufre el virus y que se ponen en evidencia mediante estudios con anticuerpos monoclonales, determinan variantes antigénicas incapaces de ser neutralizadas (Bolin y col., 1988). Por ello, el uso de ensayos inmunoenzimáticos de la proteina no estructural p80 del virus DVB, polipéptido presente en todas las cepas del virus y producido en gran cantidad durante la replicación viral, asegura en la prueba de ELISA la detección de un gran número de seroreaccionantes al agente (Donis y Dubovi, 1987a). La prueba de ELISA utilizada en este estudio usa como antígeno viral las proteínas no estructurales 125/80.
La detección de anticuerpos frente al virus DVB por SN y no por ELISA se podría explicar por la carencia de ciertos epítopes antigénicos en el "kit" comercial utilizado que pudieran estar presentes en la cepa München usada en la SN. Es necesario recordar también que en casos de contaminación accidental de cultivos celulares utilizados para la SN con cepas ncp de DVB a trvés del suero fetal utilizado podría generar resultados erróneos en el serodiagnóstico (Abraham, 1993).
Estudios efectuados por Chu y col., (1985), Durham y Hassard (1990) y Horner y Orr (1993), revelan que existe una alta correlación en la detección de anticuerpos anti-DVB entre ambas técnicas, sin embargo la técnica de ELISA resulta ser más sensible al detectar bajas concentraciones de anticuerpos. En este estudio se encontró relación entre los títulos seroneutralizantes y los porcentajes de DO determinados por ELISA, alcanzando valores de correlación positivos y de magnitud mediana (gráfico N° 3), lo que permite inferir que se comparten ciertas proteínas virales del virus DVB y son reconocidas por los anticuerpos detectados tanto por ELISA como por SN. Por otra parte, esta asociación resultó ser estadísticamente significativa, lo que es corroborado por el trabajo de Graham y col. (1997), quienes estandarizaron un ELISA para las enfermedades virales Rinotraqueítis Infecciosa Bovina (RIB), Parainfluenza 3 (PI-3), Virus Respiratorio Sincicial Bovino (VRSB) y DVB en forma exitosa en la determinación cuantitativa de anticuerpos que demostró correlacionarse significativamente con los títulos obtenidos por SN.
Por el contrario, estudios realizados por Campodónico (1998), que relacionaron DO determinadas por ELISA con log10 de los títulos neutralizantes, no lograron demostrar esa correlación. Si bien es cierto se determinó una asociación positiva entre ambas variables, ella fue baja y no significativa.
Los resultados obtenidos en este trabajo indican que, ELISA como prueba serológica utilizada en la detección de anticuerpos anti-DVB, posee alta sensibilidad y una especificidad relativa respecto a la prueba de SN. Siendo la sensibilidad la capacidad de una técnica de dar un resultado positivo, cuando el individuo está realmente positivo (Smith, 1995), los sueros diagnosticados negativos a SN evidencian la mayor capacidad que tiene ELISA en detectar los verdaderos positivos. Algunos estudios apoyan lo anterior al referirse a que la prueba de ELISA utiliza antígenos conservados, por lo que desarrolla una mayor reactividad, Bock y col. (1986), demostraron el eficiente uso de la técnica de ELISA en el diagnóstico de DVB en forma rápida y sobre un gran número de muestras.
El análisis estadístico de las pruebas serológicas utilizadas en el estudio, muestra diferencias significativas entre ambas, por medio de la prueba de McNemar, con p<0,05 se descartó el azar y se demostró que si hay diferencias en la detección entre ambas pruebas. Según la estadística Kappa, que mide el grado de concordancia existente entre las dos técnicas, se obtuvo un valor moderado (cuadro N° 5), que segín Martin y col. (1987), determina incertidumbre al precisar cuál de las pruebas provee respuestas más valederas al ser comparadas entre allas y en ausencia de datos de sensibilidad y especificidad.
En conclusión, los resultados obtenidos permiten manifestar que la prueba de ELISA comercial utilizada presenta una mayor sensibilidad que la prueba de SN para el diagnóstico de anticuerpos anti-DVB, que resulta eficiente en la identificación de animales reaccionantes, pudiendo contribuir a evaluar la tasa de infección en estudios epidemiológicos, de manera rápida y sobre grandes poblaciones.
Además, la determinación de animales seronegativos a la prueba, contribuye en forma indirecta a la identificación rápida de animales potencialmente virémicos persistentes, principales responsables de la mantención de la infección en los rebaños.
RESUMEN
El complejo diarrea viral
bovina/enfermedad mucosa (DVB/EM), es una enfermedad viral ampliamente diseminada
en el mundo y muy importante por su acción a nivel de los parámetros
productivos y reproductivos del rebaño. En Chile, se ha informado de
prevalencias prediales superiores al 60%, lo que hace necesario disponer de
técnicas de diagnóstico lo suficientemente adecuadas y confiables
que permitan un diagnóstico rápido y de un gran número
de muestras.
El método oficialmente aceptado en el país
para el diagnóstico de DVB es la prueba de seroneutralización
(SN), la que detecta la presencia de anticuerpos contra el agente causal a nivel
del suero sanguíneo y que se considera de buena sensibilidad y especificidad,
sin embargo presenta algunas desventajas por la subjetividad de su lectura y
lo engorroso de su técnica.
El propósito de esta investigación
fue la comparación de la SN (como prueba de referencia), con un "kit"
inmunoenzimático (ELISA) comercial, en cuanto a sensibilidad y especificidad
en la detección de anticcuerpos anti-DVB. Para ello, sae analizaron 500
muestras de sueros bovinos provenientes de 50 planteles lecheros de la X Región
de Chile.
Los resultados obtenidos indican que, SN detectó
278 sueros como positivos mientras que ELISA detecto 347, lo que representa
para ELISA una sensibilidad y especificidad relativas de 91% y 57%, respectivamente.
Mediante la prueba de McNemar, se establecieron diferencias estadísticamente
significativas (p<0,05), en cuanto al serodiagnóstico obtenido por
ambas pruebas y, por medio del método estadístico Kappa, una mediana
concordancia entre ellas. Al asociar los títulos de SN con las densidades
ópticas resultantes de la prueba de ELISA, se obtuvo una asociación
positiva entre esos valores.
Se postula que ELISA detecta mayor número
de reaccionantes en virtud a su mayor sensibilidad diagnóstica en relación
a SN, por ello resulta ser un método apto para el diagnóstico
serológico de grandes poblaciones animales y de manera absolutamente
objetiva.
* Financiado por Proyecto FONDECYT 1990717
* Dr.BOMMELI AG, Liebefeld-Berna, SUIZA
BIBLIOGRAFÍA
ABRAHAM, A. 1993. Bovine viral diahhrea virus contamination of commercial bovine foetal serum. Isr.J. Vet.Med., 48 : 120-122.
BAKER, J. C. 1987. Bovine viral diarrhea virus: A review. J.A.V.M.A., 190 : 1449-1458.
BLOOD, D. C., O. M. RADOSTITIS. 1992. Medicina Veterinaria. Enfermedades causadas por virus y clamidias. Vol II, 7a ed. Nueva Editorial Interamericana, México.
BOCK, R. E., G. W. BURGESS, I. C. DOUGLAS. 1986. Devolopment of an enzyme linked immunosorbent assay (ELISA) for the detection of bovine serum antibody to bovine viral diarrhea virus. Aust.Vet.J., 63: 406-408.
BOLIN, S. R., V. MOENNING, N. E. GOURLY, J. RIDPHATH. 1988. Monoclonal antibodies with neutralizing activity segregate isolates of bovine virus dirrhea virus into groups. Arch.Virol., 99 : 117-123.
BOLIN, S. R., J. RIDPATH. 1992. Differences in virulence between two noncytopathic bovine viral diarrhea virus in calves. Am.J.Vet.Res., 53 : 2157-2163.
BROWNLIE, J. M., M. C. CLARKE, C. J. HOWARD, D. H. POCOCK. 1987. Pathogenesis and epidemiology of bovine virus diarrhea virus infection in cattle. Ann.Rech.Vét., 18 : 147-157.
CAMPODÓNICO, L. O. 1998. Evalución de un kit comercial ELISA indirecto, para el diagnóstico de la DVB en suero y leche. Memoria de título, M.V., Facultad de Ciencias Veterinarias y Pecuarias. Universidad de Chile. Santiago, Chile.
CELEDÓN, M. O., L. ROCO, G. QUINTEROS, M. SANTIBAÑEZ, P. BERRÍOS. 1997. Puesta en evidencia del virus diarrea viral bovina en bovinos clínicamente afectados. Arch.Med.Vet., 29 : 189-195.
CHU, H. J., Y. C. ZEE, A. A. ARDANS, K. DAI. 1985. Enzyme-linked immunosorbent assay for the detection of antibodies to bovine viral diarrhea virus in bovine sera. Vet.Microbiol., 10 : 325-333
CORAPI, W. V., R. O. DONIS, E. J. DUBOVI. 1988. Monoclonal antibody analyses of citopathic and noncytopathic viruses from fatal bovine viral diarrhea virus infections. J.Virol., 62 : 2823-2827.
CORIA, N. F.., M. J. F. SCHMERR, A. W. McCLURKIN, S. R. BOLIN. 1984. Differentiation of cytopathicand noncytopathic isolates of bovine viral diarrhea virus. Am.J.Vet.Res., 45 : 2129-2131
DANIEL, D. W. 1978. Applied nonparametric statistics. Houghton Mifflin Co., Boston, USA.
DINTER, Z. 1989. Diagnostic Virology. A review of methods at the National Veterinary Institute. Coordinated research programme on animal disease dignostics. National Veterinary Institute, Uppsala, Sweden.
DONIS, R. O., E. J. DUBOVI. 1987a. Differences in virus-induced polypeptides in cells infected by cytopathic and noncytopathic biotypes of virus diarrhea-mucosal disease virus. Virology, 158 : 168-173.
DONIS, R. O., E. J. DUBOVI. 1987b. Molecular specificity of the antibody responses of cattle naturally and experimentally infected with cytopathic and noncytopathic bovine viral dirrhea virus biotypes. Am.J.Vet.Res., 48 : 1549-1554.
DUBOVI, E. J. 1990. The diagnosis of bovine viral diarrhea infections: A laboratory view. Vet.Med., 85 : 1133 - 1139.
DUFFEL, S. J., J. W. HARKNESS. 1985. Bovine virus dirrhea mucosal disease infection in cattle. Vet.Rec., 117 : 240-245.
DURHAM, P. J., L.E. HASSARD. 1990. An enzyme-linked immunosorbent assay (ELISA) for antibodies to bovine viral diarrhe virus. Vet.Microbiol., 22 : 1-10.
EDWARDS, S. 1990. The diagnosis of bovine virus diarrhea/mucosal disease in cattle. Rev.Sci.Tech.Off.Int.Epiz., 9 : 115-130.
ELLIS, J. A., K. H. WEST, V. S. CORTESE, S. L. MYERS, S. CARMAN, K. M. MARTIN, D. M. HAINES. 1998. Lesions and distribution of viral antigen following an experimental infection in young seronegative calves with virulent bovine viral diarrhea virus-type II. Can.J.Vet.Res., 62 : 161-169.
FAO, ORGANIZACIÓN DE LAS NACIONES UNIDAS PARA LA AGRICULTURA Y LA ALIMENTACIÓN. 1985. Manual de técnicas de diagnóstico virológico.
FIEDLER, H., V. CUBILLOS, E. PAREDES, G. REINHARDT, S. RIEDEMANN, M. NIEDDA, M. AGUILAR. 1986. Enfermedad mucosa/diarrea viral bovina. Hallazgos anatomo-patológicos de los primeros casos en Chile. Arch.Med.Vet., 18 : 151-155.
FULTON, R.W., J. T. SALIKI, A. W. CONFER, L. J. BURGE, J. M. D'OFFAY, R. G. HELMAN, S. R. BOLIN, J. F. RIDPATH, M. E. PAYTON. 2000. Bovine viral diarrhea virus cytopathic and noncytopathic biotypes 1 and 2 genotypes in diagnostic laboratorory accessions: clinical and necropsy samples from cattle. J.Vet.Diagn.Invest., 12 : 33-38.
GILLESPIE, J. H., J. A. BAKER, K. McENTEE. 1960. A cytopathogenic strain of virus diarrhea virus. Cornell Vet., 50 : 73-79.
GRAHAM, D. A., K. A. MAWHINNEY, J. McSHANE, T. J. CONNOR, B. M. ADAIR, M. MERZA. 1997. Standarization of enzyme-linked immunosorbent assays (ELISAS) for the quantitative estimation of antibodies specific for infectious bovine rhinotracheitis virus, respiratory syncytial virus, parainfluenza-3 virus, and bovine viral diarrhea virus. J.Vet.Diagn.Invest., 9 : 24-31.
HORNER, G. W., D. M. ORR. 1993. An enzyme-linked immunosorbent assay for detection of antibodies against bovine pestivirus. New.Z.Vet.J., 41 : 123-125.
MARTIN, S. W., A. H. MEEK, P. WILBERG. 1987. Veterinary epidemiology. Principles and methods. Iowa State University Press, Iowa, USA.
MAYR, A., P. A. BACHMANN, B. BIBRACK, G. WITTMANN. 1974. Virologische Arbeitsmethoden. Band II. Serologie. Gustav Fischer Verlag, Stuttgart.
MELÉNDEZ, L. V., G. G. SCHURIG, A. A. SCHUDEL, J. E. POCIUS, L. M. DELLERS. 1987. Manual de diagnóstico rápido de enfermedades virales de los animales utilizando métodos inmunoenzimáticos. Salud animal. Publicación científica N° 15, San José, Costa Rica.
MINISTRY OF AGRICULTURE, FISHERIES AND FOOD. 1978. Manual of veterinary investigation laboratory techniques. Part 8. Virology 2nd ed. Tolcarne Drive, Pinner, Middlesex, England.
NIE, N. H., C. H. HULL, J. G. JENKINS, K. STEINBRENNER, D. H. BENT. 1975. SPSS: Statistical package for the social sciences. 2nd ed. McGraw-Hill Inc., USA.
PIZARRO, J., M. O. CELEDÓN, M. AGUILERA, A. CALISTO. 1999. Genetic characterization of bovine viral diarrhea viruses isolated in Chile. World Vet. Congr., Lyon, France, 23-26 september.
REINHARDT, G., S. RIEDEMANN, H. FIEDLER, M. NIEDDA, M. AGUILAR, V. CUBILLOS, E. PAREDES. 1986. Diarrea viral bovina/enfermedad mucosa. Primer aislamiento del agente causal en Chile. Arch.Med.Vet., 18 : 157-161.
RIDPATH, J. F., S. R. BOLIN, J. KATZ. 1992. Comparison of nucleic acid hibridization and nucleic acid amplification using conserved sequences from the 5' noncoding region for detection of bovine viral diarrhea virus. J.Clin.Microbiol., 31 : 986-989.
SMITH, R. D. 1995. Veterinary clinical epidemiology. A problem oriented approach. 2nd ed. CRC Press Inc., USA.
WHIMSTER, W. F. 1997. Biomedical research. How to plan, publish and present it. Springer Verlag, London.
XUE, W., F. BLECHA, H. C. MINOCHA. 1990. Antigenic variations in bovine viral diarrhea viruses detected by monoclonal antibodies. J. Clin.Microbiol., 28 : 1688-1693.
Aceptado: 17.07.2001