Cuadernos de Cirugía,
Vol. 17 N° 1, 2003, pp. 95-102
DOI: 10.4206/cuad.cir.2003.v17n1-15
ARTÍCULO DE ACTUALIZACIÓN
Cirugía de control de daños. Enfrentamiento actual del trauma
Sebastián Soto G, Roberto Oettinger W, Julio Brousse M y Gonzalo Sánchez C. *
Servicio de Cirugía Hospital Clínico
Regional de Valdivia.
Instituto de Cirugía, Facultad de Medicina, Universidad Austral de Chile.
* Interno de Medicina, Universidad Austral de Chile.
Resumen
Las causas de muerte más frecuentes en trauma son TEC graves, hemorragias masivas y falla orgánica múltiple. Igualmente las alteraciones metabólicas durante post cirugías prolongadas en politraumatizados, así como la reanimación excesiva, son causa de muerte en trauma penetrante. Considerando lo anterior, durante la década de los 90, surge una nueva forma de enfrentamiento quirúrgico en casos de trauma extenso, basada en secuencias preestablecidas, utilizando técnicas simples para enfrentar la urgencia, postergando el tratamiento definitivo hasta que las condiciones metabólicas del paciente lo permitan. Este concepto se conoce como cirugía de control de daños o Damage Control Surgery, cuyo nombre deriva del control de daños realizado en barcos de guerra, tendiente a estabilizarlos al haber sufrido daño severo en el casco. En sus inicios se utilizó en trauma abdominal, y actualmente se extiende a múltiples especialidades, tales como ginecología y traumatología. En este artículo se revisa la perspectiva histórica, la actitud quirúrgica y las complicaciones potenciales de este enfrentamiento.
Palabras claves: Cirugía de control de daños; Trauma; Síndrome compartamental abdominal.
Key words: Damage control surgery; Trauma; Abdominal compartamental syndrome.
CONCEPTOS GENERALES Y ASPECTOS HISTÓRICOS
En los años 70 y 80, el cirujano enfrentado al trauma tenía una conducta agresiva, y frente a hallazgos intraoperatorios complejos intentaba darles solución definitiva, prolongando considerablemente el tiempo quirúrgico, reponiendo excesivamente fluidos, permitiendo la aparición de complicaciones metabólicas, hoy conocidas como la tríada mortal del trauma: hipotermia, coagulopatía y acidosis. Habitualmente los pacientes sobrevivían a la cirugía pero fallecían en las horas siguientes en UCI, producto de trastornos de la coagulación o por falla orgánica múltiple (FOM). Debido al aumento progresivo en la energía del trauma con el devenir de los años, el tiempo quirúrgico se ha alargado conllevando mayor morbilidad y mortalidad, lo que provoca la aparición de este nuevo enfoque con el fin mejorar estos índices1,2.
En el año 1900 se describe por primera vez el packing intrabdominal en la forma de packing hepático. En aquellos años se realizaba suturando material absorbible o irreabsorbible al sitio de la hemorragia, produciéndose un sangrado incoercible al momento del retiro de dicho material. Por lo anterior, se pone atención en el enfoque militar del trauma que se basaba en el uso de medidas sencillas con el fin de salvar la vida en el campo de batalla, llegando a su apogeo durante la II Guerra Mundial en que a todo soldado con herida de colon, se le realizaba indistintamente una colostomía1-3.
En 1968 cobra nuevo vigor la utilización del packing hepático al reportar sobrevida de un caso en que se realiza con gasa, retirándola con éxito y sin sangrado a los 6 días de instalada. En 1981, Feliciano y cols. reportan sobrevida en 9 de 10 pacientes tratados de esta forma4-6. Al año siguiente este enfoque se extiende a otros órganos y se establece el beneficio de esta técnica al evitar la aparición de hipotermia, coagulopatía y acidosis, tríada letal en todo paciente traumatizado4,7-9.
ENFOQUE DEL CONTROL DE DAÑOS
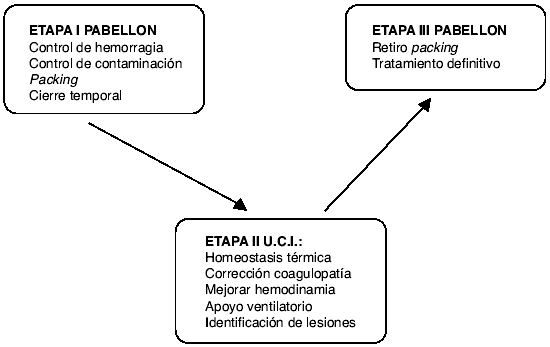
Se diferencian 3 etapas
(Figura 1):
1. Laparotomía inicial.
2. Resucitación.
3. Cirugía definitiva.
Laparotomía inicial.
La decisión de una cirugía abreviada se debe tomar dentro de los primeros 15 minutos de operación, lo que raramente ocurre en equipos poco familiarizados con esta técnica10. Las condiciones locales que llevan a escoger esta cirugía incluyen, hemorragia masiva, hipotermia, coagulopatía, inestabilidad hemodinámica e imposibilidad de cierre de tórax o abdomen producto de edema visceral9. A pesar de lo anterior, los criterios de exclusión no están bien definidos. Morris y cols. identifican 3 categorías de pacientes que deben ser excluidos, mayores de 70 años, TEC severo y paro cardiorrespiratorio prehospitalario11. Lo anterior es bastante aceptado, salvo la edad, ya que mientras más añoso el paciente, más beneficios obtiene con esta técnica.
Debido a la falta de protocolos para definir la técnica de cierre provisorio, ésta queda a elección del equipo tratante. Una opción es la utilización de pinzas de campo, abarcando 1 cm en cada borde de la herida y dejando 1 cm entre sí. Es bastante útil, ya que permite una apertura rápida incluso en UCI de ser necesario.
Otra opción es la utilización de una Bolsa Bogotá2. Este concepto nace en el Hospital Santa Fe de Bogotá, Colombia, donde la falta de recursos lleva a un grupo de cirujanos a utilizar bolsas recolectoras de orina estériles, cortadas a través de su diámetro mayor, con el fin de cerrar en forma transitoria el abdomen fijándola a la piel con pinzas de campo o sutura con nylon corrido5 (Figuras 2, 3 y 4). Las ventajas de esta técnica incluyen bajo costo, disponibilidad y transparencia, que permite visualizar sangrado, necrosis o filtración de contenido intestinal12,13.
De utilizar la técnica de packing para algún órgano, debe realizarse con gasas o compresas sobre y bajo la lesión con el fin de comprimirla en ambos sentidos, teniendo presente que puede desencadenar aumento progresivo en la presión intrabdominal10.
 |
| FIGURA 1. Diagrama enfoque control de daños. |
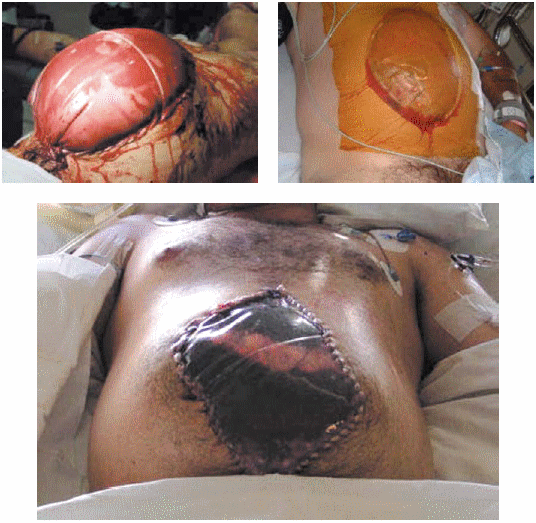 |
| FIGURAS 2, 3 y 4. Bolsa Bogotá. |
Existen como alternativa, para casos de sangrado intrahepático, el uso de sonda Foley o Sengstaken Blakemore. Esta última puede utilizarse en lesiones hepáticas con el balón gástrico insuflado por detrás del hígado y el esofágico taponando el sitio de sangrado10,11,14.
Siempre hay que tener presente la embolización angiográfica cuando se disponga de ella14.
A continuación se describirán brevemente ciertas técnicas para órganos específicos.
Hígado
La técnica básica para el control de hemorragia es el packing perihepático, de la forma antes descrita, que detiene la mayoría del sangrado, salvo el proveniente de arterias de gran calibre. Para realizarlo adecuadamente el hígado debe ser comprimido en forma anteroposterior, lo que se logra mediante la movilización del ligamento hepático derecho e instalando compresas por delante y detrás de éste, como también en los espacios hepatorenales. De esta forma puede ser controlado incluso el sangrado de la vena cava inferior y venas retrohepáticas. De persistir la hemorragia por falla de coagulación, el manejo ideal es la embolización angiográfica selectiva, o el uso de sellantes a base de fibrina, tal como fibrin glue, cuyo costo es prohibitivo en nuestro medio14,15.
Bazo
Exceptuando las lesiones menores que pueden ser manejadas con sutura primaria, la esplenectomía es la técnica de elección.
Grandes vasos abdominales
El mejor abordaje de la aorta abdominal se logra con la rotación de todas las vísceras a izquierda left medial visceral rotation, también conocida como maniobra de Mattox, ya que se expone la aorta abdominal en toda su longitud (Figura 5). De esta forma en manos experimentadas, la aorta es rápidamente reparada con sutura primaria o con prótesis. En caso de lesiones de vasos ilíacos es mejor la utilización de un shunt por sobre la lesión con tubos endotraqueales, permitiendo suturar sin inconvenientes (Figura 6).
En casos de hematoma retroperitoneal asociado a fractura de pelvis, reparar primero esta última y luego manejar el hematoma, si no se traduce en sangrado incontrolable que lleva a la muerte.
Tubo digestivo
Luego de controlada la hemorragia se explora la cavidad, identificando sitios de filtración de contenido intestinal que se controlan con sutura primaria con el fin de evitar mayor contaminación. En casos de lesiones extensas se resecan los segmentos comprometidos y se cierran ambos cabos, dejando la reconstrucción para un segundo tiempo.
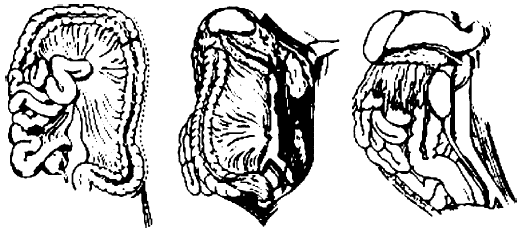 |
| FIGURA 5. Maniobra de Mattox. |
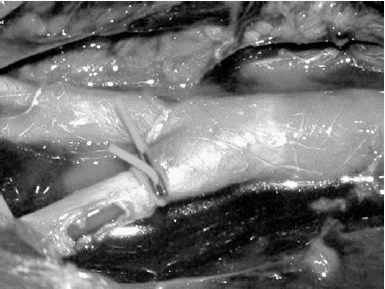 |
| FIGURA 6. Shunt arteria iliaca izquierda. |
Páncreas
Las lesiones pancreáticas siempre se reparan en segundo tiempo y sólo se desbridan, ya que siempre se asocian a lesiones de otros órganos.
Pulmón
La mayoría de los casos van a resección, no se aceptan lobectomías regladas, debe usarse el método más sencillo posible para controlar sangrado y fugas de aire, siendo ideal el uso de grapadoras lineales, lo que permite preservar la mayor cantidad posible de tejido pulmonar funcionante. Las lesiones de estructuras hiliares deben controlarse en un primer momento mediante presión digital, teniendo presente que, de clampearse, el 50% de los pacientes fallece por falla cardíaca derecha.
Resucitación.
Los desafíos de esta etapa deben ser enfrentados en UCI por un equipo multidisciplinario, basados en la reevaluación constante. El objetivo principal es evitar la aparición de la tríada consistente en hipotermia, acidosis y coagulopatía, por lo tanto la corrección de lo anterior y la mantención de una función pulmonar adecuada son fundamentales.
Corrección de la temperatura
Es la primera prioridad luego de la laparotomía inicial, ya que todo politraumatizado pierde 4,6º C por hora durante la cirugía9. Hipotermia se define como temperatura corporal menor de 35º C. Afecta a todos los sistemas corporales y desencadena trastornos de la coagulación, ya que por más que se aporten plaquetas y plasma fresco congelado, la cascada de coagulación no se desencadena si la temperatura corporal es inferior a 34º C9.
Una buena forma de evitar esto es el uso de cobertores eléctricos y circulación de aire temperado en la sala, evitando siempre la excesiva exposición cutánea. El volumen a aportar debe ser temperado y, de ser necesario, se instalan tubos pleurales para realizar lavados constantes con suero tibio, teniendo presente el uso de circulación extracorpórea si la temperatura corporal es menor de 33º C3,10,16.
Corrección de la coagulopatía
En aquellos pacientes que continúan con sangrado, éste se hace evidente dentro de la primera hora posterior a la laparotomía inicial. El desafío radica en determinar si el sangrado se debe a alteraciones en la cascada de la coagulación o a una hemostasia insuficiente. Siempre tener presente que la causa más común en pacientes politransfundidos es la trombocitopenia, ya que el aporte de gran cantidad de cristaloides y glóbulos rojos produce dilución de las proteínas que actúan en la cascada de la coagulación. Además el clampeo por más de 30 de la aorta por sobre el tronco celíaco se traduce en disfunción hepática y el mismo tejido necrótico libera sustancias que alteran la coagulación18.
Para evitar lo anterior la reposición de hemoderivados debe ser constante hasta lograr tiempo de protrombina 1,25 veces al valor normal, recuento de plaquetas mayor de 100,000 x mm3 y fibrinógeno > 100 mg/dl3. Con las condiciones anteriores el paciente puede reingresar a pabellón, de ser necesario, sin mayor riesgo.
Corrección de la acidosis
La acidosis metabólica persistente es signo de hipoperfusión, por lo tanto la terapia se orienta a mantener una oxigenación adecuada, optimizar el gasto cardíaco y asegurar el transporte de oxígeno adecuado mediante un hematocrito de al menos de 21%.
El uso de inótropos positivos debe ser considerado sólo si no se logra oxigenación apropiada con aporte de volumen y niveles de hemoglobina adecuados16.
Por otro lado el aporte de bicarbonato de sodio es regla si el pH es inferior a 7,23.
Optimización de la función pulmonar y oxigenación
Este tipo de pacientes siempre requerirá ventilación mecánica, cuyo objetivo es mantener la saturación de oxígeno sobre 92%, con FiO2 menor de 60%. Se debe monitorizar la presión de arteria pulmonar, manteniendo la presión del capilar pulmonar por sobre 15 mm Hg, aportando 600 cc O2/m2/min. El objetivo final es mantener el pH entre 7,35 7,45, PCO2 entre 35 45 mm Hg y bicarbonato entre 22 27 mmol/lt. La utilización de sedación y bloqueadores neuromusculares es de regla para optimizar el consumo de oxígeno.
Cirugía definitiva
Se lleva a cabo con el paciente normotérmico, hemodinámicamente estable y sin coagulopatía. Las indicaciones para reingresar a pabellón incluyen retiro de packing, cierre de toracotomía o laparotomía, retiro de tejido isquémico o necrótico y tratamiento de lesiones sin riesgo vital que quedaron sin tratar en la cirugía inicial.
No existe consenso respecto al lapso entre la cirugía inicial y la definitiva, pero generalmente ésta se lleva a cabo entre 18 a 48 horas de practicada la primera11,16,17.
La reoperación temprana permite eventualmente un cierre definitivo precoz, que favorece la rehabilitación, permitiendo la movilización a corto plazo, evitando así la aparición de úlceras por presión.
Reoperaciones no planificadas y complicaciones post operatorias.
En este tipo de pacientes las complicaciones son habituales, siendo la más frecuente y mortal la falla orgánica múltiple y los abscesos intrabdominales que causan la muerte en 15-20% de los enfermos5,11,17-19.
Las indicaciones de reoperación no planificada se resumen en la Tabla 1.
CAUSAS
DE REOPERACIÓN NO PLANIFICADA |
1. Sangrado continuo
a pesar de normalización de cascada de coagulación. 2. Presión intrabdominal > 25 cm de agua con alteraciones propias de síndrome compartamental. 3. Peritonitis. |
Síndrome compartamental abdominal
Todo paciente sometido a laparotomía abreviada está en riesgo de sufrir esta complicación, que se define como alteraciones fisiológicas de los órganos intrabdominales producto del aumento de la presión intrabdominal y que de no tratarse oportunamente tiene curso fatal.
Los factores que influyen en su aparición incluyen edema visceral, aporte excesivo de fluidos, packing y sangrado persistente.
Esta complicación se instala dentro de las primeras 24 horas y es de progresión rápida. Clínicamente se presenta con caída del gasto cardíaco, aumento de resistencia vascular periférica, oliguria, anuria, aumento de la presión de vía aérea e hipoxia19-20.
El método más fidedigno para evaluar la aparición de esta complicación es la medición de la presión intravesical a través de sonda Foley de triple lumen.
Aparece cuando la presión intravesical supera los 10 cm de agua y se clasifica de la forma que se muestra en la Tabla 2.
Grado
(cm de agua) |
Presión
intravesical |
I II III IV |
10 15 15 25 25 35 > 35 |
El tratamiento es estándar y consiste en la descompresión, salvo el grado I que se pueden observar por tiempo prudente20-22.
DISCUSIÓN
Con el correr de los años la cirugía, al igual que otras especialidades médicas, se ha visto enfrentada a múltiples desafíos y cambios, dados fundamentalmente por los avances científicos y tecnológicos y por los cambios en los perfiles epidemiológicos.
El enfoque del control de daños en cirugía ha adquirido gran fuerza durante la última década, en base a la experiencia adquirida durante la II Guerra Mundial, y engloba una forma de enfrentar desafíos quirúrgicos en pacientes con lesiones complejas y extensas2.
Este nuevo enfoque deja de lado aproximaciones clásicas frente a cierto tipo de lesiones, por lo cual se requiere mirar a nuestros pacientes a través de una nueva óptica con el fin de resolver sus problemas de la manera más rápida y menos iatrogénica posible. Lamentablemente algunas de las formas tradicionales de enfrentar a pacientes con lesiones complejas se basan en la experiencia personal y no en estudios prospectivos randomizados2,23-25.
Por esto, en los años 80, en forma simultánea en distintos hospitales del mundo se empieza a utilizar alternativas que acorten el tiempo operatorio y disminuyan la mortalidad. Aquellos que inicialmente aplicaban estos conceptos fueron catalogados como cirujanos temerosos y/o malos técnicos. Paradojalmente, hoy son conocidos como padres del trauma moderno, tal como Mattox, Feliciano, Burch, Hirshberg y tantos otros alrededor del mundo.
Este enfoque ha permitido derribar innumerables mitos en trauma, tal como que toda herida penetrante abdominal debía ser explorada. Por otro lado permite simplificar, desde el punto de vista técnico, sobre todo para aquellos cirujanos que se ven enfrentados en forma ocasional a trauma mayor o para aquellos que trabajan en áreas rurales y con pocos recursos, permitiendo así salvar la vida del paciente y derivarlo a centros de mayor complejidad.
En nuestro país existe poca experiencia con este enfoque, salvo en la casa central de la Asistencia Pública de Santiago que funciona en base al trauma, lo que se ve reflejado en la inexistencia de publicaciones nacionales de este tema. Para aquellos que nos sentimos atraídos por el tema del trauma, en cierta medida, nos genera inquietud la escasa cantidad de pacientes de este tipo a los que nos vemos enfrentados, pero al mantenernos al día con los conceptos y técnicas en uso, nos consideramos capacitados para enfrentar este tipo de situaciones cuando sea necesario26.
Aún hoy existen preguntas sin responder y en la medida que se avance en cuanto a conocimiento y tecnología, éstas se acrecentarán y nos incentivarán a seguir respondiéndolas y al mismo tiempo fomentarán la aparición de nuevas interrogantes. Actualmente los esfuerzos en ese sentido están orientados a determinar predictores de sobrevida con el enfrentamiento de control de daños previo al arribo al centro hospitalario23.
REFERENCIAS
1. Sauaia A, Moore FA, Moore EE, Moser KS, Brennan R, Read RA, Pons PT: Epidemiology of trauma deaths: A reassessment. J Trauma 1995; 38: 185-93
2. Mattox K: Introduction, background, and future proyections of damage control surgery. Surg Clin North Am 1997; 77: 753-9
3. Moore E: Staged laparotomy for the hypothermia, acidosis, and coagulopathy syndrome. Am J Surg 1996; 172: 405-10
4. Cue JI, Cryer HG, Miller FB, Richardson JD, Polk HC Jr: Packing and planned reexploration for hepatic and retroperitoneal hemorrhage: Critical refinements of a useful technique . J Trauma 1990; 30: 1007-13
5. Hirshberg A, Mattox K: Planned reoperation for severe trauma. Ann Surg 1995; 222: 3-8
6. Carrillo C, Fogler R, Shaftan G: Delayed gastrointestinal reconstruction following massive abdominal trauma. J Trauma 1993; 34: 233-5
7. Svoboda JA, Peter ET, Dang CV, Parks SN, Ellyson JH: Severe liver trauma in the face of coagulopathy. A case for temporary packing and early reexploration. Am J Surg 1982; 144: 717-21
8. Stone H, Strom P, Mullins R: Management of the major coagulopathy with onset during laparotomy. Ann Surg 1983; 197: 532-5
9. Burch J, Denton J, Noble R: Physiologic rationale for abbreviated laparotomy. Surg Clin North Am 1997; 77: 779-82
10. Hirshberg A, Walden R: Damage control for abdominal trauma. Surg Clin North Am 1997; 77: 813-20
11. Morris JA Jr, Eddy VA, Blinman TA, Rutherford EJ, Sharp KW: The staged celiotomy for trauma, issues in unpacking reconstruction. Ann Surg 1993; 217: 576-86
12. Tremblay LN, Feliciano DV, Schmidt J, Cava RA, Tchorz KM, et al: Skin only or silo closure in the critically ill patient with an open abdomen. Am J Surg 2001; 182: 670-5
13. De la Fuente M, Mendoza VH, Robledo- Oyarzún F: Cierre temporal de la pared abdominal con polietileno. Cir Ciruj 2002; 70: 157-63
14. Poggetti RS, Moore EE, Moore FA, Mitchell MB, Read RA: Ballon tamponade for bilobar transfixing hepatic gunshot wounds. J Trauma 1992; 33: 694-7
15. Chapman WC, Clavien P, Fung JJ, Block JE: Managing hepatic bleeding with autologous plasma, collagen-based fibrin sealant. Arch Surg 2001; 136: 966-7
16. Gentilello LM, Cobean RA, Offner PJ, Soderberg RW, Jurkovich GJ: Continuous arteriovenous rewarming: Rapid reversal of hypothermia in critically ill patients. J Trauma 1992; 32: 316-27
17. Martin R, Byrne M: Postoperative care and complications of damage control surgery. Surg Clin North Am 1997; 77: 929-42
18. Burch JM, Ortiz VB, Richardson RJ, Martin RR, Mattox KL, Jordan GL Jr.: Abbreviated laparotomy an planned reoperation for critically injured patients. Ann Surg 1992; 215: 476-84
19. Rotondo MF, McGonigal MD, Schwab CW, Kauder DR, Hanson CW: Damage Control: An approach for improved survival in exsanguinating penetrating abdominal injury. J Trauma 1993; 35: 375-83
20. Schein M, Wittmann DH, Aprahamian CC, Condon RE: The abdominal compartment syndrome: The physiological and clinical consequences of elevated intra-abdominal pressure. J Am Coll Surg 1995; 180: 745-53
21. Raeburn CD, Moore EE, Biffl WL, Johnson JL, Meldrum DR, et al: The abdominal compartment syndrome is a morbid complication of postinjury damage control surgery. Am J Surg 2001; 182: 542-6
22. Biffl WL, Moore EE, Burch JM, Offner PJ, Franciose RJ, Johnson JL: Secondary abdominal compartment syndrome is a highly lethal event. Am J Surg 2001; 182: 645-8
23. Asensio JA, McDuffie L, Petrone P, Roldan G, Forno W, et al: Reliable variables in the exsanguinated patient wich indicate damage control and predict outcome. Am J Surg 2001; 182: 743-51
24. Cox EF, Flancbaum L, Dauterive AH, Paulson RL: Blunt trauma to the liver: Analysis of management and mortality in 323 consecutive patients. Ann Surg 1988; 207: 126-34
25. Stone HH, Fabian TC, Satiani B, Turkleson ML: Experiences in the management of pancreatic trauma. J Trauma 1981; 21: 257-61
26. Hirschberg A, Mattox K: Damage Control in Trauma Surgery. Br J Surg 1993; 80: 1501-2