Cuad. Cir. 2007; 21: 31-37
DOI: 10.4206/cuad.cir.2007.v21n1-05
CASO CLÍNICO
Pancreatectomía corporocaudal con preservación esplénica
Francisco Venturelli M 1, Carlos Cárcamo I. 2
1
Residente Cirugía. Instituto de Cirugía. Facultad de Medicina. Universidad Austral
de Chile.
2 Profesor Auxiliar de Cirugía. Facultad de Medicina.
Universidad Austral de Chile. Correspondencia a: ccarcamo@uach.cl.
RESUMEN
En este artículo se presenta un caso clínico de un paciente con tumor de la cuerpo del páncreas, el cual se trató mediante tratamiento quirúrgico prácticando una pancreatectomía corporocaudal con conservación esplénica. Además se revisa el tratamiento quirúrgico de los tumores del cuerpo y cola de páncreas, con especial énfasis en comparar la pancreatectomía distal con conservación esplénica vs la sin ella. Se mencionan las técnicas de conservación esplenica y la técnica laparoscopica con sus resultados. La resección del bazo se asocia a una morbilidad mayor, además que, el resecarlo significa que el paciente debe ser sometido a un esquema de profilaxis contra infecciones. Se concluye que la pancreatectomia distal mas conservación esplenica es la mejor terapia cuando se cumplen sus indicaciones, pero faltan estudios prospectivos randomizados para certificarlo.
Palabras claves: pancreatectomía distal; conservación esplénica; páncreas; Tumor sólido pseudopapilar.
Key words: Distal pancreatectomy; splenic preservation; páncreas; Solid-Pseudopapillary Tumor.
INTRODUCCIÓN
La pancreatectomía distal es la resección del tejido pancreático que se extiende a la izquierda de la línea media. No incluye el duodeno, ni la vía biliar1. Esta cirugía es el tratamiento de elección de tumores benignos y malignos en el cuerpo y cola de páncreas.1,2
La primera resección de páncreas distal fue realizada a fines del sigo XVIII. (1) La cirugía de páncreas durante varias décadas presentó una mortalidad elevada (21%)3. En los últimos años los centros con alto volumen de pacientes, han mostrado resultados bastantes alentadores1. Es así como Fernández del Castillo et al. en 1995 reporta un índice de complicaciones de un 20% con una mortalidad de 1,4% en 71 pacientes pancreatectomizados distales.4
Muchos cirujanos practican la resección del páncreas distal conjuntamente con la resección del bazo, porque es técnicamente más fácil y les permite acortar el tiempo operatorio, no teniendo en consideración que este órgano cumple un rol fundamental en el control inmunológico y metabólico del organismo.5
Se presenta un caso clínico, con el objetivo de dar a conocer la conducta quirúrgica de un tumor de cuerpo de páncreas sin compromiso esplénico en el cual se resecó la porción distal del páncreas conservando el bazo. Además se realiza una revisión de la literatura.
CASO CLINICO
Mujer de 41 años, sin antecedentes mórbidos de importancia. El 31/12/06 comienza con cuadro caracterizado por dolor tipo cólico en hipocondrio derecho de intensidad moderada asociado a vómitos biliosos, motivo por el cual consulta en el hospital de Los Lagos, donde se manejó en forma sintomática. Debido a que la paciente persistió con la sintomatología decide consultar en Valdivia el 2/1/07. En ese momento, se solicita ecografía abdominal que muestra imágenes compatibles con colecistitis aguda litiásica, además de una lesión corporal pancreática de etiología incierta, de aspecto nodular, ovoidea, bien definida cuyo tamaño es de 4 x 3 cm en su diámetro anteroposterior y transversal, respectivamente. Bazo de estructura y tamaño conservado.
Se deriva a la asistencia pública del Hospital Regional Valdivia, donde se constata la persistencia del cuadro. Al examen físico se pesquisa fiebre por lo que se hospitaliza. Hemograma con 14400 GB y pruebas hepáticas normales. Se solicita TAC de abdomen que informa la presencia de una tumoración de partes blandas hipodensa a nivel del cuerpo del páncreas que mide 4,8 x 5,0 cm anteroposterior y transversal, que se contrasta parcialmente con el medio de contraste. Los contornos son bien definidos y regulares, contactando y desplazando la cara posterior del estómago, de la cual impresiona estar separado por un plano de clivaje hipodenso. No se observa dilatación del Wirsung. Proceso Uncinado pancreático de estructura conservada. A nivel interaortocava existen 2 imágenes nodulares con diámetro de 1 cm, compatible con adenopatías. Vesícula de paredes edematosas y con un cálculo de 24 mm.
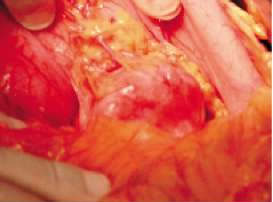
Se toman CEA y Ca -19-9 que resultan en 2,3 y 0,6 U/ml respectivamente. Debido a los hallazgos en la TAC y a que el cuadro clínico cedió con manejo conservador, decide realizar cirugía electiva dándose de alta transitoria el 6/1/07. El 19/1/07 es llevada a pabellón En el intraoperatorio se visualiza una vesícula sin características inflamatorias y un tumor quístico del páncreas que impronta el estómago, de 6 cm de diámetro, no se encuentran nódulos hepáticos ni peritoneales (Figura 1). Se practica una pancreatectomía corporocaudal con preservación esplénica más colecistectomía clásica (Figuras 2 y 3). Se deja un drenaje al lecho por contrabertura el cual se retira al cuarto día postoperatorio dando 30 cc hemático oscuro y se da de alta sin complicaciones.
 |
FIGURA
1. Tumor Corporal de Pancreas |
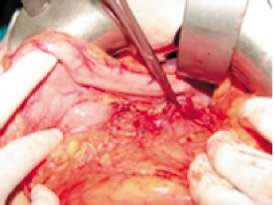 |
FIGURA 2.
Lecho postquirúrgico. Pinza en vasos espléncios.
|
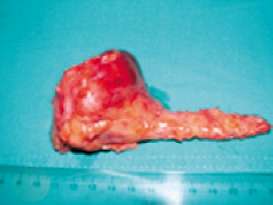 |
| FIGURA 3. Pieza quirúrgica. |
Biopsia diferida informa (20/3/07): Macroscopía: se visualiza una lesión abolonada de 6,5 cm en su diámetro mayor. Al corte se reconoce un tumor sólido de bordes expansivos de color blanco grisáceo con áreas de acentuada hiperemia. Histología: se reconoce neoplasia con patrón sólido, alveolar, pseudopapilar y pseudoglandular. Destaca la presencia de numerosas células de núcleos pleomórficos. Necrosis negativo. Escasas mitosis. Inmunohis-toquímica: Vicentina, CD 56, progesterona, enolasa neuroespecífica, Ki67, CD 10 y galectina 3 positivas (se repitela KI 67 y sale negativa). CEA, PAN CK, CK 7, EMA, Cromogranina, estrógeno negativos. Linfoganglio: 1 sin metástasis.
Diagnóstico: Aspecto histológico compatible con tumor sólido pseudopapilar de páncreas de 6,5 cm de diámetro mayor, sin invasión perineural, límites quirúrgicos negativos.
DISCUSIÓN
Los pacientes esplenectomizados se asocian a un aumento de la morbilidad comparado con la población general (infecciones, enfermedad tromboembólica, etc.)2, 6-9. Es así como en una serie de 19680 pacientes con un seguimiento a 6,9 años, Bisharat N et al. demostró que la incidencia de sepsis post-esplenectomía es de un 3,2% con una mortalidad de 1,4%.6
El mecanismo por el cual aumentarían las infecciones en el postoperatorio inmediato en los pacientes con una esplenectomía no está claro. Algunos autores sugieren que la esplenectomía produciría una disminución en la concentración circulatoria de anticuerpos, en la actividad de macrófagos y en el porcentaje de CD4 y linfocitos.11,12
Debido a la alta mortalidad que tienen las infecciones postesplenectomía, es que se han desarrollado técnicas para preservar este órgano en las pancreatectomías distales.
La pancreatectomía distal con conservación esplénica se puede llevar a cabo mediante dos técnicas. La primera, descrita por Mallet-Guy en 1943, técnica clásica y más utilizada; consiste en dividir los vasos del páncreas y el bazo con cuidado llegando hasta el plano posterior del páncreas, donde se procede a identificar y ligar los pequeños y cortos vasos pancreáticos que son rama de la vena y arteria esplénica2. La segunda, descrita por Warshaw en 1988, consiste en ligar los vasos esplénicos, dejando el bazo irrigado sólo por los vasos gástricos cortos y los gastroepiploicos izquierdos.13
Ambas técnicas tienen inconvenientes. La de Mallet-Guy exige un mayor tiempo operatorio, debido a que es técnicamente más demandante, al tener que realizar una disección cuidadosa de las pequeñas ramas de los vasos esplénicos2, 5. La descrita por Warshaw, tiene el riesgo de producir isquemia del bazo, con el consecuente infarto esplénico, debido a que al ligar sus principales vasos, conlleva una drástica disminución de su irrigación. Sin embargo, hay estudios que muestran que esto no ocurriría2, 10. En el año 2007 Nicolas Carre re, et al., publicó el primer estudio de cohorte retrospectivo que incluyó a 125 pacientes con pancreatectomía distal abierta entre los años 1990 y 2005. En 38 pacientes se trató de conservar el bazo mediante la técnica de Warshaw de los cuales 2 (5,2%) cursaron con infarto esplénico inmediato. De los 36 pacientes restante ninguno tuvo signos de infarto durante 3 meses de seguimiento mediante angiografía, cintigrafía, CT scan o US scan y estudio hematológico (recuento de plaquetas y cuerpos de Howell- Jolly). Si bien este no es un estudio prospectivo, deja una clara evidencia de la seguridad de la esplenectomía con esta técnica, en cuanto a la vitalidad del bazo a largo plazo.2
Sin embargo la preservación esplénica en ocasiones puede ser técnicamente muy difícil y con un alto riesgo de complicación, por lo que la conservación de este órgano debe ser realizada en forma selectiva evaluando caso a caso. Para ello hay que basarse en la relación anatómica de las estructuras, ausencia o presencia de compromiso de la vena esplénica por el tumor, compromiso del hilio esplénico y la extensión de la resección.1
Las indicaciones de esplenectomía en una pancreatectomía distal son1,2:
1. Tumor de la cola del páncreas con sospecha de malignidad.
2. Cáncer de páncreas que necesite la extracción del bazo para conseguir una resección oncológica.
3. Compromiso tumoral de los vasos esplénicos o peripancreáticos.
4. Presencia de compromiso linfonodal al TC
5. Citología o histología que evidencia un adenocarcinoma o carcinoma endocrino.
Cuando no se cumplen estas indicaciones, por ejemplo en el caso de patologías benignas y/o con baja probabilidad de malignización, practicar una esplenectomía es controversial.
Está claro que el resecar el bazo aumenta los riesgos de infecciones severas, por lo que uno debiera en lo posible tratar de preservarlo. El problema es que el tratar de preservar el bazo puede tener igual o más complicaciones que el resecarlo. Como no hay estudios randomizados prospectivos que comparen ambas técnicas, no se puede saber en este momento que conducta es mejor en cuanto a riesgo vs beneficio.
Nicolas Carre re, et al.2 2007 en su estudio de cohorte retrospectivo incluyó a 76 pacientes con tumores pancreáticos benignos y de bajo riesgo de malignidad (31 y 30 respectivamente) 38 fueron sometidos a cirugía conservadora bajo técnica de Warshaw y 36 con esplenectomía con pancreatectomía distal abierta entre los años 1990 y 2005. Sus resultados mostraron que el tiempo operatorio promedio fue de 170 minutos (100350 min) para el grupo conservador y 180 minutos (90300 min) para el radical (p=0.42). El promedio de sangrado fue de 100 ml (401200 ml) para el grupo conservador y 180 ml (501100 ml) para el radical (p= 0.28), el tamaño tumoral fue de 30 mm (10150 mm) en el grupo conservador y 40 mm (580 mm) en el radical (p=0.88.), la mortalidad perioperatoria fue 0 (0%) para el grupo conservador y 1 (3%) para el radical (p=0.31), la estadía hospitalaria fue de 10 días (730) para el grupo conservador y 11 días (746) para el radical (p= 0.06), las complicaciones tardías fueron 7 (18%) para el conservador 6 (16%) para el radical (p=0.76). Todas variables sin diferencias estadísticamente significativas (p>0,05).
Donde sí hubo diferencia fue en la morbilidad: 5 (13%) para el grupo conservador 13 (34%) para el radical (p=0.03)
En el análisis univariado el único factor que mostró ser significativo como riesgo de complicaciones postoperatorias fue la esplenectomía (odds ratio: 3.2; 95%, intervalo de confianza: 1.110.2; p = 0.04).
Durante el seguimiento a 65 +-5 meses, ninguno presentó hipoesplenismo, ni sepsis severa, ni complicación tromboembólica.
En otras series los resultados han sido controversiales. Richardson and Scott-Conner7, en un estudio restrospectivo en 21 pacientes, (10 grupo I: esplenectomía y 11 grupo II: conservación esplénica utilizando ambas técnicas ), no observaron un aumento de la morbilidad postoperatoria (4 complicaciones en el grupo I (40%) vs 3 complicaciones en el II (36%)). En un paciente operado con la técnica de Warshaw ocurrió un infarto esplénico lo cual no se tradujo en mortalidad.
Utilizando ambas técnicas Aldridge and Williamson, reportaron 77 pacientes (42 (55%) con esplenectomía y 35 (45%) sin ella. No hubo mortalidad. En cuanto a la morbilidad, ésta fue de 10 pacientes en el grupo con esplenectomía (24%) vs 7 pacientes en el grupo sin ectomía esplénica (20%) (p>0,05). En los 5 pacientes que se ligaron los vasos esplénicos (técnica de Warshaw) no hubo hipoesplenismo al control con cintigrafía e índices hematológicos.14
Shoup et al.8 demostró que las infecciones perioperatorias y las complicaciones severas son significativamente mayores en los pacientes pancreatectomizados distales con esplenectomía (28% y 11%) que en los pacientes con preservación esplénica (9% y 2%). Los días de hospitalización fueron más en los esplenectomizados (9 vs. 7 días).
Lillemoe et al.1 realizó un estudio retrospectivo entre 1984 y 1997 recolectando 235 pacientes sometidos a pancreatectomía distal electiva, sin diferenciar la técnica quirúrgica, tanto por patologías benignas como malignas. Se excluyeron los pacientes por trauma y cáncer gástrico. Se realizó esplenectomía en el 84% de los pacientes (198 pacientes) y presentaron un índice de complicaciones similar al grupo sin esplenectomía 30% vs 30%. La estadía hospitalaria fue mayor para el grupo sin esplenectomía (21 días vs 13 días (p=0,008). Las diferencias en sangrado intraoperatorio (p=0,14), el tiempo operatorio (p=0,685), la morbilidad (p=0,935) y la mortalidad (p=0,553) no fueron estadísticamente significativas.
Al comparar lesiones benignas (170) y malignas (65), tampoco hubo diferencias en cuanto a estadía hospitalaria (p=0,977), sangrado (p=0,815), tiempo operatorio (P=0,082), morbilidad (P=0,633) y mortalidad (P=0,521)
Benoist S, et al.10, reportaron en 1999 una serie de 40 casos revisados en forma retrospectiva con patología pancreática benigna que fueron tratados mediante una pancreatectomía distal. 15 pacientes fueron sometidos a esplenectomía y 25 a cirugía conservadora con técnica de Mallet-Guy. Los pacientes del grupo conservador presentaron un mayor índice de fistula pancreática con 6 vs 3 casos (40% vs 12%) (p<0,05), así como también más abscesos subfrénicos (27% vs 14%) (p<0,05). No hubo evidencia de hipoesplenismo (trombocitopenia y Howell-Jolly). No hubo mortalidad. No hubo diferencias significativas en relación al total de complicaciones entre ambos grupos 6(40%) en el conservador y 5(20%) en el radical p>0,05. La estadía hospitalaria fue de 19 días (6-46) para el conservador y 12 días (7-45) para el radical (Splenectomy Group) (p<0.05). Con estos resultados Benoist S sugiere reconsiderar la conservación rutinaria del bazo como técnica de elección en lesiones benignas del cuerpo y cola del páncreas.
Chi-Hsun Hsieh et al., utilizando la técnica Mallet-Guy para la conservación esplénica, reportó una serie de 5 casos con tumores benignos. No hubo morbimortalidad. El promedio de duración de la cirugía fue 238 min, pérdida sanguínea 170 ml y la estadía hospitalaria 8,4 días5.
Koukoutsis I et al., revisó en forma retrospectiva una base de datos prospectiva con 49 pacientes con pancreatectomía distal por cáncer y trauma abdominal. La morbilidad fue de 24,1% en las pancreatectomías distales con esplenectomía y un 15% sin esplenectomía (p=0.496) El riesgo de sepsis en tumores benignos fue de (0.28%-1.9%), con un índice de mortalidad de 2.2%.9
Hay varios estudios que muestran que la esplenectomía está asociada a una mayor morbilidad al compararla con la cirugía conservadora2, 7-9. El único trabajo que muestra lo contrario es el de Benoist S, pero no alcanza significancia estadística.10 Al contrario, al evaluar la estadía hospitalaria, la cirugía conservadora presenta más días de hospitalización1, 10. Sin embargo, al parecer, la estadía hospitalaria no solo depende de si se preserva o no el bazo. Nicolas Carre re et al.2 en el 2007, en tumores benignos y de bajo riesgo de malignidad con técnica Warshaw, no encontró diferencias en los días de hospitalización entre 74 pacientes (10 días, 730, para el conservador y 11 días, 746 para el radical (p= 0.06). Por otra parte, Chi-Hsun Hsieh et al., en tumores benignos con técnica de Mallet-Guy, tuvo una estadía hospitalaria similar a la encontrada por Nicolas Carre´re (8,4 días)5. Por lo tanto en tumores benignos y/o de bajo riesgo de malignidad debiera ser similar la estadía hospitalaria en pacientes con y sin esplenectomía.
Aldridge and Williamson,14 en 35 pacientes con ambas técnicas y Benoist S10 en 25 pacientes con la técnica de Mallet-Guy no presentaron infarto esplénico y/o hipoesplenismo. Por otro lado mediante la técnica de Warshaw, Nicolas Carre re, et al.2, 2007, reportó 2 infartos esplénicos inmediatos en 38 pacientes (5,2%) y Richardson and Scott-Conner5 reportaron 1 en 11 pacientes (9%). Por lo tanto la conservación esplénica mediante ambas técnicas es segura en cuanto a la viabilidad del bazo.
Al comparar los 2 estudios que sólo utilizaron una técnica preservadora de bazo, (Nicolas Carre, Warshaw y Benoist S, Mallet-Guy), ninguno tuvo mortalidad. La morbilidad fue mayor para la técnica clásica (Mallet-Guy) (13% vs 40%), así como también la estadía hospitalaria 19 días (6 -46) vs 10 días (730), pero Nicolas Carre tuvo 2 infartos esplénicos vs ninguno de Benoist S.
INFECCIONES Y ESPLENECTOMÍA:
Los pacientes sin bazo tanto funcional como anatómico, tiene un significativo mayor riesgo de presentar infecciones graves como la overwhelming sepsis postesplenectomía. (PSS)15 La (PSS) es producida en un 50-90% por el Streptococcus pneumoniae15,16. Lo sigue el Haemophilus influenzae typo b y en tercer lugar la Neisseria meningitidis. Bacterias menos comunes son la Salmonella, Escherichia coli, Staphylococcus aureus, Pseudomonas aeruginosa, Enterococcus species, Bacteroides species, Plesiomonas shigelloides, Eubacterium plautii and Pseudomonas pseudomallei.17, 18
Singer definió la PSS como una septicemia, meningitis o neumonía usualmente fulminante que ocurre días o años postesplenectomía. Se han reportado casos hasta 40 años postesplenectomía.17 La incidencia de PSS es de un 4.25% a un a 40% con una mortalidad de 50 a 70%, a pesar de los antibióticos y tratamiento médico intensivo.16-18. El 68 % de las muertes ocurre en las primeras 24 hrs y el 80% dentro de las 48 hrs.15 La muerte por sepsis postesplenectomía es 200 veces más prevalente que los pacientes con sepsis en la población general.15,16,19 Su presentación clínica se caracteriza por un corto pródromo de fiebre baja, con calosfríos, faringitis, dolor muscular, vómitos y/o diarrea. En pocas horas pasa rápidamente a un shock séptico con hipotensión y anuria. Generalmente no hay evidencia clínica de un foco de infección. Además se le puede agregar CID, púrpura fulminante, gangrena de la extremidad, convulsiones y coma.17
El diagnóstico del hipoesplenismo o aesplenia, se hace mediante la visualización sanguínea de los cuerpos de Howell-Jolly (remanentes nucleares de los eritrocitos que son removidos normalmente por el bazo), trombocitosis y monocitosis.15,17,18
La prevención de la PSS es a través de 3 métodos: inmunoprofilaxis, profilaxis antibiótica (amoxicilina) y educación. En muchos estudios hay una baja adherencia a medidas preventivas.19,20
1. Inmunoprofilaxis
Vacuna antineumocócica (PPV23): Esta vacuna está recomendada para pacientes esplenectomizados. Contiene 23 serotipos que son la causa del 85 a 90% de las infecciones invasivas en el adulto y el niño15, 17. La vacuna debe ser administrada como mínimo 2 semanas antes de la cirugía. En caso de esplenectomía de urgencia se debe vacunar inmediatamente al recuperarse de la cirugía o al alta hospitalaria.15 Si se realiza una QMT o RDT inmunosupresora la vacunación debe retardarse 6 meses.15
No hay consenso sobre la reinmunización en pacientes aesplénicos o hipoesplénicos. La USA Center for Disease Control (CDC) and Prevention Advisory Committee on Immunisation Practices (ACIP) recomienda la revacunación con PPV23 en pacientes hipoesplénicos y aesplénicos después de los 5 años.18,21
Vacuna contra el Haemophilus influenzae type b: La Hib está recomendada para pacientes con hipoesplenismo y aesplénicos. Su efecto en prevenir la PSS es controversial y la reinmunizacion no está clara.15, 17, 18
Vacuna contra la Influenza: Esta vacuna está recomendada anualmente porque diminuye el riesgo de infecciones por neumococo y Haemophilus influenzae.15
2. Antibióticos
El uso de antibióticos profilácticos es controversial porque no hay estudios de buena calidad que demuestren su eficacia en pacientes esplenectomizados.16
La profilaxis antibiótica se puede realizar con amoxicilina, amoxi-clavulánico o cefuroximo.17,18
3. Educación de los pacientes:
Hay estudios que muestran que hasta un 84% de los pacientes esplenectomizados no saben que tienen un aumento en el riesgo de presentar infecciones ni la precauciones que deben tomar.15
Si los pacientes son educados para pedir atención medica inmediata la mortalidad desciende a un 10%.17
PANCREATECTOMÍA DISTAL LAPAROSCÓPICA:
El primer reporte de pancreatectomía distal con conservación esplénica fue presentado por Gagner M quien de 9 casos, sólo 1 terminó con una esplenectomía.22
Mabrut el al en el año 2005 publicó el estudio multicéntrico más grande, con 96 pancreatectomías distales de las cuales, en 72 se conservó el bazo.23
Tataza et al.24 en el 2003 publicó las indicaciones para la pancreatectomía distal laparoscópica:
Lesiones benignas o de bajo gado de malignidad (pancreatitis crónica, tumor de los islotes del páncreas, neoplasias quísticas).
Tumores mayores a 2 cm de diámetro,
Tumores en el cuerpo y cola de páncreas
Tumores conectados al conducto pancreático.
El porcentaje de conversión de la pancreatectomía distal laparoscópica es de un 12% Las causas de conversión son: anatomía dificultosa, tiempo operatorio prolongado, hemorragia y falla en la localización tumoral.
El tiempo operatorio va de 104 a 395 min, la pérdida de sangre va desde no medible hasta 566 ml, la estadía hospitalaria va de 5 a 34 días.
Complicaciones son: fistulas pancreáticas (12%), sangrado, infarto esplénico, abscesos e infección.
La mortalidad publicada es menor al 1%.25
CONCLUSIÓN
La pancreatectomía con conservación esplénica es hasta ahora la mejor cirugía para los tumores de cuerpo y cola de páncreas. La conservación esplénica, mediante cualquiera de las 2 técnicas, debe hacerse sólo cuando está indicada, con el fin de conseguir el mejor resultado para el paciente, debido a que su resección se asocia a morbimortalidad.
Si es necesario realizar la esplenectomía es importante someter al paciente a la profilaxis contra las infecciones correspondiente y hacer un seguimiento adecuado para realizar un diagnóstico temprano de hipoesplenismo.
Faltan estudios prospectivos randomizados para poder evaluar mejor los resultados de las técnicas quirúrgicas.
La pancreatectomía distal laparoscópica con conservación esplénica es una técnica de reciente comienzo, que hasta ahora ha presentado buenos resultados.
BIBLIOGRAFÍA
1. Lillemoe KD, Kaushal S, Cameron JL, Sohn TA, Pitt HA, Yeo CJ. Distal Pancreatectomy: Indications and Outcomes in 235 Patients. Ann. Surg. 1999; 229: 693-700
2. Carre' re N, Abid S, Henri C, Bloom E, Prade' re B. Spleen-preserving Distal Pancreatectomy with Excision of Splenic Artery and Vein: A Case-matched Comparison with Conventional Distal Pancreatectomy with Splenectomy. World J Surg 2007; 31: 375-82.
3. Salcuni PF, Foggi E, Zola C, Pellegrino F. Surgical treatment of cancer of the pancreas. Minerva Chir. 1979; 34: 165-78.
4. Fernandez-del Castillo C, Rattner DW, AL Standards for pancreatic resection in the 1990s. Arch Surg. 1995; 130: 295-9
5. Hsieh CH, Yeh CN, Chen MF. Spleen-preserving Distal Pancreatectomy without Division of Splenic Artery and Vein as a Procedure for Benign Distal Pancreatic Lesion. Chang Gung Med J. 2002; 25: 23-8.
6. Bisharat N, Omari H, Lavi I, Raz R. Risk of infection and death among post-splenectomy patients. J Infect. 2001; 43: 182-6.
7. Richardson DQ, Scott-Conner CE. Distal pancreatectomy with and without splenectomy. A comparative study. Am Surg. 1989; 55: 21-5.
8. Shoup M, Brennan MF, McWhite K, et al. The value of splenic preservation with distal pancreatectomy. Arch Surg 2002; 137: 164-8.
9. Koukoutsis I, Tamijmarane A, Bellagamba R, Bramhall S, Buckels J, Mirza D. The impact of splenectomy on outcomes after distal and total pancreatectomy. World Journal of Surgical Oncology 2007; 5: 61.
10. Benoist S, Dugue L, Sauvanet A, et al. Is there a role of preservation of the spleen in distal pancreatectomy? J Am Coll Surg 1999; 188: 255-60.
11. Billiar TR, West MA, Hyland BJ, et al. Splenectomy alters Kupffer cell response to endotoxin. Arch Surg 1988; 123: 327-32.
12. Wolf HM, Eibl MM, Georgi E, Samstag A, Spatz M, Uranus S, Passl R. Long-term decrease of CD4 + CD45RA+ T cells and impaired primary immune response after post-traumatic splenectomy. Br J Haematol 1999; 107: 55-68.
13. Warshaw AL. Conservation of the spleen with distal pancreatectomy. Arch Surg 1988; 123: 550-3.
14. Aldridge MC, Williamson RC. Distal pancreatectomy with and without splenectomy. Br J Surg 1991; 78: 976-9.
15. Melles DC, de Marie S. Prevention of infections in hyposplenic and asplenic patients: an update. Neth J Med. 2004; 62: 45-52.
16. Waghorn DJ. Overwhelming infection in asplenic patients: current best practice preventive measures are not being followed. J. Clin. Pathol. 2001; 54: 214-8.
17. Brigden ML Detection, education and management of the asplenic or hyposplenic patient. Am Fam Physician. 2001; 63: 499-506.
18. Working Party of the British Committee for Standards in Haematology Clinical Haematology Task Force. Guidelines for the prevention and treatment of infection in patients with an absent or dysfunctional spleen. BMJ 1996; 312: 430-4.
19. Beytout J, Tournilhac O, Laurichesse H. Asplenia and hyposplenism. Presse Med. 2003; 32: S5-9.
20. Williams DN, Kaur B. Postsplenectomy care. Strategies to decrease the risk of infection. Postgrad Med. 1996; 100: 195-8.
21. Prevention of pneumococcal disease: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm. Rep 1997; 46: 1-24.
22. Gagner M, Pomp A. Laparoscopic pancreatic resection:is it worthwhile? J Gastrointest Surg. 1997; 1: 20-6.
23. Mabrut JY, Fernandez-Cruz L, Azagra JS, Bassi C, Delvaux G, Weerts J, Fabre JM, Boulez J, Baulieux J, Peix JL, Gigot JF. Laparoscopic pancreatic resection: results of a multicenter European study of 127 patients. Surgery. 2005; 137: 597-605.
24. Tagaya N, Kasama K, Suzuki N, Taketsuka S, Horie K, Furihata M, Kubota K. Laparoscopic resection of the pancreas and review of the literature. Surg Endosc. 2003; 17: 201-6.
25. Aluka KJ, Long C, Rickford MS, Turner PL, McKenna SJ, Fullum TM. Laparoscopic distal pancreatectomy with splenic preservation for serous cystadenoma: a case report and literature review. Surg Innov. 2006; 13: 94-101.