Cuad. Cir. 2008; 22: 36-42
DOI: 10.4206/cuad.cir.2008.v22n1-06
CASO CLÍNICO
Interrupción percutánea de vena cava inferior
Rocío Sánchez C 1, Alejandro Murúa A 2, Carlos Fonfach Z 2, Cristián Jara D 3, Sebastián Soto G 4
1
Médico General.
2 Residente Cirugía. Instituto de Cirugía.
Universidad Austral de Chile.
3 Residente de Cirugía. Universidad de Valparaíso.
4 Cirujano Vascular. Hospital Regional de
Punta Arenas.
Correspondencia a: Dr. Sebastián Soto G. ssoto1@puc.cl.
RESUMEN
El tromboembolismo pulmonar (TEP) representa una causa frecuente de muerte en pacientes hospitalizados, siendo su principal causa la trombosis venosa profunda (TVP) de las extremidades inferiores, cuya medida de profilaxis es, entre otras, el uso de Heparina. Ocasionalmente se debe recurrir a medidas invasivas como lo es el control de la vena cava inferior.
Este artículo presenta un caso de interrupción percutánea de vena cava inferior. Se pretende actualizar la información respecto al uso de los filtros y enfatizar la tendencia actual a ser un procedimiento en expansión. Los diseńos han ido evolucionando y los beneficios permiten demostrar que el filtro de vena cava (FVC) es una opción terapéutica en pacientes seleccionados.
Palabras claves: Interrupción de la vena cava inferior; Filtro vena cava; Trombosis Venosa Profunda.
Key words: Inferior Vena Cava Interruption; Vena Cava Filter; Deep Vein Thrombosis.
CASO CLÍNICO
Paciente de 68 ańos, sexo masculino, procedente de Valdivia, con antecedentes de Cáncer de Próstata en remisión completa, sometido a prostatectomía radical y radioterapia el ańo 2004. Ingresa al subdepartamento de Urología por cuadro de 4 meses de evolución, caracterizado por incontinencia urinaria y hematuria progresiva, con compromiso hemodinámico al momento de la consulta, por lo que requiere múltiples transfusiones sanguíneas desde su ingreso. Inicialmente se sospecha cuadro de cistitis actínica, que fue descartado por estudio urológico con Tomografía axial computada (Uro TAC), la cual evidenció gran tumor vesical con probable invasión colónica. Es evaluado por coloproctólogo, quien descarta origen colónico del tumor primario.
Durante su hospitalización, cursa con edema de la extremidad inferior izquierda, evaluado por Cirugía Vascular se realiza Ecografía Doppler que evidencia trombosis venosa profunda que compromete femoral superficial distal, poplitea y venas distales de pierna izquierda.
Se sugiere interrupción de vena cava, dada la contraindicación de anticoagulación por hematuria masiva y necesidad de cirugía urológica urgente.
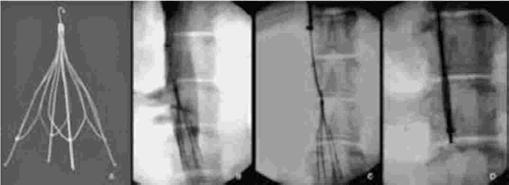
Previo a ligadura bilateral de las arterias hipogástricas, Cistectomía y Ureterostomía derecha se instala filtro de vena cava, Ć vena tech LP 7 F, Braun por vía percutánea femoral derecha, con técnica Seldinger y bajo visión radioscópica, desplegándose a nivel de L2 – L3.
El paciente evolucionó favorablemente, siendo dado de alta con controles en cirugía, urología y cuidados paliativos.
DISCUSIÓN
El TEP sigue constituyendo una de las principales causas de mortalidad intrahospitalaria, a pesar de los avances terapéuticos y la universalización de la profilaxis para la TVP. La incidencia de la enfermedad tromboembólica venosa (ETV) y su elevada morbimortalidad no ha variado durante las últimas décadas.
En los Estados Unidos son reportados más de 600,000 casos anuales con una mortalidad del 30% para el TEP masivo y de los que sobreviven al evento inicial, el 25% fallecerá por TEP recurrente1-2.
Los pacientes con historia de TVP tienen más de un 30% de recurrencia en los 3 ańos siguientes y casi 50% de probabilidades de haber tenido algún evento previo, inclusive de forma asintomática2-3.
En los pacientes con TVP y/o TEP, la terapia anticoagulante es la piedra angular del tratamiento1-33.
Si consideramos que el TEP se produce en el 95% de los casos por TVP de los miembros inferiores, de los cuales el 50% son asintomáticos, ante la contraindicación o inefectividad del tratamiento anticoagulante oral (TACO) se considera oportuno la interrupción quirúrgica de la vena cava inferior5.
En Chile se inició la experiencia con estos dispositivos en 1983, momento desde el cual se han publicado los resultados obtenidos con este procedimiento2,6,7.
HISTORIA
Al realizar una revisión histórica, en el ańo 1784 John Hunter practicó la primera ligadura de la vena femoral por tromboflebitis supurativa. Desde entonces han pasado 220 ańos, en los cuales se han realizado muchos cambios en las técnicas de interrupción de la vena cava, desde la ligadura hasta el empleo actual de filtros definitivos, temporales y/o recuperables14.
Hoy en día, los dispositivos intraluminales colocados con técnicas percutáneas, han pasado a ser el procedimiento de elección, debido a que se realizan bajo anestesia local con mínima morbimortalidad15.
En la década de los 60 Eichelter y Schenk16 iniciaron la era de la interrupción endoluminal de la vena cava. Posteriormente, Mobin-Uddin17 introdujo su “paraguas” para la interrupción endovascular de la cava, sin embargo esta presentó una alta morbimortalidad, asociada a migración y embolización.
En 1972, el doctor Lazar J. Greenfield y Garman Kimmel18, diseńaron un filtro cónico de acero inoxidable para la interrupción endovascular de la vena cava inferior. Mejoras posteriores en las décadas de los 80 y 90 lo hicieron aún más seguro permitiendo su instalación vía percútanea19.
FILTROS
De acuerdo al avance que fue presentando el procedimiento en sí, tanto en la técnica de introducción, como en el diseńo y propiedades de los filtros, se les fue exigiendo características y atributos cada vez más específicos, destacando unos sobre otros.
A continuación se detallan los atributos de un filtro ideal20:
1.
No trombogénico, biocompatible, mantenimiento de sus características
en el tiempo. |
TIPOS DE FILTROS
De acuerdo a los atributos antes mencionados y al propósito que se persigue con la instalación de un filtro, éstos pueden ser divididos en tres grandes grupos: definitivos, temporales y recuperables.
1.- Definitivos
La mayoría de las publicaciones bibliográficas hasta el momento, hacen referencia a los filtros definitivos. Estos se liberan y permanecen de por vida en su lugar de ubicación en la vena cava, esto, producto de que no existen riesgos demostrados de permanecer in situ a largo plazo v/s los ampliamente demostrados de retiro posterior a las 3 semanas que incluyen la ruptura de la vena cava.
Debido al avance tecnológico y a la competitividad comercial ha surgido una gran variedad de dispositivos tales como:
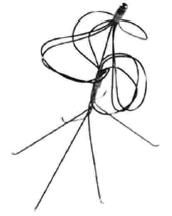
a) Nido de pájaro (Bird nest) (Fig.1), desarrollado en 1982 y aprobado por la food and drug administration (FDA), fabricado en acero inoxidable Cook. Tiene su principal indicación en megacavas (24-48 mm). Se describe de compleja colocación y está asociado a una menor permeabilidad de vena cava inferior (VCI)21-24.
 |
FIGURA
1: Bird nest. |
b) Simon nitinol (Fig. 2), desarrollado en 1988 y aprobado por la FDA en 1990. Tiene como característica el no ser ferromagnético21-24.
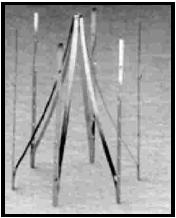 |
FIGURA
2: Simon nitinol. |
c) Venatech – LGM– (Fig. 3), (1986, FDA: 1989). de Braun®. Puede ser instalado por vía yugular, femoral o subclavia, no ferromagnético. Se reporta una permeabilidad de la VCI de 78-92%21-23.
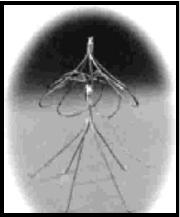 |
FIGURA
3: Venatech – LGM. |
d) Greenfield-Kimroy (Fig. 4), fabricado en Nitinol (1991), es de mayor fuerza radial y más liviano, tiene una permeabilidad de VCI a 30 días de 100%. No ferromagnético, se reporta una trombosis del acceso en sólo un 8.7% y presenta una baja tasa de migración y TEP recurrente (aprox. 3.3%)22-24.
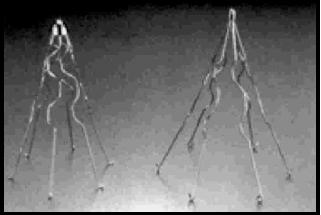 |
| FIGURA 4: Greenfield-Kimroy. |
2.- Temporales
Los filtros temporales quedan conectados a través de un catéter o guía con el exterior y permanecen en la vena cava durante un período breve inferior a 15 días, siendo necesario extraerlos.
La idea de los dispositivos temporales es muy atractiva, sobre todo para las indicaciones de profilaxis de corta duración, pero no han logrado una buena aceptación ni un uso masivo debido principalmente a la rápida endotelización que se produce, en general, a los 15 días (aunque en algunas publicaciones se habla de hasta 130). La endotelización precoz podría producir: lesión en la VCI al remover el dispositivo o una trombosis extensa de la misma debido al dańo endotelial y TEP secundario.
Además este tipo de dispositivos requieren de un sistema complejo para su retiro y cierto grado de habilidad del operador.
Algunos tipos de filtros temporales son21-23:
a)
Thery, metálico.
b) Antheor. Silastic, debido a una alta tasa de migración fue retirado
del mercado.
c)
Tempofilter I y II, de Braun se instala por vía yugular. Tiene un
dispositivo para implante subcutáneo y recuperación en 20 días.
3.- Recuperables
Tienen una configuración similar a los filtros definitivos y en caso de necesidad pueden actuar como tales; la diferencia esá en que poseen un pequeńo gancho que permite de forma muy fácil recapturarlos y extraerlos.
Para evitar que estos filtros recuperables migren, poseen unos pequeńos ganchos de sujeción que penetran en la pared de la vena cava25. Esta agresión producida en el endotelio, condiciona una reacción fibrosa que tiende a englobar las patas del filtro en la propia pared de la vena, lo que dificulta o impide su extracción, planteándonos la siguiente interrogante: żQué período de tiempo sería necesario para que se produzca esta reacción fibrosa?
En este sentido la casa comercial del filtro Gunther-Tulip, recomienda su retirada antes de los 12 días. Diversos autores han realizado estudios en modelos animales que muestran que después de los 14 días se produce esta importante reacción fibrosa alrededor de las patas del filtro, que impide su extracción25-26. No obstante, con este filtro y con otros dos prototipos se han comunicado períodos más largos de extracción sin dificultad, que oscilan entre 21 y 134 días24-26, sin embargo la gran mayora de éstos se usan como dispositivos definitivos.
Algunos tipos de filtros recuperables:
a) Opt Ease, fabricado por Cordis® de nitinol, de introducción percutánea y de bajo perfil: 6 french, no ferromagnético.
b) Gunther-Tulip (Figura 5). Permanente o removible a los 14 días, es de bajo perfil: 8.5 french. Puede ser instalado por vía yugular y femoral. No ferromagnético.
 |
| FIGURA 5: Gunther-Tulip. |
c) Filtro de Bard (Bard Peripheral Vascular). (Figura 6).
 |
FIGURA
6: Filtro de Bard. |
INDICACIONES
Es necesario destacar que no existe un consenso respecto a las indicaciones de instalación de un filtro de vena cava inferior, esto debido a la escasez de trabajos randomizados y controlados sobre el tema.
Sin embargo, la literatura actual provee información suficiente que avala la técnica y seguridad de la interrupción de la vena cava.
Si bien un filtro en la vena cava inferior ofrece protección del embolismo pulmonar a partir de una TVP de las extremidades inferiores o ileopelviana, evidentemente expone al paciente a una baja, pero cierta incidencia de complicaciones asociadas al filtro. Por lo tanto, el implante de un filtro debe responder a una indicación clara.
Existen indicaciones ampliamente aceptadas o absolutas, éstas se refieren principalmente a aquellos pacientes que no pueden ser anticoagulados, cuando el tratamiento anticoagulante oral haya fracasado en prevenir recurrencia de embolismo o la imposibilidad de tolerar un evento embólico subsiguiente7,27-30,32. Los pacientes en los que está contraindicada la anticoagulación o con ciertas complicaciones también deben manejarse con la inserción del filtro exclusivamente.
Aquellos pacientes considerados dentro de las indicaciones relativas, son aquellos que potencialmente podrían presentar una enfermedad trombo embólica31. La decisión para instalar un filtro de vena cava inferior requiere de un adecuado juicio clínico-quirúrgico; y tanto ésta como la colocación del filtro deben ser realizadas idealmente por un cirujano vascular.
Indicaciones Absolutas7-10:
1. Pacientes con evidencias de embolismo pulmonar o trombosis venosa de la cava, iliaca, femoro-poplítea y uno o más de los siguientes:
a. Contraindicación absoluta para la anticoagulación.
-
Accidente Cerebrovascular hemorrágico.
- Hemorragia digestiva.
- Hemorragia retroperitoneal.
- Hemoptisis masiva.
- Metástasis Cerebral.
-
Accidente Cerebrovascular masivo.
- Trauma del Sistema Nervioso Central.
- Trombocitopenia < 50.000.
b. Complicación hemorrágica de la anticoagulación.
c. Falla de una adecuada anticoagulación:
- En los que se objetiva TEP recurrente.
- Imposibilidad de lograr AC adecuada
2. TEP masivo o en pacientes con trombos amenazantes en extremidades inferiores o sector iliocavo.
3. Enfermos con TVP Iliofemoral con coágulo flotante, ya que en éstos, a pesar de AC, el riesgo descrito de TEP es hasta de 26% (TVP unilateral) y de 42.8% (bilateral).
4. Enfermedad Cardiopulmonar severa y TVP (ej. Corpulmonar con hipertensión pulmonar).
5. Pobre adherencia a la terapia anticoagulante.
Indicaciones Relativas7-10
1. Profilaxis de TEP en pacientes con trauma.
2. Tratamiento del TEP en pacientes con cáncer.
3. Pre o post embolectomía pulmonar.
4. Profilaxis de TEP en pacientes ortopédicos de alto riesgo.
5. Prevención de TEP en pacientes con Enfermedad Pulmonar Obstructiva Crónica y TVP.
6. Prevención de TEP en pacientes con escasa reserva Cardiopulmonar y TVP.
7. Tratamiento de tromboembolismo venoso en embarazadas.
8. Tratamiento de tromboembolismo venoso en pacientes trasplantados de órganos.
9. Contraindicación relativa de la anticoagulación.
10. Embolismo séptico persistente a pesar de tratamiento correcto.
COMPLICACIONES
Las complicaciones de los filtros de vena cava inferior son infrecuentes. Las más importantes son la migración del dispositivo, la trombosis en el sitio de punción y la trombosis de la vena cava. La recurrencia de TEP es cercana al 3% y se presenta por lo general durante los primeros meses posteriores al implante del dispositivo10-13.
Las complicaciones pueden producirse en tres situaciones:
1. Durante la inserción:
a. Deformación del filtro.
b. Fractura del filtro.
c. Apertura incorrecta.
d. Implante incorrecto.
e. Embolia proximal grave, por menor tamańo que
la VCI.
2. En el sitio de punción
a. Hematoma.
b. Fístulas arteriovenosas.
c. Neumotórax.
3. Inherentes al filtro
a. Migración.
b. Angulación.
c. Oclusión completa de la vena cava inferior.
d. Lesión endotelial y hemorragia.
e. Infección.
f. Estenosis de la VCI.
CONTRAINDICACIONES
Las únicas contraindicaciones absolutas de inserción de filtro de vena cava inferior son: la incapacidad de acceso a vena cava inferior, coagulopatía severa (insuficiencia hepática, falla multisistémica) o pacientes con bacteremias o infecciones no tratadas.
TÉCNICA QUIRÚRGICA
La técnica específica va a depender del modelo del dispositivo y del cirujano, sin embargo, casi todos los sistemas comparten características generales y suele ser, habitualmente, una técnica sencilla, variando muy poco de dispositivo a dispositivo. Idealmente se prefiere una sala con fluoroscopía para asegurar su adecuado posicionamiento12.
Independiente de las posibles variaciones entre dispositivos, la punción venosa con técnica de Seldinger por va subclavia, yugular o femoral suele ser indistinta y vía a depender de la experticia y preferencia del operador. Posterior al despliegue del dispositivo es importante corroborar su colocación por debajo de las venas renales (independientemente de la vía de implante) pues existe la posibilidad de complicaciones trombóticas que resultan en deterioro catastrófico de la función renal.
El filtro puede instalarse por sobre las venas renales en algunos casos especiales:
1. Pacientes con trombos suprarrenales
y falla de la anticoagulación.
2. Trombosis de las venas renales como fuente embolígena.
3. Mujeres embarazadas o que anticipan embarazo.
4. Trombos por encima de un filtro existente.
5. Embolismo pulmonar luego de trombosis venosa gonadal.
6. Variante anatómica: vena cava inferior duplicada,
baja inserción de venas renales.
En la literatura se describe una mayor incidencia de TEP recurrente y trombosis de la VCI, probablemente debida a dos factores: mayor tiempo de seguimiento en las series y una población en donde la asociación con cáncer es mayor. Existen además implantes en la vena cava superior, pero corresponden a reporte de casos aislados3.
CONCLUSIONES
El gold standard en el tratamiento de la TVP y/o TEP, continúa siendo el tratamiento anticoagulante
Las únicas indicaciones formales para la interrupción de la vena cava son las categóricas:
1. contraindicación o complicaciones de
la anticoagulación.
2. tromboembolismo pulmonar repetitivo a pesar de anticoagulantes.
3. postromboembolectomía pulmonar y/o Trombolisis.
En relación a las indicaciones relativas, la decisión requiere de un adecuado juicio clínico-quirúrgico; y el procedimiento debe ser realizado idealmente por un cirujano vascular.
El uso de filtros de VCI es eficaz y seguro en prevenir el TEP masivo, complicaciones a largo plazo son infrecuentes, la incidencia alejada de TVP se compara favorablemente con la reportada en pacientes con TVP sin filtro.
REFERENCIAS
1. Wood KE. Major Pulmonary Embolism review of a pathophysiologic approach to the golden hour of hemodynamically significant pulmonary embolism. Chest 2002; 121: 3, 877-905.
2. Arriagada J, Ivette, Mertens M, Renato, Valdes E, Francisco et al. Interrupción de la vena cava inferior mediante filtros de inserción percutánea: Indicaciones y resultados en 287 pacientes. Rev. Méd. Chile, mar. 2007, vol.135, no.3, p. 351-8.
3. Goldhaber SZ. Pulmonary embolism. The New England Journal of Medicine 1998; 339(2): 93-104.
4. Streiff MB. Vena caval filters: a comprehensive review. Blood 2000; 95: 3669-77.
5. Greenfield LJ, Proctor MC. Current indications for caval interruption: Should they be liberalized in view of improving technology. Semin Vasc Surg 1996; 9: 50-8.
6. Velásquez A, Valdés F, Krämer A, Mertens R. Interrupción transyugular de vena cava inferior. Experiencia con el filtro de Greenfield en 24 pacientes. Rev Chil Cardiología 1990; 9: 281.
7. Mertens R, Valdés F, Krämer A, Vergara J. Interrupción vena cava inferior mediante filtros. Indicaciones y resultados en 111 pacientes. Rev Méd Chile 1998; 126: 65-660.
8. Streiff MB. Vena Caval Filters: A Comprehensive Review. Blood 2000; 95: 3669-77.
9. Tapson VF and Witty LA. Massive Pulmonary Embolism. Clinics in Chest Medicine. 1995; 329-339.
10. Paredero MV, Gómez B. Filtros de vena cava. Indicaciones actuales. Archivos de Cirugía Vascular 1999, VIII(4): 213-6.
11. Greenfield LJ. Suprarenal filter placement. J Vasc Surg 1998; 28: 432.
12. Dorfman GS. Percutaneous inferior vena cava filters. Radiology 1990; 174: 987-992.
13. Whitehill TA. Caval interruption methods: Comparison of options. Semin Vasc Surg 1996; 9: 59-69.
14. Adams JT, DeWeese JA. Partial interruption of the inferior vein cava with a new plastic clip. Surg Gynecol Obstet 1966; Nov: 1087-8.
15. Eichelter P, Schenk W. Prophylaxis of pulmonary embolism. A new experimental approach with initial results. Arch Surg 1968; 97: 348.
16. Mobin-Uddin K, Smith PE, Martinez LD. A vein cava filter for the prevention of pulmonary embolism. Surg Forum 1967; 18: 209-11.
17. Greenfield LJ, McCurdy Jr, Brown P P, Elkins RC. A new intracaval filter permitting continued flow and resolution of emboli. Surgery 1973; 73: 599-606.
18. Rojas G, Enriquez E, Garmilla J, Gerson R, Varela M. Un nuevo filtro de Greenfield de titanio para la interrupción endovascular percutánea de la vena cava inferior. An Med Asoc Med Hosp ABC 1992; 37: 75-78.
19. Kinney TB. Update on inferior vena cava filter. J Vasc Interv Radiol. 2003; 14: 425-40.
20. Hicks MF and Dorfman GS. Vena Caval Filters. Vascular Diseases–Surgical & interventional Therapy. Vol 2. Churchill Livingstone Inc. 1994. Pag. 1017-1044.
21. Greenfield LJ and Cho KJ. The Titanium Greenfield Vena Cava Filter and 12 French Introducer System – Concept and Technique. Medi-tech Education Center. 1990, Boston Scientific Corporation.
22. Asch MR. Initial experience in humans with a new retrievable inferior vena cava filter. Radiology 2002; 225: 835-44.
23. Neuerburg J, Gunther R, Rassmussen E, Vorwerk D, Tonn K, Handt S, et al. New retrievable percutaneous vena cava filter: experimental in vitro and in vivo evolution. Cardiovasc Intervent Radiol 1993; 16: 224-9.
24. De Gregorio MA, Gimeno MJ, Tobio R, Lostale F, Mainar A, Beltrn JM, et al. Animal experience in the Gunther Tulip retrievable inferior vena cava filter. Cardiovasc Intervent Radiol 2001; 24: 413-7.
25. Ansell J. Vena cava filter: Do we know all that we need to know?. Circulation 2005; 112: 298-9.
26. Wood KE. Major pulmonary embolism. Chest 2002; 121: 877-905.
27. Decousus H, Leizorovicz A, Parent F, Page Y, Tardy B, Girard P. A clinical trial of vena cava filter in the prevention of pulmonary embolism in patients with prximal deep-vein thrombosis. N Engl J Med 1998; 338: 409-15.
28. Torbiscki A. guidelines on diagnosis and management of acute pulmonary embolism. Eur Heart J 2000; 21: 1301-36.
29. Grassi J C. Quality improvement guidelines for percutaneuos permanent inferior vena cava filter placement for the prevention of pulmonary embolism. J Vasc Interv Radiol 2003; 14: S271-5.
30. Saenz de la Calzada. Guía practica clínica de la Sociedad Espańola de Cardiología en tromboembolismo e hipertensión pulmonar. Rev Esp Cardiología 2001; 54: 194-210
31. Greenfield LJ, Rutherford RB. Participants in The Vena Cava Filters Consensus Conference: Recommended reporting standards for vena caval filter placement and patient follow-up. J Vasc Interv Radiol 1999; 10: 1013-9.
32. Ariza MG, Sotomayor PA, Aguiran EA y col. Estratégia terapéutica no farmacológica; filtros de vena cava inferior en el tratamiento de la enfermedad tromboembólica venosa. Arch Bronconeumol (Universidad de Zaragoza, Espańa) 1995; 31: 347-8.
33. Becher DM, Philbrick JT, Selby JB. Inferior vena caval filters, indications, safety and effectiveness. Arch Intern Med 1992; 152: 1985-94.