Cuad.
Cir. 2010; 24: 11-16
DOI: 10.4206/cuad.cir.2010.v24n1-02
CASOS CLÍNICOS
Tumor sólido-pseudopapilar del páncreas. Presentación de 3 casos clínicos
Drs. Francisco Venturelli M 1, Cristian Carrasco L 3, Maeva del Pozo L 2,3, Carlos Cárcamo I 1,4, Marcela Cárcamo Ibaceta 5, Aliro Venturelli Leonelli 1,4.
1
Instituto de Cirugía. Facultad de Medicina. Universidad Austral de Chile.
2
Instituto de Histología y Patología. Facultad de Medicina. Universidad Austral
de Chile.
3
Subdepartamento de Anatomía Patológica. Hospital Clínico Regional de Valdivia.
4 Subdepartamento
de Cirugía. Hospital Clínico Regional de Valdivia.
5 Magíster
en Epidemiología.
Correspondencia a: Dr. Francisco Venturelli, fcoventurelli@gmail.com.
RESUMEN
El tumor sólido-pseudopapilar del páncreas (TSPP) es una neoplasia infrecuente (1-2% de los tumores exocrinos), que afecta predominantemente a mujeres jóvenes, con bajo potencial de malignidad (15% da metástasis). Su diagnóstico preoperatorio es difícil, principalmente debido a que a la imagenología no tiene una característica que la pueda diferenciar de otros quistes pancreáticos, por lo que generalmente es un hallazgo histopatológico. El tratamiento quirúrgico presenta buena sobrevida, incluso en presencia de metástasis. Presentamos 3 casos con cuadro clínico, imagenología, tratamiento e histopatología, con el fin de aportar más información, sobre esta infrecuente patología.
Palabras claves: tumor sólido-pseudopapilar, tumores quísticos, páncreas.
Key words: solid pseudopapilar neoplasm, cystic neoplasm, pancreas.
INTRODUCCIÓN
El tumor sólido pseudopapilar del páncreas (TSPP) es una neoplasia del páncreas exocrino, de baja incidencia, con bajo potencial maligno, que afecta predominantemente a mujeres jóvenes1.
Chile es uno de los países con mayor incidencia de tumores pancreáticos2, ocupando el TSPP el 1-2% de ellos3. A pesar de su baja incidencia el 75% de los casos han sido publicados en la última década, lo que podría estar indicando, que cada vez más nos veremos enfrentados a esta incierta patología4. A pesar que su incidencia pareciera ir en aumento, hasta el año 2005 sólo había 500 casos publicados1, lo que ha imposibilitado un consenso de manejo, de allí la importancia de dar a conocer el diagnóstico y tratamiento de cada caso.
El objetivo de este artículo es mostrar nuestra experiencia en 3 casos clínicos ocurridos en un período menor a un año y revisar el estado del arte en relación a esta patología.
CASO CLÍNICO 1
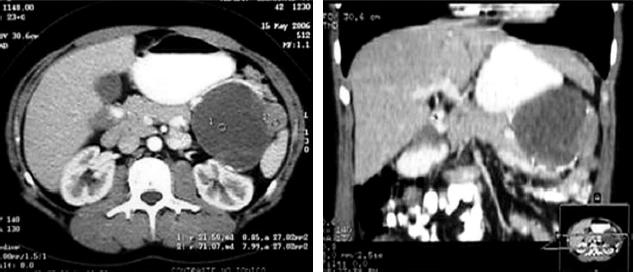
Mujer de 42 años, consulta por cuadro de 3 meses de evolución de dolor hipogástrico leve intermitente asociado a distensión abdominal, flatulencia y dispepsia. Ecografía abdominal informa masa en hipocondrio izquierdo, en relación a la cola del páncreas, separada del riñón y bazo. Estudio serológico resulta negativo para hidatidosis. La tomografía helicoidal computada de abdomen evidencia la cola del páncreas desplazada hacia anterior, comprimiendo la curvatura mayor gástrica, cara medial del bazo y cara anterior del riñón izquierdo, en relación a una formación redondeada de aspecto quístico de aproximadamente 8 cm de diámetro, tabicada, de paredes de moderado grosor con áreas cálcicas en su interior, que se magnifica escasamente con el medio de contraste (Figura 1). Se plantea el diagnóstico diferencial entre pseudoquiste y cistoadenoma macroquístico pancreático.
Se practica tumorectomía más esplenectomía, por adherencia al hilio esplénico. Evoluciona satisfactoriamente siendo dada de alta al tercer día postoperatorio. La biopsia de la pieza quirúrgica informa presencia de un ovoide quístico necrótico de 8 cm con pared de espesor variable, con áreas sólidas y extensa necrosis hemorrágica. El estudio histopatológico diagnóstica un tumor sólido-pseudopapilar del páncreas, con márgenes quirúrgicos libres (Figura 3, 4, Tabla 1).
CASO CLÍNICO 2
Mujer de 41 años que consulta por cuadro agudo de dolor tipo cólico, en hipocondrio derecho, asociado a vómitos. Ecografía abdominal muestra imagen compatible con colecistitis aguda litiásica, además de una imagen de 4 x 3 cm en relación al páncreas, de aspecto nodular, ovoidea y bien definida. Se realiza tomografía helicoidal computada de abdomen que además de informar una vesícula de características inflamatorias, describe la presencia de tumor de 4,8 x 5 cm a nivel del cuerpo del páncreas, que desplaza la cara posterior del estómago, hipodensa, de contornos bien definidos y regulares, que se contrasta parcialmente con el medio de contraste. Antígeno carcinoembrionario 2,3 U/ml. Se practica pancreatectomía corporocaudal, con preservación esplénica, más colecistectomía clásica (Figura 2). Se da de alta al 5 día postoperatorio sin complicaciones. Biopsia informa presencia de un tumor de 6,5 cm de diámetro mayor, sólido, sin necrosis, con histopatología concordante con TSPP; márgenes quirúrgicos libres y resección de un linfonodo sin compromiso metastásico (Figura 3, 4, Tabla 1).
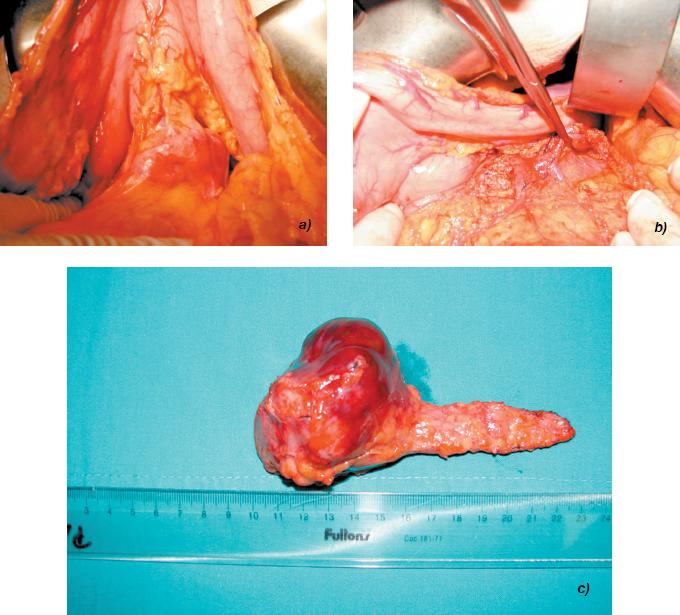 |
FIGURA
2. a) Tumor quístico in situ, b) Lecho quirúrgico (Pinza en vena
esplénica), c) Pieza operatoria (sin esplenectomía). |
CASO CLÍNICO 3
Mujer de 22 años con antecedentes de ovario poliquístico y usuaria de anticonceptivos orales. Presenta cuadro de dolor epigástrico postprandial, que evoluciona a todo el hemiabdomen izquierdo, irradiándose a dorso, hemitórax y brazo ipsilateral, de carácter opresivo y asociado a dispepsia. Ecografía abdominal informa masa de 9,8 x 8,1 cm anteromedial al polo superior del riñón izquierdo en relación a la cola del páncreas, heterogénea, redondeada, con contornos lisos y precisos, y con múltiples zonas de distinta densidad en su interior. Tomografía helicoidal computada de abdomen evidencia masa de 11 x 10 cm en la cola del páncreas, redondeada, de contornos definidos, aspecto capsular, estructura homogénea, con áreas predominantemente hipodensas entremezcladas con zonas de mayor densidad que se impregnan con el medio de contraste; no invade estructuras vecinas; resto del páncreas y bazo de características conservadas; planteando como primera posibilidad una neoplasia epitelial sólida y papilar. Se practica pancreatectomía distal con esplenectomía y resección del ángulo esplénico del colon por compromiso del pedículo esplénico y mesocolon. Biopsia informa presencia de tumor de 12 cm de diámetro mayor, que da salida a material necrohemorrágico, con histología compatible con TSPP; márgenes quirúrgicos negativos; se resecaron 3 linfonodos sin compromiso metastásico (Figura 3, 4, Tabla 1).
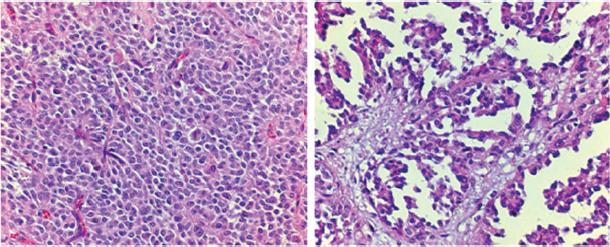 |
| FIGURA 3. Histología H-E. Se visualiza patrón sólido y pseudopapilar. |
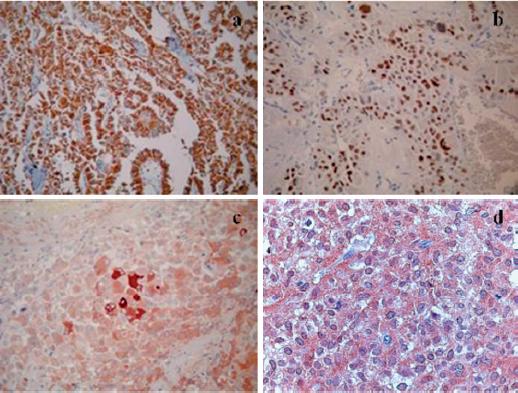 |
FIGURA
4. Marcadores con técnica de inmunohistoquímica. a: Vimentina (+), b: Progesterona (+), c: alfa-1 antitripsina (+), d: Enolasa neuroespecífica (+). |
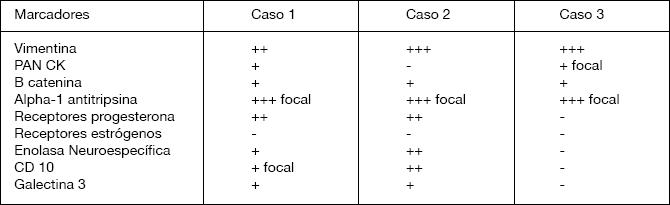 |
+:
Leve, ++: moderada, +++: intenso, -: negativo. La tinción para Beta catenina y receptores de progesterona fue nuclear, la tinción para Vimentina, Citoqueratinas, Alfa-1 Antitripsina, Enolasa Neuroespecífica, Galectina 3 fue citoplasmática. La tinción para CD 10 fue de membrana. Focal en células o grupos aislados que no representan más del 10%. En los casos no especificados la tinción fue difusa. |
DISCUSIÓN
La OMS define al TSPP como una neoplasia epitelial exocrina de tipo borderline (neoplasia sólida-pseudopapilar) con potencial maligno (carcinoma sólido-pseudopapilar)2. La teoría más aceptada sobre su origen hace referencia a que se formaría a partir de tejido estromal ovárico ectópico (de localización pancreática) durante la embriogénesis5,6.
Su edad de presentación es en promedio, 35 años (8-67), con una relación hombre:mujer de 1:7-106,7. La localización más frecuente es la cabeza y cola pancreática. El 15% de los casos son asintomáticos6; en el resto, los síntomas provienen de la compresión de estructuras vecinas (malestar inespecífico, dolor abdominal, etc), por lo que al momento del diagnóstico, el tamaño tumoral generalmente alcanza los 7 cm7,8. Raramente producen ictericia, no infiltran la vía biliar3.
En los exámenes de laboratorio se encuentra normalidad de los valores de amilasemia y marcadores tumorales, tanto plasmáticos como del líquido quístico (CEA, CA 19-9 plasmáticos y TAG-72 y CA-15-3 del líquido quístico)9,10.
El estudio imagenológico comprende: ecografía abdominal, tomografía computada abdominal, endosonografía y resonancia nuclear magnética; las 2 primeras son las más utilizadas9. La ecografía muestra una masa sólida, sólida-quística o quística, única sin tabicaciones, con calcificaciones en su interior, rodeada de una cápsula bien definida10. La tomografía computada lo describe como una gran masa sólida, sólida-quística o quística generalmente mayor de 8 cm, capsulada, con calcificaciones internas y/o capsulares, con áreas necrohemorrágicas (hipodensas) y áreas sólidas papilares (hiperdensas) que desplazan estructuras vecinas, con vía biliar y conducto pancreático fino10,11; esta última tiene una exactitud diagnóstica de un 60%8. Debido a que con estas características es muy difícil diferenciarlo de los otros tumores quísticos del páncreas12, en más de un 50% de los casos el diagnóstico preoperatorio es incierto, planteándose como diagnósticos diferenciales los pseudoquistes y las neoplasias quísticas mucinosas (cistoadenomas, cistoadenocarcinoma)13; estas últimas también se presentan habitualmente en mujeres (84%), pero a edades más tardías (promedio 53 años), se localizan más frecuentemente en el cuerpo y cola pancreática (75%)14 y tienen marcadores tumorales del líquido quístico y plasmático elevados. En la tomografía computada están compuestas por varias cavidades (menos de 6 de más de 2 cm de diámetro cada uno), además de la presencia de septos, proyecciones papilares y calcificaciones15.
El diagnóstico preoperatorio se puede realizar mediante una punción con aguja fina del quiste, siendo característico encontrar en los TSPP una estructura pseudopapilar, acidofilia con células PAS + y gránulos citoplasmáticos resistentes a la diastasa16. El inconveniente de esta técnica es el riesgo de diseminación frente a un cistoadenocarcinoma, por lo que no está del todo recomendada10.
Macroscópicamente se caracteriza por ser una masa única, que puede estar adherida al bazo, generalmente fluctuante7 con diámetro promedio de 10,5 cm (5-19), vascularizado, encapsulado y con márgenes lobulados, bien definidos. En su interior presenta degeneración hemorrágica quística, con calcificaciones intratumorales3,13.
Histológicamente está constituido de tejido necrohemorrágico rodeado por una cápsula fibrosa, bajo la cual se reconoce tejido tumoral formado por células uniformes de citoplasma eosinófilo que alternan con células de aspecto espumoso. Estas células se disponen en un patrón sólido con necrosis, que crea la apariencia de papilas ordenadas alredededor de vasos hialinizados. La inmunohistoquímica y la inmunoquímica es (+) para vicentina, alfa antitripsina, NSE en el 90% de los casos, (+) para citoqueratina en un 70% de los casos5,8. Además puede ser (+) para la alfa antiquimiotripsina y receptores de progesterona5.
Pueden malignizarse hasta en un 15-20%7,10,17. La forma maligna se presenta más frecuentemente en hombres y por lo general presentan metástasis al momento del diagnóstico, siendo los órganos más frecuentemente afectados el hígado, vena porta y bazo6. Las metástasis ocurren en promedio a los 8,5 años del diagnóstico de la enfermedad y generalmente en pacientes mayores de 36 años8. Los criterios de malignidad histopatológicos sugeridos por la OMS son invasión perineural, invasión vascular e invasión profunda a los tejidos vecinos.
El tratamiento de las formas benignas y malignas es la resección completa tumoral, incluyendo metástasis17,18, mediante técnicas abiertas o laparoscópicas, siendo las más utilizadas la pancreatoduodenectomía abierta y pancreatectomía distal laparascópica con conservación esplénica (con o sin ligadura de vena y arteria esplénica), exceptuando los casos en que el tumor está adherido al hilio esplénico19,20,21. Dentro de las terapias paliativas está descrita la quimio-radioterapia, pero no hay un esquema universal y los resultados no son concluyentes.
El pronóstico es bueno. La sobrevida a 4 y 20 años es de 100 y 85% respectivamente. La cirugía paliativa también reporta buenos resultados con sobrevida mayor a 10 años. El control postoperatorio debe mantenerse por un largo período, ya que se han reportado recidivas hasta 20 años postcirugía22.
Como conclusión el TSPP es un tumor de diagnóstico histopatológico, que se presenta generalmente en mujeres jóvenes. Con el tratamiento quirúrgico presenta un buen pronóstico, incluso cuando está diseminado.
REFERENCIAS
1. Frantz VK. Tumors of the pancreas. En: Atlas of Tumor Pathology, Section vii. Fasc 27 and 28. Washington, DC: Armed Forces Institute of Pathology; 1959; 32-7.
2. Klöppel G, Lüttges J, Klimstra D, Hruban R, Kern S, Adler G. Tumours of the exocrine pancreas. Solid-pseudopapillary neoplasm. En: HAMILTON, Starley and AALTONEN, Lauri. Pathology & Genetics. Tumor of the digestive system. Francia, Editorial IARC. 2000; 246-8.
3. Salvia R, Festa L, Butturini G, Tonsi A, Sartori N, Biasutti C, et al. Pancreatic cystic tumors. Minerva Chir 2004; 59: 185-207.
4. Washington K. Solid-pseudopapillary tumor of the pancreas: challenges presented by an unusual pancreatic neoplasm. Ann Surg Oncol 2002; 9: 3-4.
5. Martin R, Klimstra D, Brennam M, Conlon K. Solid-pseudopapillary tumor of the pancreas: a surgical enigma?. Ann Surg Oncol 2002; 9: 35–40.
6. Papavramidis T, Papavramidis S. Solid pseudopapillary tumors of the pancreas: review of 718 patients reported in english literature. J Am Coll Surg 2005; 200: 965-72.
7. Eder F. Schulz HU, Röcken C, Lippert H. Solid-pseudopapillary tumor of the pancreatic tail. World J Gastroenterol 2005; 11: 4117-9.
8. Huang HI, Shih SC, Chang WH, Wang TE, Chen MJ, Chan YJ. Solid-pseudopapillary tumor of the pancreas: clinical experience and literature review. World J Gastroenterol 2005; 11: 1403-9.
9. Coleman KM, Doherty MC, Bigler SA. Solid-pseudopapillary tumor of the pancreas. Radiographics 2003; 23: 1644-8.
10. Zhang H, Liang TB, Wang WI, Shen Y, Ren GP, Zheng SS. Diagnosis and treatment of solid-pseudopapillary tumor of the pancreas. Hepatobiliary Pancreat Dis Int 2006; 5: 454-8.
11. Dong DJ, Zhang SZ. Solid-pseudopapillary tumor of the pancreas: CT and MRI features of 3 cases. Hepatobiliary Pancreat Dis Int 2006; 5: 300-4.
12. Sarr M, Carpenter H, Prabhakar L, Orchard T, Hughes S, Van Heerden J, et al. Clinical and pathologic correlation of 84 mucinous cystic neoplasms of the pancreas: can one reliably differentiate benign from malignant (or premalignant) neoplasms?. Ann Surg 2000; 231: 205-12.
13. Fernández JA. Tumores quísticos del páncreas: revisión de la literatura. Cir Esp 2003; 73: 297-308.
14. Box JC, Douglas HO. Management of cystic neoplasms of the pancreas. Am Surg 2000; 66: 495-501.
15. Balci C, Semelka R. Radiologic features of cystic, endocrine and other pancreatic neoplasms: Imaging of pancreatic disease. Eur J Radiol 2001; 38: 113-9.
16. Pelosi G, Iannucci A, Zamboni G, Bresaola E, Iacono C, Serio G. Solid and cystic papillary neoplasm of the pancreas: a clinico-cytopathologic and immunocytochemical study of five new cases diagnosed by fine-needle aspiration cytology and rewiew of the literature. Diagn Cytopathol 1995; 13: 233-46.
17. Mulkeen A, Yoo P, Cha A. Less common neoplasms of the pancreas. World J Gastroenterol 2006; 12: 3180-5.
18. Tipton SG, Smyrk TC, Sarr MG, Thompson GB. Malignant potential of solid pseudopapillary neoplasm of the pancreas. Br J Surg 2006; 93: 733-7.
19. Shimizu S, Tanaka M, Konomi H, Mizumoto K, Yamaguchi K. Laparoscopic pancreatic surgery: current indications and surgical results. Surg Endosc. 2004; 18:402-6.
20. Kaneko H, Takagi S, Joubara N, Yamazaki K, Kubota Y, Tsuchiya M, et al. Laparoscopy-assisted spleen-preserving distal pancreatectomy with conservation of the splenic artery and vein. J Hepato Biliary Pancreatic Surg 2004; 11: 397–401.
21. Tagaya N, Kasama K, Suzuki N, Taketsuka S, Horie K, Furihata M, et al. Laparoscopic resection of the pancreas and review of the literature. Surg Endosc 2003; 17: 201-6.
22. Frago R, Fabregat J, Jorba R, García-Borobia F, Altet J, Serrano MT. Solid pseudopapillary tumors of the pancreas: diagnosis and curative treatment. Rev Esp Enferm Dig 2006; 98: 809-19.