Cuad.
Cir. 2010; 24: 28-33
DOI: 10.4206/cuad.cir.2010.v24n1-05
TRABAJO DE ACTUALIZACIÓN
Gangrena de Fournier
Cristian Cancino B 1, Rodolfo Avendaño H 2, Carolina Poblete Andrade 3, Katia Guerra H 3
1 Residente
de Urología, Instituto de Especialidades, Facultad Medicina, Universidad Austral
de Chile
2 Cirujano
Coloproctólogo. Subdepartamento de Cirugía Adulto, Hospital Clínico Regional
Valdivia Profesor Auxiliar de Cirugía. Facultad de Medicina. Universidad Austral
de Chile.
3
Interna de Medicina, Escuela de Medicina, Universidad Austral de Chile
Correspondencia a: Dr. Rodolfo Avendaño H., rudyavenda@yahoo.com.
RESUMEN
La Gangrena de Fournier es una enfermedad infecciosa caracterizada por una fascitis necrotizante de evolución fulminante que afecta a la región perineal, genital o perianal, presentando una rápida progresión y alta letalidad, siendo la etiología identificable en un 95% de los casos. La enfermedad ha sido descrita en ambos géneros, con edad promedio de presentación de 40 años y una mayor prevalencia en hombres, con una relación 10:1. La variedad de manifestaciones clínicas dificulta el diagnóstico, el que es fundamentalmente clínico. El tratamiento debe ser oportuno y agresivo, contemplando tres pilares fundamentales: manejo hidroelectrolítico y nutricional, antiobioterapia de amplio espectro y desbridamiento quirúrgico amplio. En este artículo presentamos una revisión sistemática actualizada de la literatura acerca de esta interesante entidad patológica, con especial énfasis en la epidemiología, etiología, presentación clínica, diagnóstico y tratamiento.
Palabras claves: Gangrena de Fournier; fascitis necrotizante.
Key words: Fournier’s gangrene; necrotizing fascitis.
INTRODUCCIÓN
La Gangrena de Fournier es una enfermedad infecciosa sinérgica polimicrobiana, caracterizada por una fascitis necrotizante de la región perineal, genital o perianal, que incluso puede comprometer la pared abdominal1,2. Esta enfermedad se conoce desde la antigüedad; se sospecha que el rey Herodes de Judea la padeció asociada a diabetes mellitus, y el médico persa Avicenna la identificó en el año 877 d.C.3,4 La primera descripción formal de la enfermedad fue realizada en 1764 por Baurienne5. En 1871 Joseph Jones elaboró la primera descripción en América, sin embargo su epónimo proviene del dermatólogo y venereólogo francés Jean Alfred Fournier, quien en 1883 describió 5 casos de fascitis necrotizante de la región genitoperineal que se caracterizaba por edema escrotal doloroso de comienzo abrupto, con rápida progresión a gangrena, sin causa definida, en hombres jóvenes previamente sanos6.
A través del tiempo se han empleado diversos términos para describir esta condición clínica: Gangrena Estreptocócica, Fascitis Necrotizante, Flegmón periuretral, Celulitis Sinérgica Necrotizante, Síndrome idiopático del Pene y Escroto y Erisipela Gangrenosa Perineal2,7,8. No obstante, esta enfermedad está aún asociada con el epónimo Fournier.
La Gangrena de Fournier constituye una emergencia quirúrgica potencialmente letal que afecta a hombres, mujeres y niños, presentando una gran variabilidad en las manifestaciones clínicas, la cual se ha visto incrementada por el aumento de la población inmunodeprimida. Debido a esto último, se requiere un tratamiento agresivo, oportuno y multidisciplinario con el fin de obtener los mejores resultados en este grupo de pacientes.
DEFINICIÓN
Se define como una fascitis necrotizante tipo I que afecta al periné, genitales o región perianal, caracterizada por una evolución fulminante, presentando una rápida progresión y acción sinérgica polimicrobiana que se extiende a lo largo de los planos fasciales, produciendo endarteritis obliterante y trombosis de los vasos subcutáneos, resultando en necrosis del tejido isquémico1,7.
EPIDEMIOLOGÍA
La Gangrena de Fournier ha sido descrita en ambos géneros y en todas las edades. Se han publicado aproximadamente 70 casos en la literatura médica de pacientes pediátricos afectados8. En el caso de las mujeres, esta enfermedad se ha asociado a infección de las glándulas de bartolino, aborto séptico e infección de episiotomía, entre otros. Los hombres superan a las mujeres en prevalencia, con una relación de 10:1. Esta disparidad en los casos se podría explicar por la dificultad de reconocer la condición en la población femenina, y porque éstas poseen un mejor sistema de drenaje de secreciones a través de la vagina2.
La edad promedio de presentación es de 40 años9. El mayor número de casos publicados se ha producido en EEUU y Canadá. La verdadera incidencia de la enfermedad es desconocida, pero se registraron entre 1989 a 1998 un promedio de 97 casos por año2, lo cual ha aumentado en las últimas décadas, producto de una mayor sensibilización, información, longevidad e inmunosupresión de la población.
ETIOLOGÍA
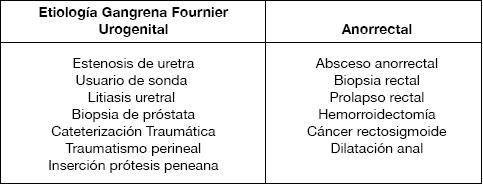
A pesar de que la Gangrena de Fournier fue definida en su descripción original como una entidad idiopática, actualmente la etiología es identificable en un 95% de los casos11. Dentro de las causas más comunes encontramos las infecciones anorrectales (30%-50%), infecciones genitourinarias (20%-40%) e infecciones cutáneas (20%)12. (Tabla 1). El origen anorrectal es la etiología más frecuente y tiende a presentar un peor pronóstico en relación a las causas urológicas13,14.
 |
En los casos en que no es posible determinar el origen de la infección, se debe sospechar un origen abdominal, el cual debe ser investigado, ya que esto puede cambiar significativamente el manejo clínico de estos pacientes1. (Tabla 2).
 |
Los agentes causales son diversos, incluyendo una combinación de gérmenes aerobios y anaerobios como Streptococcus, Staphylococcus aureus, Bacteroides, E. coli, Klesiella sp., Enterococos y Pseudomonas, con un promedio de tres bacterias en los cultivos de cada paciente diagnosticado16,17. Los gérmenes anaerobios son aislados con menor frecuencia de lo esperado, debido a problemas en la recolección o procesamiento de la muestra17.
Estos microorganismos son de baja virulencia y un gran número de ellos pertenece a la flora habitual de vía digestiva y periné. Sin embargo, en presencia de alguna lesión local asociada a patologías sistémicas como diabetes mellitus, alcoholismo, neoplasias, VIH, insuficiencia renal, desnutrición y drogas inmunosupresoras, estas bacterias se tornan extremadamente destructivas17.
El deterioro de la inmunidad celular provoca que la infección se disemine a una velocidad alarmante de aproximadamente 2,3 cm/hr.8, por lo que una infección perianal puede penetrar la fascia de Colles, tomar anteriormente la fascia de Buck, la fascia de Dartos y alcanzar con rapidez la fascia de Scarpa y propagarse por la pared abdominal hasta la clavícula18.
PRESENTACIÓN CLÍNICA
La presentación clínica es variable, pudiendo caracterizarse por un dolor anorectal o genital con mínima evidencia de necrosis cutánea, o mostrar una rápida extensión de la necrosis en la piel y tejidos blandos. Incluso, en algunas ocasiones se puede presentar como una sepsis sin foco aparente19.
Se ha podido distinguir clínicamente cuatro fases distintas. La 1ª fase dura habitualmente 24 a 48 hrs. y se caracteriza por una evolución inespecífica, semejante a un cuadro gripal, asociada a un endurecimiento local con prurito, edema y eritema de los tejidos afectados. En la 2ª fase (fase invasiva), la cual es de corta duración, surgen manifestaciones inflamatorias locales, como dolor perineal, eritema escrotal y/o peneano y fiebre. La 3ª fase (fase de necrosis) se caracteriza por un rápido agravamiento del estado general, con evolución a shock séptico en el 50% de los casos. A nivel local, aumenta la tensión de los tejidos con flictenas hemorrágicas que evolucionan rápidamente a necrosis. En la 4ª fase se produce la restauración de los tejidos necrosados, con cicatrización lenta, inicialmente granulación profunda y posteriormente epitelización. Existe también un restablecimiento progresivo de los parámetros generales20.
DIAGNÓSTICO
El diagnóstico se basa en el examen clínico, por medio del cual el origen de la infección puede ser establecido en la mayoría de los pacientes1. Exámenes como los hemocultivos (positivos en 20% de los casos), el hemograma y el estudio bioquímico permiten orientar la antibioterapia, establecer índices pronósticos y evaluar la evolución del tratamiento21.
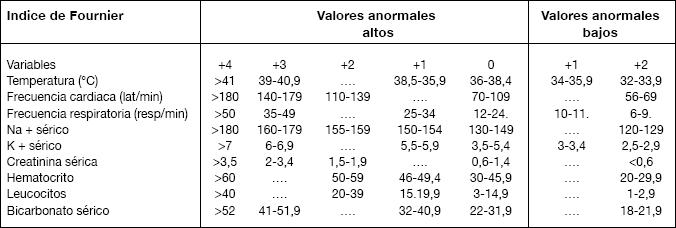
El índice de severidad de Fournier es una herramienta que nos entrega información sobre el pronóstico de estos pacientes. Si el índice es > 9, la mortalidad es cercana al 75%; si el índice es 9, la tasa de supervivencia alcanza el 78%22. (Tabla 3).
 |
A pesar de que el diagnóstico de Gangrena de Fournier es eminentemente clínico, la evaluación imagenológica es útil en los casos en que existe duda diagnóstica, y para determinar la real extensión de la lesión. La radiografía de pelvis puede mostrar aire en los tejidos. La ecografía es útil para diferenciar anomalías intraescrotales y puede evidenciar engrosamiento e inflamación de la pared escrotal con gas en su interior23. La tomografía computada es la mejor técnica de imagen en estos casos, ya que es más específica para determinar la extensión de la enfermedad, etiología subyacente, engrosamiento de los planos fasciales con presencia de gas,infiltración de la grasa, y eventual progresión intraabdominal o retroperitoneal24.
La presencia de gas en los tejidos blandos puede detectarse de manera precoz, antes que en el examen clínico, mediante la tomografía computada. Sin embargo, la ausencia de aire subcutáneo en el escroto o periné no excluye el diagnóstico de Gangrena de Fournier, ya que se ha reportado hasta un 10% de pacientes cuyas imágenes no muestran enfisema subcutáneo25.
TRATAMIENTO
Los pilares fundamentales en el tratamiento de la Gangrena de Fournier son el manejo hidroelectrolítico y nutricional, la antiobioterapia de amplio espectro y el desbridamiento quirúrgico amplio. Sin embargo, debemos tener en consideración que esta enfermedad constituye una emergencia quirúrgica, por lo que la remoción extensa de los tejidos desvitalizados no debe ser retrasada26.
El apoyo nutricional debe ser considerado para mantener un balance nitrogenado positivo que garantice una adecuada cicatrización de la herida, la cual ocurre por segunda intención. Sin embargo, en los casos de lesiones extensas se hace necesario cubrir los defectos con colgajos miocutáneos o injertos de espesor total21.
En relación a la terapia antibiótica se recomienda el uso de un esquema triasociado que incluya cefalosporinas de tercera generación o aminoglucósidos para combatir aerobios gram-negativos, penicilina para especies de Estreptococo, y metronidazol o clindamicina para cubrir gérmenes anaerobios26.
El objetivo de la cirugía es eliminar todos los tejidos no viables, controlar la progresión de la infección local y aliviar la toxicidad sistémica. El desbridamiento quirúrgico debe ampliarse hasta que los tejidos estén bien perfundidos y se identifique tejido vital. El tejido que es fácilmente separado del plano fascial tiene que ser completamente eliminado. De ser factible, debe mantenerse puente de piel para evitar el ano flotante1,2.
Es frecuente que se requiera de nuevas exploraciones para manejar el proceso infeccioso, con un promedio de 3 reintervenciones por paciente7. Debe sospecharse el origen abdominal si no se encuentra un claro origen perineal, por lo que en este caso debe considerarse una exploración abdominal27.
La realización de colostomía debe evaluarse en forma particular y no plantearse de forma arbitraria en la primera intervención. Su objetivo es proteger la herida de la contaminación fecal, de manera de bajar la carga bacteriana en el área cruenta y evitar que se perpetúe el cuadro infeccioso. Actualmente, las indicaciones absolutas de colostomía son la incontinencia fecal clínica y la perforación rectal. No debería realizarse la colostomía únicamente basándose en la superficie corporal afectada o la competencia inmunológica del paciente28. En los últimos meses han aparecido nuevos dispositivos que permiten realizar una derivación fecal sin colostomía. Entre ellos se encuentra el Flexi Seal, el cual consiste en un sistema de manejo de deposiciones de silicona, que presenta un balón de retención que se introduce en el interior del recto, con un dispositivo de señal que indica cuando el balón está inflado. Además posee un lumen de irrigación para administrar fluidos y una bolsa recolectora con filtro de carbón. De esta manera es posible evitar las complicaciones relacionadas a la colostomía, incluyendo las derivadas de la posterior reconstitución del tránsito29.
La cistostomía debe ser planteada cuando el origen de la infección es urológico; en estenosis de uretra y extravasación de orina1.
En la mayoría de los casos los testículos no se ven comprometidos, debido a que su irrigación proviene de la arteria testicular, cuyo origen es intraabdominal. Los testículos se necrosan cuando la fuente infecciosa es retroperitoneal, intraabdominal, o cuando aumenta la extensión de la lesión. La orquidectomía puede ser necesaria hasta en un 24% de los casos30.
A pesar de que no se ha demostrado ningún beneficio definitivo con el uso de oxígeno hiperbárico, es razonable su utilización después de un desbridamiento quirúrgico adecuado31.
Después del tratamiento quirúrgico, es necesario realizar curaciones diarias con cambio de vendaje y evaluación constante de la herida operatoria, hasta la formación de tejido granulatorio eficiente. Por otra parte, se ha demostrado el uso de miel no procesada como método para acelerar la cicatrización, digerir tejidos necróticos y destruir gérmenes gracias a sustancias antimicrobianas inespecíficas que contiene. Además, la miel estimula el crecimiento y la multiplicación de células epiteliales en los bordes de la herida, lo cual se evidencia en la primera semana de aplicación local9,31.
El cierre asistido por vacío (VAC por Vacuum-Assisted Closure), es una técnica relativamente nueva para el manejo de las heridas, la cual ha comenzado a ser utilizada en los casos de Gangrena de Fournier, obteniendo heridas mucho más limpias sin exudados, aún en el caso de heridas extremadamente problemáticas y con bolsillos profundos32.
PRONÓSTICO
La tasa de mortalidad fluctúa de un 3 a un 38% en las distintas series, dependiendo de la agresividad de la patología y la precocidad del tratamiento quirúrgico. El riesgo de mortalidad aumenta con la edad y el compromiso sistémico, siendo las causas de muerte más frecuentes la sepsis severa, coagulopatías, insuficiencia renal aguda, cetoacidosis diabética y falla multiorgánica8.
El pronóstico después de la enfermedad es generalmente bueno, pero existe hasta un 50% de hombres afectados en la región peneana que presentan dolor durante la erección, debido al proceso cicatrizal32.
La Gangrena de Fournier es una patología que debe sospecharse en todo paciente con compromiso de genitales y región perineal, independiente del sexo y la edad. Asociado a un tratamiento quirúrgico agresivo y precoz, que permita reducir la tasa de mortalidad tan elevada que presenta aún esta enfermedad.
REFERENCIAS
1. Morpurgo E, Galandiuk S. Fournier’s gangrene. Surg Clin North Am 2002; 82: 1213-24.
2. Eke N. Fournier’s Gangrene. A review of 1726 cases. Br J. Surg 2000, 87: 718-28.
3. Litchfield WR. The bittersweet demise of Herod the Great. J R Soc Med 1998; 91: 283-4.
4. Nathan B. Fournier’s gangrene: a historical vignette. J Can Surg 1998; 41: 72.
5. Baurienne H. Sur une plaie contuse qui s’est terminee par le sphacele de le scrotum. J Med Chir Pharm 1764; 20: 251-6.
6. Fournier JA. Gangrene foudroyante de la verge. Medecin Pratique 1883; 4: 589-97.
7. García M, Acuña L, Gutierréz G, Martínes M. Gangrena de Fournier: Nuestra Experiencia en 5 años, revisión de la literatura y valoración del índice de severidad. Actas Urol. Esp. 2009; 62(7): 532-540.
8. Urdaneta-Carruyo E, Méndez-Parra A, Urdaneta-Contreras AV. Gangrena de Fournier en la edad pediátrica. Memorias Congreso Nacional de Puericultura y Pediatría. Puerto La. Cruz, Venezuela, 2005.
9. Urdaneta Carruyo E, Méndez Parra A, Urdaneta Contreras A. Gangrena de Fournier. An Med Interna 2007; 24: 190-194.
10. Paty R, Smith AD. Gangrene and Fournier’s gangrene. Urol Clin North Am. Feb 1992; 19(1): 149-62.
11. Jorge P. Gómez. Gangrena de Fournier. Arch. Esp v.59 n.8 Madrid oct. 2006.
12. A Thwaini, A Khan, A Malik, J Cherian, J Barua, I Shergill, and K Mammen. Fournier’s gangrene and its emergency management. Postgrad Med J. 2006 August; 82(970): 516-519.
13. Benizri E, Fabiani P, Migliori G, et al. Gangrene of the perineum. Urology 1996; 47: 935-9.
14. Baskin LS, Carroll PR, Cattolica EV, et al. Necrotising soft tissue infections of the perineum and genitalia. Br J Urol 1990; 65: 524–9.
15. Yaghan RJ, Al-Jaberi TM, Bani-Hani I. Fournier’s gangrene. Changing face of the disease. Dis Colon Rectum 2000; 43: 1300–8.
16. Asci R, Sarikaya S, Bu¨yu¨ Kalpelli R, et al. Fournier’s gangrene: risk assessment and enzymatic debridement with lyophilized collagenase application. Eur Urol 1998; 34: 411–8.
17. Yaghan RJ, Al-Jaberi TM, Bani-Hani I. Fournier’s gangrene. Changing face of the disease. Dis Colon Rectum 2000; 43: 1300–8.
18. Saijo S, Kuramoto Y, Yoshinari M. et al. Extremely extended Fournier’s gangrene. Dermatologica 1990. 181: 228–32.
19. Paty R, Smith AD. Gangrene and Fournier’s gangrene. Urol Clin North Am 1992; 19: 149-62.
20. Encycl Med Chir. Nephrologie-Urologie. 2001; 18- 642- A10.
21. Horta R, Cerqueira M, Marques M, Ferreira P, Reis J y Amarante J. Gangrena de Fournier: de urgencia urológica hasta el departamento de cirugía plástica. Actas Urol Esp. 2009; 33(8): 925-9.
22. Laor E, Palmer LS, Tolia BM, Reid RE and Winter HI: Outcome prediction in patients with Fournier’s gangrene. J Urol 1995; 154: 89.
23. Kane CJ, Nash P, McAninch JW. Ultrasonographic appearance of necrotizing gangrene: aid in early diagnosis. Urology 1996; 48: 142–4.
24. Levenson RB, Singh AK, Novelline RA. Fournier gangrene: role of imaging. Radiographics. 2008 Mar 28(2): 519-28.
25. Sherman J, Solliday M, Paraiso E, Becker J, Mydlo JH. Early CT findings of fournier´s gangrene in a healthy male. Clin Imaging 1998 ; 22(6): 425-7.
26. Xeropotamos NS, Nousias VE, Kappas AM. Fournier’s gangrene: diagnostic approach and therapeutic challenge. Eur J Surg 2002; 168: 91-5.
27. Gerber GS, Guss SP, Pielet RW. Fournier’s gangrene secondary to intra-abdominal processes. Urology 1994; 44: 779–82.
28. Billy Jiménez Bobadilla et al. Utilidad de la colostomía en la gangrena de Fournier y su valor predictivo de mortalidad. Cirujano General Vol. 30 Núm. 3 – 2008.
29. O. Estrada, I. Martinez, M. Del Bas, S. Salvans, L.A. Hidalgo. Rectal diversion without colostomy in Fournier´s gangrene. Tech Coloproctol (2009) 13: 157-159.
30. Martínes F; Rodrigues C; Solano M; Necrosis testicular por Gangrene de Fournier: un caso excepcional. Arch Esp Urol. 2002 Apr 55(3) 309-11.
31. Subrahmanyam M, Ugane SP. Honey dressing beneficial in treatment of Fournier’s gangrene. Indian Journal of Surgery 2004; 66: 75-7.
32. Thomas Santora, MD, Fournier Gangrene, Emedicine. Updated: Mar 19, 2009.