Cuad.
Cir. 2011; 25: 75-80
DOI: 10.4206/cuad.cir.2011.v25n1-11
ARTÍCULO DE ACTULIZACIÓN
Prevención y tratamiento de náuseas y vómitos postoperatorios
Prevention and treatment of postoperative nausea and vomiting
Erick Castillo F. 1, Valentina Hernández N. 2, Carolina Quintana P. 2, Alvaro Elgueta C. 3
1 Residente
de Cirugía. Instituto de Cirugía. Universidad Austral de Chile.
2 Interna de Medicina. Universidad Austral
de Chile.
3 Médico
Anestesiólogo. Hospital Base Valdivia. Correspondencia: Dr. Felipe Imigo,
felipeimigo@gmail.com.
RESUMEN
Las náuseas y vómitos postoperatorios son complicaciones habituales de la anestesia y la cirugía en la práctica diaria, por lo que todo cirujano debe ser capaz de reconocerlas y enfrentarlas como tal. Sin embargo, la prevención y manejo de éstos no siempre es el adecuado, lo cual repercute en el confort de los pacientes. Descartando que esta complicación sea secundaria a la intervención quirúrgica, es necesario tener conocimiento respecto al arsenal farmacológico disponible en nuestro medio que nos permita un postoperatorio mejor tolerado. El objetivo de este trabajo es dar a conocer la evidencia actual respecto al óptimo manejo de estas complicaciones.
Palabras claves: antieméticos, náuseas y vómitos normal.
ABSTRACT
The postoperative nausea and vomiting are common complications of anesthesia and surgery in daily practice, so that every surgeon should be proficient to recognize and treat them as such. However, their prevention and management is not always adequate, which affects the comfort of patients. Discarding this complication secondary to surgical intervention, is necessary to have knowledge about the pharmacological arsenal available in our environment that allows us a better tolerated postoperatively. The aim of this paper is to present the current evidence regarding the optimal management of these complications.
Key words: antiemetics, nauseas and vomiting.
INTRODUCCIÓN
Las náuseas y vómitos postoperatorios (NVPO) son complicaciones habituales en el ámbito anestésico y quirúrgico, alcanzando en pacientes de bajo riesgo una incidencia de 25-30% y en los de alto riesgo hasta 70-80%.
Además del disconfort que genera en los pacientes, determinan mayor morbilidad postoperatoria, dada principalmente por alteraciones hidroelectrolíticas y riesgo de broncoaspiración. Asimismo, el fenómeno de valsalva aumenta la tensión en la línea de sutura, favoreciendo la formación de hematomas y dehiscencias.1
Por otra parte, no deja de ser importante el aumento que genera en los costos en salud, ya que el 76% y 78% de los pacientes ambulatorios, considera a las náuseas y los vómitos, respectivamente, como un factor importante de ser abolido en el postoperatorio, de hecho, estarían dispuestos a pagar en promedio 56 dólares por un antiemético que evitará completamente las NVPO. Los que presentaron náuseas y vómitos pagarían 73 y 100 dólares, respectivamente.
Existen pocos estudios que demuestren la asociación de factores de riesgo independiente con la presentación de un episodio de NVPO, sin embargo dentro de los más nombrados se encuentran el sexo, antecedentes de tabaquismo, cinetosis, tipo y duración de la cirugía, fármacos anestésicos y tratamiento del dolor pre y postoperatorio.2,4
FISIOPATOLOGÍA
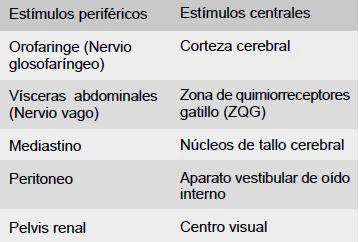
El centro del vómito se encuentra en la formación reticular ascendente del troncoencéfalo, relacionándose con el núcleo del tracto solitario (NTS) y el área postrema, en la cual se localiza la zona de quimiorreceptores gatillo (ZQG) (Figura 1).
FIGURA 1. El centro
del vómito recibe estímulos centrales y periféricos
a través de la ZQG. |
 |
El área postrema no posee barrera hematoencefálica efectiva, por lo que recibe estímulos presentes en la sangre o el líquido cefalorraquídeo y luego los transmite a la ZQG.5,6
Se han descrito distintos tipos de receptores que intervienen en la generación de náuseas y vómitos, como los receptores de dopamina tipo 2 (D2), receptores de serotonina tipo 3 (5-HT3), receptores de histamina tipo 1 (H1) y receptores colinérgicos muscarínicos tipo 1 (M1).
La mayoría de los fármacos antieméticos ejercen su acción por bloqueo de uno o más de estos receptores. La ZQG es rica en receptores D2 y 5-HT3. El NTS posee múltiples receptores, como los D2, H1, M1, receptores del sistema opioide endógeno y receptores del sistema neurokinina.
Al estimularse estos receptores, ejecutan la señal al centro del vómito, originando el estímulo eferente, el que se transmite por las vías eferentes vegetativas (pares craneales V, VII, IX, X y XII) y somáticas (nervios frénicos, intercostales y abdominogenitales), para finalmente producir el reflejo del vómito.5,6
Los receptores D2 se encuentran también a nivel gástrico y al parecer intervienen en la inhibición de la motilidad gástrica, retardando el vaciamiento gástrico.
También existen otros estímulos que generan náuseas y vómitos, tales como hipotensión arterial, hipovolemia, estimulación vagal, dolor, hipoxemia y fármacos (opiáceos, etomidato, neostigmina y óxido nitroso).7
FACTORES DE RIESGO
Se han descrito diversos factores asociados a náuseas y vómitos postoperatorios, que se pueden clasificar en dependientes del paciente, de la intervención quirúrgica y de la técnica anestésica.
Inherentes al paciente
Los factores de riesgo descritos como predictores independientes de NVPO son: 1) sexo femenino, hasta tres veces más riesgo de sufrir NVPO; 2) condición de no fumador, dos veces más riesgo que los fumadores, sin embargo, el mecanismo fisiopatológico de este efecto protector no está claro; 3) historia de NVPO o de cinetosis; 4) situaciones médicas que predisponen a NVPO, como patologías gastrointestinales (hernia hiatal, reflujo gastroesofágico), metabólicas (diabetes mellitus, uremia elevada, desequilibrios hidroelectrolíticos), tumores cerebrales (por aumento de la presión intracraneana), abdomen agudo y/o obstrucción intestinal.8
Propios de la intervención quirúrgica
Las cirugías con mayor incidencia de NVPO según Apfel son la colecistectomía laparoscópica y las histerectomías9. Sin embargo, existe controversia si es que constituye un factor de riesgo independiente.10
Por el contrario, la duración de la cirugía se ha establecido como un predictor independiente de NVPO. Se estima que cada 30 minutos de aumento en el tiempo quirúrgico, incrementa el riesgo de NVPO en un 60%, a partir de un riesgo basal del 10%. Por lo tanto, luego de 30 minutos, el riesgo aumentaría de un 10% a un 16%.
Relacionados con la técnica anestésica
A diferencia de los anteriores, los factores relacionados con la anestesia se pueden controlar, por lo que se deben tener en cuenta en el enfrentamiento inicial.
Los más relevantes son el uso de anestesia general con anestésicos volátiles, de óxido nitroso y de opioides en el intra y postoperatorio.
Aunque la anestesia raquídea puede asociarse a reacción vagal, se describe una menor incidencia de NVPO cuando se emplean técnicas de anestesia regional.
La anestesia general inhalatoria presenta un riesgo de NVPO dos veces mayor, comparada con la anestesia intravenosa total con propofol.
Un estudio randomizado concluyó que los anestésicos volátiles fueron la principal causa de vómitos en el postoperatorio precoz, y demostró un efecto dosis-dependiente similar para los distintos halogenados (isoflurano, enflurano y sevoflurano).
Respecto al óxido nitroso, dos meta-análisis concluyeron que la omisión del óxido nitroso reduce el riesgo de NVPO en un 28%.11,12
En relación a los opioides, se conoce que su acción emetizante se debe a estimulación directa de la ZQG, prolongación del vaciamiento gástrico, reducción de la motilidad gastrointestinal y sensibilización del sistema vestibular. Se ha determinado una clara relación entre la incidencia de NVPO con las dosis de opioides pre y postoperatorios utilizados.
RECOMENDACIONES DE MANEJO
Las estrategias sugeridas para el manejo de las NVPO son estratificar en los pacientes el riesgo de sufrir NVPO, reducir los factores de riesgo basal, realizar profilaxis sólo en pacientes de alto riesgo y considerarla en pacientes de moderado riesgo, utilizar terapia de rescate en aquellos pacientes en que la profilaxis no fue efectiva y en aquellos pacientes con NVPO que no recibieron.13
Fármacos utilizados en tratamiento
NVPO Antagonistas del receptor de serotonina
Ondansetrón
Se ha demostrado que la eficacia de este fármaco es mayor al ser administrado al final de la cirugía, y que tiene mayor efecto en disminuir los vómitos con respecto a las náuseas. La dosis recomendada para profilaxis es 4 a 8 mg en adultos y 50 a 100 ug/kg en niños, requiriendo un número necesario a tratar (NNT) de 5 a 6.17
En 2004, Apfel et al demostraron que el uso de ondansetrón disminuía en un 26% el riesgo de presentar NVPO.18
En otro estudio realizado se encontró que la reducción a la mitad de la dosis de ondansetrón aumentó el riesgo de náuseas o vómitos en 1,43 (1,08 a 1,90).
Dentro de los efectos secundarios se describen cefalea, mareo, enrojecimiento, elevación enzimas hepáticas y constipación.17
Tropisetrón
La dosis recomendada para profilaxis es de 2 a 5 mg. El NNT para prevenir náuseas es de 6,7 y para prevención de vómitos 5.17
Granisetrón
Reducir a la mitad la dosis de granisetrón aumentó el riesgo de vómitos 1,64 (1,23 a 2,20), náuseas o vómitos 2,12 (1,48 a 3,05) y necesidad de tratamiento 2,10 (1,21 a 3,66).
Actualmente se recomienda para el manejo de NVPO, a dosis de 0,35 a 3 mg. Para el tratamiento de NVPO establecido bastarían dosis de 0,1 mg.
Hasta el momento no existe evidencia que demuestre diferencias en eficacia o efectos secundarios entre los diferentes antagonistas de receptor de serotonina.17
Otros fármacos
Droperidol
Ha sido utilizado como fármaco de primera línea en profilaxis de NVPO, ya que en dosis de 1,25 mg, ha demostrado ser mejor respecto a costo-efectividad que ondansetrón (dosis 4 mg).
La mayor eficacia se logra con 1,5 a 2,5 mg de droperidol, con NNT de 7. En niños la dosis recomendada es 50 a 75 ug/kg. Se ha visto que es más efectivo cuando se administra al final de la cirugía y cuando se administra en conjunto con morfina como analgésico (15 a 20 ug por mg de morfina). Sedación y somnolencia son poco comunes como efectos secundarios al utilizar bajas dosis. Se han reportado casos de prolongación de QT asociado al uso de droperidol en dosis habituales, en 2001 la FDA emitió una advertencia al respecto, provocando una disminución importante en el uso de droperidol en USA.17
Metoclopramida
La dosis alta ha demostrado ser efectiva en el manejo de emesis inducida por quimioterapia, sin embargo se asocia a múltiples efectos adversos. Para reducirlos, se han realizado estudios utilizando bajas dosis de metoclopramida, de los cuales aproximadamnte el 50% ha mostrado que metoclopramida no es más efectiva que placebo en reducir NVPO. Henzi et al reportó que metoclopramida no tiene efecto antinauseoso, con un NNT de 9,1 para prevenir vómitos tempranos (antes de 6 hrs) y 10 para prevenir presencia de vómitos tardíos.17
Dexametasona
Dado el éxito en el uso de dexametasona para prevenir emesis por quimioterapia, se estudió su uso en prevención de NVPO. Se recomienda su administración en dosis de 5 a 10 mg en adultos. En un meta-análisis se demostró que es especialmente efectiva en reducir la incidencia de NVPO tardíos con un NNT de 4,3. Además sería más efectiva si se administra previo a la inducción anestésica que posterior a ésta.17
En otro estudio se encontró que la reducción a la mitad de la dosis de dexametasona aumentó el riesgo de náuseas en 1,5 (1,02 a 2,24) y de náuseas o vómitos en 1,41 (1,05 a 1,88). Así mismo, se demostró que su uso en pacientes en comparación con su no administración redujo el riesgo de NVPO en 26,4%.2
Clonidina
Se desconoce la manera de interpretar la relación dosis-respuesta de la clonidina, porque no fue efectiva cuando se combinaron todos los estudios controlados con placebo. Es posible que las dosis mayores de clonidina puedan tener un efecto comparadas con placebo.
Asociación de fármacos antieméticos
Se realizó un análisis post-hoc después de la publicación del estudio IMPACT.17 El estudio evaluó la interacción de tres fármacos antieméticos (dexametasona, droperidol, ondansetrón) en 4083 participantes. Los resultados evidenciaron que el efecto de cada fármaco fue independiente de si el fármaco se administró solo, o asociado a uno o a los otros dos fármacos.
De esta forma, se realizó un estudio en el cual todos los participantes recibieron un fármaco antiemético y un grupo de ellos un segundo fármaco antiemético. El grupo control fueron los pacientes que recibieron sólo un antiemético y un placebo por el segundo fármaco.
Se calculó que los intervalos de confianza del 95% de estas dos categorías de estudios se superpusieron para cada medida de resultado de cada fármaco, es decir, no hubo pruebas de que los efectos de estos fármacos se modificaran con la administración de un segundo o tercer fármaco.
La única excepción fue con el uso de granisetrón. Los intervalos de confianza del 95% no se superpusieron en ninguna medida de resultado y el riesgo relativo en cada resultado fue menor en el subgrupo de estudios con administración de granisetrón, asociada con otro antiemético. Por sí solo, este resultado apoyaría la hipótesis de que el efecto del granisetrón es sinérgico con el de otros antieméticos.
Terapia antiemética profiláctica multimodal
Con el objetivo de disminuir la aparición de NVPO, se creó una estrategia que incluye el uso de premedicación con midazolam, inducción y mantención de la anestesia con remifentanilo, evitando relajantes musculares y óxido nitroso, oxígeno al 80%, ketorolaco y una combinación de droperidol 0,625 mg, dexametasona 10 mg y ondansetrón, administrados al finalizar la cirugía, la cual mostró una tasa de respuesta del 98%, además de mayor satisfación del paciente respecto al grupo que recibió terapia antiemética según necesidad.18
Efectos secundarios del uso de antieméticos
De los estudios incluidos, aproximadamente un tercio no informó efectos secundarios. Sin embargo es necesario considerar la existencia de efectos secundarios raros, que por ser muy infrecuentes no ocurrieron o no fueron identificados por los autores como secundarios al uso del fármaco.
En el 2001 la FDA incluyó en el etiquetado de droperidol la advertencia de posible asociación del fármaco con la prolongación del intervalo QT, arritmias torsades de pointes y muerte. Los efectos secundarios asociados al uso de fármacos antieméticos se encuentran aún en discusión, existiendo médicos que no consideran válidas estas asociaciones.
Profilaxis antiemética
El beneficio del uso de un fármaco antiemético profiláctico depende del riesgo de desarrollar los resultados adversos que se previenen y de la gravedad de éstos, considerando los efectos no deseados provocados por el uso del fármaco. Es así como la mayoría de los pacientes no se beneficia con la administración de un antiemético profiláctico, pero todos están expuestos al riesgo de desarrollar los efectos secundarios asociados a su uso.
Para reducir la exposición de los pacientes a la profilaxis antiemética innecesaria, se han utilizado sistemas de calificación para predecir las náuseas o vómitos postoperatorios, pero estos sistemas pueden no ser siempre predictores útiles.16
CONCLUSIONES
La mayoría de los pacientes que reciben un fármaco para prevenir las náuseas o los vómitos después de la cirugía no obtendrán beneficio alguno del mismo.
Se notifica que las náuseas o los vómitos afectan como máximo a 80 de 100 personas después de la cirugía. Si todas estas 100 personas reciben un fármaco, 28 se beneficiarán y 72 no.
Las náuseas y los vómitos juntos son generalmente menos frecuentes y por consiguiente los fármacos son menos útiles. De cada 100 personas, de las cuales 30 presentarán vómitos o náuseas después de la cirugía si reciben placebo, diez personas se beneficiarán con un fármaco y 90 no. Entre uno a cinco pacientes de 100 que reciben un antiemético profiláctico puede esperar presentar un efecto secundario leve, como cefalea, sedación o sensación de sequedad en la boca.
Existen pruebas convincentes de que ocho fármacos reducen las NVPO en una proporción similar: droperidol, granisetrón, metoclopramida, ondansetrón, tropisetrón, dolasetrón y dexametasona.
Sólo hay pruebas limitadas de que al aumentar la dosis del fármaco se obtenga un mayor beneficio: hay pruebas convincentes de que mayor cantidad del droperidol es más efectivo. Para dexametasona y el ondansetrón las pruebas son limitadas. Las pruebas de las diferencias de la eficacia de estos ocho fármacos no son convincentes.
REFERENCIAS
1. Kovac AL. Prevention and treatment of postoperative nausea and vomiting. Drugs 2000; 59: 213-43.
2. Apfel C, Roewer N, Korttila K. How to study postoperative nausea and vomiting. Acta Anaesthesiologica Scandinavica 2002, 46: 921-8.
3. Cohen M, Duncan P, Deboer D, Tweed A. The postoperative interview assessing risk factors for nausea and vomiting. Anesthesia & Analgesia, 1994. Vol. 78 no. 1: 7-16.
4. Watcha M F, White P F. Postoperative nausea and vomiting: its etiology, treatment, and prevention. Anesthesiology. 1992; 77: 162-84.
5. Ho KY, Chiu JW. Multimodal Antiemetic Therapy and Emetic Risk Profiling. Ann Acad Med Singapore 2005; 34: 195-205.
6. Bel IM, Gambús PC. Risk assessment, prophylaxis and treatment for postoperative nausea and vomiting. Rev Esp Anestesiol Reanim 2006; 53: 301-11.
7. Golembiewski J, Chernin E, Chopra T. Prevention and treatment of postoperative nausea and vomiting. Am J Health-Syst Pharm 2005; 62: 1247-60.
8. Spiller RC. ABC of the upper gastrointestinal tract: Anorexia, nausea, vomiting, and pain. BMJ 2001; 323: 1354-7.
9. Apfel C, Korttila K, Abdalla M, Kerger H, Turan A, Vedder I et al. A factorial trial of six interventions for the prevention of postoperative nausea and vomiting. N Engl J Med 2004; 350: 2441-51.
10. Apfel CC, Roewer N. Risk Assessment of postoperative nausea and vomiting. Int Anaesthesiol Clin 2003; 41: 13-32.
11. Sinclair DR, Chung F, Mezei G. Can postoperative nausea and vomiting be predicted? Anesthesiology 1999; 91: 109-18.
12. Apfel CC, Kranke P, Katz MH, Goepfert C, Papenfuss T, Raush S et al. Volatile anaesthetics may be the main cause of early but not delayed postoperative vomiting: a randomized controlled trial of factorial design. Br J Anaesth 2002; 88: 659-68.
13. Habib AS, Gan TJ. Evidence-based management of postoperative nausea and vomiting: a review. Can J Anesth 2004; 51: 326-41.
14. Gan TJ, Meyer T, Apfel CC, Chung F, Davis P, Eubanks S et al. Consensus Guidelines for Managing Postoperative Nausea and Vomiting. Anesth Analg 2003; 97: 62-71.
15. Apfel CC, Korttila K, Abdalla M, Kerger H, Turan A, Vedder I, et al. IMPACT Investigators. A factorial trial of six interventions for the prevention of postoperative nausea and vomiting. N Engl J Med. 2004 Jun 10; 350(24): 2441-51.
16. Kao Lw, Kirk MA, Evers SJ, Rosenfeld SH. Droperidol, QT prolongation, and sudden death: what is the evidence? Annals of emergency medicine 2003; 41(4): 546-58.
17. Van Den Bosch JE, Kalkman CJ, Vergouwe Y, Van Klei WA, Bonsel GJ, Grobbee DE and Moons KGM. Assessing the applicability of scoring systems for predicting postoperative nausea and vomiting. Anaesthesia 2005, 60: 323-31.
18. Ashraf S. Habib MBBCH MSc FRCA, Tong J. Gan MB FRCA. Evidence-based management of postoperative nausea and vomiting: a review. Can J Anesth 2004, 51: 4 pp 326-41.
19. Watcha MF. Postoperative nausea and emesis. Anesthesiology Clin N Am 2002, 709–22.