ARTÍCULO DE ACTUALIZACIÓN
Cáncer de mama inflamatorio
Camila Toledo S1, María Paz Vera A1, Leonardo Cárcamo G2, Gladys Tapia C1, Juan Antonio Pérez P3.
1 Interno
de Medicina. Universidad Austral de Chile.
2 Residente de Cirugía. Universidad Austral
de Chile.
3 Equipo Cirugía Oncológica, Subdepartamento
de Cirugía. Hospital Base Valdivia. Correspondencia a: Dr. Leonardo Cárcamo
G, leonardocarcamog@gmail.com
RESUMEN
El cáncer de mama inflamatorio es una patología poco frecuente, sin embargo, su importancia radica en la agresividad de su evolución. A nivel nacional no existe estadística certera respecto al porcentaje del cáncer inflamatorio de mama como tal. En el Hospital Base de Valdivia, constituye el 3,3% de los carcinomas mamarios invasores según una revisión de los últimos 3 años. El diagnóstico de esta patología está basado en la sospecha clínica, en pacientes que presenten eritema, edema, piel de naranja, nódulos y/o induración mamaria. La histopatología del tumor primario y de la piel permite la confirmación diagnóstica. En cuanto al tratamiento, en la actualidad existe consenso de que las pacientes deben ser sometidas a un tratamiento multimodal, éste consiste en quimioterapia neoadyuvante, para luego efectuar la terapia locorregional. Lo particular de este tipo de cáncer, es que posee características biológicas intrínsecas de rápida progresión y alto poder de diseminación, lo que le confiere un mal pronóstico.
(Palabras claves: mama; neoplasia; cáncer de mama inflamatorio).
ABSTRACT
Inflammatory breast cancer is a rare disease, but its importance lies in the aggressiveness of its evolution. At the national level there is no accurate statistics on the percentage of inflammatory breast cancer as such. In the Base Hospital of Valdivia, constitute 3.3% of invasive breast carcinomas according to a review of the past 3 years. The diagnosis of this disease is based on clinical suspicion in patients presenting with erythema, edema, cellulitis, nodules, and / or breast induration. The histopathology of the primary tumor and skin allows diagnostic confirmation. As for treatment, there is now consensus that patients should be subjected to a multimodal treatment, starting with neoadjuvant chemotherapy and then perform locoregional therapy. The particularity of this type of cancer is that it has intrinsic biological characteristics of rapid progression and high power spread, which gives a poor prognosis.
(Key words: breast, neoplams, inflammatory breast cáncer.)
GENERALIDADES
El cáncer de mama es una de las neoplasias más frecuentes en la mujer, y se constituye como una de las principales causas de muerte por cáncer dentro del mismo género.
Una forma clínica corresponde al carcinoma inflamatorio mamario (CIM), el cual es una patología muy poco frecuente, y que representa menos del 2% de la totalidad de los carcinomas mamarios1,2, sin embargo, su importancia radica en la agresividad de su evolución.
Es una variante distinta al cáncer de mama no inflamatorio, y presenta como características clínicas: enrojecimiento difuso mamario, edema cutáneo y "piel de naranja". El diagnóstico es básicamente clínico y resulta de gran ayuda la confirmación histopatológica, sin ser ésta indispensable. Es evidente que corresponde a la variante más agresiva del cáncer de mama y que su diagnóstico es generalmente en un estadío avanzado, con una diseminación sistémica precoz, alta tasa de recidiva y escasa respuesta al tratamiento, lo que conlleva un mal pronóstico.1,2'3,4
EPIDEMIOLOGÍA
Se estima que a nivel mundial, el cáncer de mama en todas sus formas, presenta una incidencia cercana a los 700.000 casos nuevos cada año con alrededor de 300.000 fallecimientos5. En nuestro país6, la incidencia estimada por el Programa Nacional de Cáncer de Mama, fue cercana a los 3.100 casos nuevos el 2009, con una tasa de mortalidad observada de 14,5 por 100.000 mujeres.
Al respecto, el cáncer localmente avanzado y el CIM, constituyen un grupo heterogéneo de cáncer de mama que alcanza a un 27% de todos los cánceres diagnosticados en el sistema público de salud6. A nivel nacional no existe estadística certera respecto del porcentaje de CIM como tal. En el Hospital Base de Valdivia, en una revisión de los carcinomas mamarios invasores manejados en Unidad de Patología mamaria en los 3 últimos años, el CIM constituye el 3,3%.
En Estados Unidos se ha estimado que este tipo de patología maligna corresponde a aproximadamente el 2% de todos los cánceres invasores de mama, encontrándose en las mujeres de raza negra una mayor incidencia y una edad menor de presentación en comparación con las mujeres de raza blanca7.
ETIOLOGÍA Y FACTORES DE RIESGO
En la actualidad se han identificado sólo algunos factores de riesgo que se han podido relacionar con el CIM, y entre ellos destacan: etnia afroamericana y el alto índice de masa corporal.1
CLÍNICA
Las pacientes con CIM típicamente presentan: eritema, edema, piel de naranja, y en estadios más avanzados de la enfermedad, la coloración de la mama puede cambiar desde un rosado pálido a un rojo oscuro o morado. El bloqueo de los conductos linfáticos por émbolos tumorales provoca la aparición de nódulos en la piel y la induración mamaria1,4,5.
En un estudio realizado en el Hospital Oncológico Padre Machado de Venezuela, se evidenció que los signos clínicos se presentaban con la siguiente frecuencia: eritema en un 95,8%, edema de piel en un 91,6%, induración mamaria en un 62,5% y retracción complejo areola pezón en un 37,5%. El promedio de presentación de los síntomas fue de 4,63 meses2.
 |
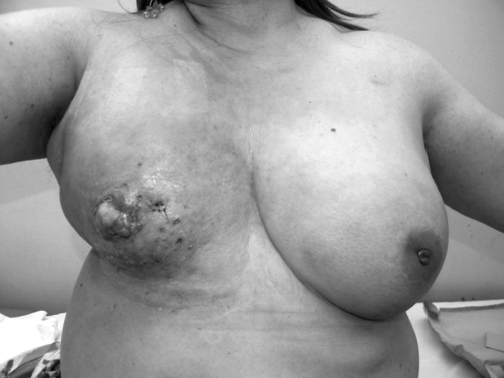
FIGURA
1: Cáncer inflamatorio de mama bilateral. |
Durante el examen físico, la mayoría de las pacientes (62,5%)2 no presenta masa palpable en relación a la mama afectada. No obstante, es posible constatar los cambios ya descritos en la piel.
Al momento del diagnóstico, entre el 55-85% de las pacientes presenta linfoadenopatías axilares y/o supraclaviculares clínicamente comprometidas1,8,9
Se debe tener presente que la clínica puede ser distinta según la raza, así por ejemplo, se ha descrito que este cáncer, en mujeres africanas se expresa casi únicamente con aumento de volumen y piel de naranja, siendo muy excepcional el edema y eritema.1
DIAGNÓSTICO
El diagnóstico del CIM está dado por la sospecha clínica e idealmente por la confirmación mediante la histopatología del tumor primario y de la piel2,3,4,5,10.
Los criterios diagnósticos mínimos estipulados por el último consenso internacional de expertos se definen como:1
| 1) |
Aparición
rápida de eritema, edema y/o "piel de naranja" y/o calor mamario,
con o sin masa palpable. |
| 2) | Menos
de 6 meses de evolución. |
| 3) | Eritema ocupa al menos 1/3 de la mama. |
Es esencial siempre realizar una historia clínica y examen físico completo, asociado al estudio imagenológico y hallazgos patológicos inherentes a la enfermedad9.
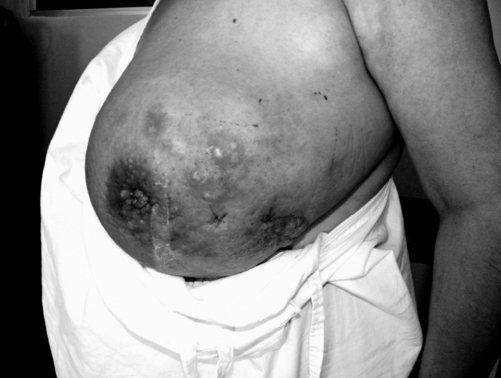 |
FIGURA
2: Apariencia típica de cáncer inflamatorio de mama. |
Imagenología
El rol que cumplen las imágenes dentro de este cuadro es principalmente identificar el tumor primario y facilitar la biopsia, evaluar el estadio locorregional, diagnóstico de metástasis a distancia, finalmente, evaluar la respuesta tumoral a terapia neoadyuvante1,11.
Mamografía
Catalogada como el gold standard en el estudio del cáncer de mama no inflamatorio, no ha demostrado mayor utilidad en esta patología. No existe evidencia sobre cambios precoces mamográficos previos al diagnóstico clínico y sólo se pueden observar signos inespecíficos como el engrosamiento trabecular y cutáneo de la mama afectada1,3,8,11. Es además técnicamente difícil de realizar debido al dolor y rigidez de la mama.
Ultrasonografía
El ultrasonido por su parte, ha entregado resultados más alentadores, delineando lesiones focales en el parénquima mamario, detectando metástasis linfonodales hasta en un 93% en zona axilar y 50% en zona supraclavicular o mamaria interna, facilitando así la toma de biopsias. Suele observarse un área de infiltración del parénquima mamario o un conglomerado de masas dentro de la mama con compromiso de piel y edema subcutáneo1,11.
Resonancia magnética
Ha demostrado ser un examen muy sensible y preciso para señalar una lesión primaria, pudiendo encontrar engrosamiento difuso de la piel asociado a aumento de volumen mamario, edema, tumor y/o refuerzo parenquimatoso anormal. Se discute su rol costo-beneficio y no se considera un examen de rutina actualmente. Su uso radica como herramienta de investigación para evaluar respuesta a nuevas terapias1,11.
PET/TC
Constituye un excelente examen que no es capaz tan sólo de diagnosticar el tumor primario con gran sensibilidad, sino que además es capaz de evaluar la extensión de la enfermedad, el mejor sitio para biopsia (según tasa metabólica) y evaluar fidedignamente los resultados del tratamiento.
Nuevamente se discute también si es un examen costo-efectivo, no encontrándose recomendado actualmente su uso rutinario1,11.
Histopatología
El hallazgo más consistente desde el punto de vista histopatológico en el CIM, es la presencia de numerosos émbolos neoplásicos que invaden los vasos linfáticos tanto en dermis papilar como reticular. Constituye un hallazgo patognomónico y cabe destacar que no existe relación entre el número de émbolos linfáticos tumorales y el compromiso cutáneo en estas pacientes. Paradójicamente no se aprecia inflamación en la muestra como indica su nombre.
Para la toma de biopsia de piel, se sugiere un segmento de 2 mm a 8 mm en diámetro de las áreas más prominentes del aumento de volumen y representativas de coloración cutánea mamaria1. Se describe que estos émbolos tumorales se encuentran hasta en el 75% de los casos, por lo que su ausencia no descarta un CIM.1,3,5
Idealmente se deben obtener además muestras del tumor subyacente y/o linfonodales previo inicio del tratamiento, ya que nos aportará información importante como el estado de los receptores hormonales, la presencia de HER-2, el grado de diferenciación y el tipo histológico entre otros, información importante que nos definirá un pronóstico más certero y nos orientará hacia la terapia que más beneficiará a nuestro paciente. Cabe destacar que al momento del diagnóstico puede ser la única oportunidad para la toma de biopsia, ya que posterior quimioterapia puede incluso desaparecer el tumor, haciendo imposible un nuevo estudio histológico.1,3,5,12
Biología Tumoral
El CIM presenta características intrínsecas que lo diferencia del resto de los cánceres de mama, las cuales determinan en gran medida la agresividad de la patología. Entre ellas observamos un menor porcentaje de receptores hormonales, sobreexpresión del p53, presencia exagerada de E-cadherina y MUC1 (adhesión y aumento de potencial de diseminación angiolinfática), aumento de RhoC y sobreexpresión de HER-2.
El caso de la sobreexpresión de HER-2 es especial en el CIM. La evidencia avala que la presencia de HER-2 representa un factor de mal pronóstico en el cáncer de mama no inflamatorio, sin embargo, en el CIM hay controversia, existiendo evidencia que refiere no alterar el pronóstico e incluso que podría representar un factor favorable13.
DIAGNÓSTICO DIFERENCIAL
Es necesario tener presente algunas patologías como diagnóstico diferencial del CIM, sin embargo, con una adecuada anamnesis y estudio histológico es posible distinguirlas. Algunas de ellas son: infecciones bacterianas como abscesos no puerperales, abscesos retroareolares recurrentes producto de una ectasia ductal complicada y mastitis, (que generalmente están asociadas a fiebre y leucocitosis, a diferencia del cáncer inflamatorio, que no es un verdadero proceso inflamatorio), dermatitis post-radiación, insuficiencia cardíaca congestiva, linfomas primarios, entre otras.1,14
Generalmente lo que dificulta más el diagnóstico es poder diferenciar un cáncer inflamatorio de un cáncer de mama no inflamatorio localmente avanzado, o de una recurrencia que comprometa la piel, lo que se conoce como cáncer inflamatorio secundario.14
ESTADIFICACIÓN
La presencia de infiltración linfonodal y el grado de diseminación, es lo que proporciona una pauta de información relevante en la estatificación del CIM, datos que sin duda también marcan un pronóstico.1,14
Entre el 55% y el 85% de los pacientes presentan metástasis regionales a los linfoganglios axilares o supraclaviculares que podrían ser eventualmente detectados en el examen físico al momento del diagnóstico.
El American Joint Committee on Cáncer 2010 (AJCC)1, refiere en el TNM del CIM como tumor primario T4d, pudiendo pertenecer a los estadios clínicos IIIB, IIIC o IV según el estado linfonodal y presencia de enfermedad metastásica1,2.
TRATAMIENTO
Durante años se intentó manejar la patología mediante cirugía o radioterapia aisladas, presentando altos índices de recidiva local (hasta 50%) y una sobrevida de prácticamente 0% a 5 años.15 En la actualidad existe consenso de que las pacientes con CIM deben ser sometidos a un tratamiento multimodal. Éste consiste en comenzar con quimioterapia neoadyuvante para luego efectuar la terapia locoregional.1,15
Quimioterapia
La quimioterapia neoadyuvante ha demostrado ser la principal arma terapéutica en el CIM, contribuyendo en gran medida a la sobrevida en general y a la tasa de recurrencia local.
Se reporta una sobrevida libre de enfermedad entre 20 a 45% a 5 años y una sobrevida global entre 30 y 70%.
El esquema ideal está aún por definirse, sin embargo se pregona actualmente la terapia combinada de antraciclina más taxanos.1,5,13
Es necesario hacer énfasis en la respuesta tanto clínica como patológica del tumor frente a la quimioterapia. Éste es el principal factor pronóstico, determinando tanto la sobrevida libre de enfermedad como la sobrevida global. Por esto es que debe hacerse énfasis en lograr una respuesta patológica completa1,10,15.
Otro tema en discusión es la quimioterapia a altas dosis, la que consiste en un tratamiento agresivo para luego trasplantar progenitores hematopoyéticos. Ha demostrado resultados promisorios, pero a costa de un aumento en los efectos adversos.1,5,16 Es por eso que se ha buscado algún marcador para determinar quiénes se beneficiarían de la terapia y seleccionar a los candidatos. Es ahí donde se ha postulado la medición de células tumorales circulantes como un test útil, habiendo demostrado que en niveles bajo 5 presenta una mejor respuesta y pronóstico.17
Trastuzumab
Las pacientes que sobreexpresan el gen HER2, deben recibir junto a la quimioterapia neoadyuvante, trastuzumab1,14. Su adición a la terapia ha demostrado mayor tasa de respuesta tumoral. Debe mantenerse una vez terminado el tratamiento hasta completar 1 año de éste14,18,19.
Cirugía
El tratamiento quirúrgico permite el control local y/o regional de la enfermedad1,5,14,20,21. La recomendación para aquellas pacientes que respondieron a la neoadyuvancia es realizar una mastectomía simple extendida, mientras que en aquellas que no respondieron, se debería considerar la radioterapia y posteriormente reevaluar la operabilidad1,5. Debido a que las pacientes necesitarán radioterapia postoperatoria, la reconstrucción mamaria se prefiere postergar para después que ésta se haya realizado5,10,14.
Linfonodo Centinela
No está recomendado, dado:
| 1) |
Compromiso
axilar al diagnóstico entre 55% y 85%. |
| 2) | Émbolos tumorales impiden flujo tinción. |
| 3) | Tumores grandes presentan múltiples drenajes linfáticos. |
| 4) | Fisiología de drenaje alterado por quimioterapia. |
| 5) | Es posible regresión histológica del primer nódulo, pero persistencia en los demás tras quimioterapia. |
| 6) | Precisión del 87.5% con valor predictivo negativo de 71.4%.22 |
Radioterapia
La radioterapia post quirúrgica está recomendada en el tratamiento del CIM, ha demostrado aumentar la sobrevida y disminuir la tasa de recurrencia. La dosis por lo general es de 60 cGy, observándose algunos pacientes que se benefician de un aumento a 66 cG y como lo son:23
| 1) |
<45 años |
| 2) | Márgenes quirúrgicos cercanos o positivos. |
| 3) | 4 o más linfonodos posterior a tratamiento sistémico. |
| 4) | Mala respuesta al tratamiento sistémico. |
Quimioterapia adyuvante
La evidencia actual es escasa en relación a la utilidad de continuar con quimioterapia post cirugía, y en general si la paciente ha completado sus ciclos preoperatorios, no habría indicación adicional para su continuación14.
Terapia endocrina adyuvante
Si la paciente tiene receptores de estrógeno y progesterona positivos debe recibir terapia hormonal5,14.
Nuevas Terapias
Actualmente se están llevando a cabo numerosos estudios acerca de nuevas alternativas terapéuticas que logren producir un quiebre en esta patología de tan mal pronóstico. Entre ellas encontramos fármacos antiangiogénicos como Bevacizumab24, que ha demostrado utilidad mejorando la tasa de respuesta patológica completa. Otros como el Semaxanib y el Pazopanib25 no han tenido tanto éxito, debido a la alta incidencia de efectos adversos asociados a ellos, sin mostrar claro impacto en el pronóstico. También se postula el Tipifarnib1, un inhibidor de la farnesyl transferasa con resultados promisorios.
Merece mención especial el Lapatinib, un inhibidor de tirosinkinasa de acción dual sobre el HER2 y EGFR, que en teoría debería superar en eficacia al Trastuzumab. Se están llevando estudios actualmente, habiendo demostrado su seguridad y eficacia clínicamente18,26
SEGUIMIENTO
Los objetivos de la evaluación post tratamiento para el CIM se enfocan en la detección temprana de la recidiva local, regional o sistémica de la enfermedad, tratamiento de recurrencias y pesquisa precoz de complicaciones.
Se recomienda un seguimiento estricto cada 4 meses durante los 2 ó 3 primeros años, cada 6 meses, desde el tercer al quinto año y en forma anual posteriormente.
El abordaje clínico debe ser completo, y según los hallazgos encontrados, recurrir a otros estudios complementarios.
PRONÓSTICO
El CIM es la forma más agresiva y mortal de cáncer de mama invasivo.
Lo particular de este tipo de cáncer, es que posee características biológicas intrínsecas de una rápida progresión, con un alto poder de diseminación, capacidad de vascularización y potencial angioinvasor.
La expresión de marcadores moleculares como la sobreexpresión de HER2, y E-cadherina, bFGF, VEGF, IL-6, e IL-8 y factores linfoangiogénicos como VEGF-C, VEGF-D, VEGFR-3, Prox-1, y el receptor endotelial de vasos linfáticos además de la regulación disminuida de p27kip1,y las probables mutaciones del gen p53 son factores moleculares, que son reconocidos por tener un peor pronóstico.27
Estos factores se asocian significativamente con el mayor tamaño del tumor y la enfermedad diseminada al momento del diagnóstico10,28.
Además se han descrito en estudios la presencia de genes en el CIM, que no se encontrarían en el cáncer de mama habitual. Un ejemplo son los miembros de la super familia Ras, que contribuiría a la característica metastásica del cáncer, asociado a la estimulación de factores angiogénicos que promoverían su invasión.
La duración mediana de supervivencia global en mujeres es menor de 4 años, incluso con las opciones de tratamiento multimodales1,2,10. La respuesta inicial a la quimioterapia sistémica primaria, es un importante factor pronóstico.
Bibliografía reciente describe que en los últimos 40 años, la supervivencia en general ha sido baja, ya que pacientes tratados con cirugía y/o radioterapia el porcentaje de sobrevivencia a 5 años es cercano al 5%.
Con el advenimiento de la quimioterapia neoadyuvante, asociada a terapia locorregional de cirugía y radioterapia, que en muchos centros se ha adoptado como protocolo estándar de tratamiento, hay nuevas esperanzas14.
La incorporación como inicio de terapia con antraciclinas y taxanos, ha mejorado el pronóstico en comparación con medidas sólo locales, principalmente en la evaluación en la respuesta clínica general y tasas de respuesta al tratamiento1.
Otras estudios han comunicado que el tratamiento con doxorrubicina, influiría significativamente en la supervivencia global y estadio libre de enfermedad1,2.
Las esperanzas en el pronóstico del CIM, están enfocadas en lograr métodos diagnósticos en estadios tempranos y nuevas alternativas terapéuticas, fundamentalmente para intervenir sobre las características moleculares del CIM mediante nuevos estudios1,2.
REFERENCIAS
1. Robertson F, Bondy M, Yang W, Yamauchi H, Wiggins S, Kamrudin S et al. Inflammatory breast cancer. The disease, the biology, the treatment. CA Cancer J Clin 2010; 60:351-75.
2. Peña J, Gómez A, Medina S, Muñoz J, Pezzetti L, Pacheco J. Cáncer inflamatorio de la mama: aspectos clínicos y tratamiento. Rev Venez Oncol 2006; 18:158-66.
3. Acea B. Carcinoma in situ, cáncer de mama en el varón y carcinoma inflamatorio. En: Parrilla P, García J, ed: Cirugía AEC. Madrid: Editorial Médica Panamericana, 2010; 1009-16.
4. Sandra M. Swain, et al. Clinical Aspects of Inflammatory Breast Cancer, Janice M. Walshe and, Breast Disease 22 (2005,2006) 35-44 35.
5. Dawood S, Merajver S, Viens P, Vermeulen P, Swain S, Buchholz T et al. International expert panel on inflammatory breast cancer: consensus statement for standardized diagnosis and treatment. Ann Oncol 2011; 22: 515-23.
6. Garantías explícitas en Salud. Guía Clínica Cáncer de mama en personas de 15 años y más. Santiago: Ministerio de Salud; 2011.
7. Peralta O. Cáncer de mama en Chile. Datos epidemiológicos. Rev Chil Obstet Ginecol 2002; 67: 439-45.
8. Anderson W, Chu K, Chang S. Inflammatory breast cancer and non inflammatory locally advanced breast carcinoma: Distinct clinic pathologicentities?. J Clin Oncol 2003; 21:2254-59.
9. Hance K, Anderson W, Devesa S, Young H, Levine P. Trends in inflammatory breast carcinoma incidence and survival: the surveillance, epidemiology, and end results program at the National Cancer Institute. J Natl Can Inst 2005; 97: 966.
10. Merajver S, Hales D. Pathology and molecular pathogenesis. 2012; 12 Up to date.
11. Alunni J, et al. Imaging inflammatory breast cancer. Diagnostic and Interventional Imaging. 2012; 93: 95-103.
12. Walshe J, Swain M. Clinical Aspects of Inflammatory Breast Cancer. Breast Disease. 2006; 22: 35-44.
13. Woodward W, Cristofanilli M. Inflammatory Breast Cancer. Semin Radiat Oncol. 2009; 19: 256-65.
14. Taghian A, Merajver S. Inflammatory breast cancer: Clinical features and treatment. 2012; 5
15. Malcolm R, Morrow M. Surgical Aspects of Inflammatory Breast Cancer. Breast Disease. 2006; 22: 67-73.
16. Wang J, Zhang Q, Zhou R, Chen B, Ouyang J. High-dose chemotherapyfollowed by autologous stem cell transplantation as a first-line therapy for high-risk primary breast cancer: a meta-analysis. PLoS One. 2012; 7: e33388.
17. Mego M, Gao H, Reuben J. Prognostic Value of EMT-Circulating Tumor Cells in Metastatic Breast Cancer Patients Undergoing High-Dose Chemotherapy with Autologous Hematopoietic Stem Cell Transplantation. J Cancer. 2012; 3: 369-80.
18. Dawood S, Ueno N, Cristofanilli M. The Medical Treatment of inflammatory Breast Cancer. Seminars in Oncology 2008; 35: 64-71.
19. Semiglazov V, Eiermann W, Zambetti M, Manikhas A, Bozhok A, Lluch A, et al. Surgery following neoadjuvant therapy in patients with HER2-positive locally advanced or inflammatory breast cancer participating in the NeOAdjuvant Herceptin (NOAH) study. EJSO. 2011; 37: 856-863.
20. Singletary E. Surgical Management of Inflammatory Breast Cancer. Seminars in Oncology 2008; 35: 72-7.
21. Curcio L, Rupp E, Williams W, Chu D, Clarke K, Odom-Maryon T, et al. Beyond palliative mastectomy in inflammatory breast cancer a reassessment of margin status. Ann Surg Oncol. 1999; 6: 249-54.
22. Hidar S, Bibi M, Hidar S. Sentinel lymph node biopsy after neoadjuvant chemotherapy in inflammatory breast cancer. Int J Surg 2009; 7: 272-5.
23. Bristol I, Woodward W, Strom E, Cristofanilli M, Domain D, Singletary S, et al. Locoregional treatment outcomes after multimodality management of inflammatory breast cancer, Int J Radiat Oncol Biol Phys. 2008.1; 72: 474-4.
24. Bear H, Tang G, Rastogi P, Geyer C, Robidoux A, Atkins J, et al. Bevacizumab Added to Neoadjuvant Chemotherapy for Breast Cancer, N Engl J Med 2012; 366: 310-20.
25. Cristofanilli M, Johnston S, Manikhas A, Gomez H, Gladkov O, Shao Z, et al. A randomized phase II study of lapatinib + pazopanib versus lapatinib in patients with HER2+ inflammatory breast cancer. Breast Cancer Res Treat 2013; 137: 471-82.
26. Boussen H, Cristofanilli M, Zaks T, DeSilvio M, Salazar V, Spector N. Phase II study to evaluate the efficacy and safety of neoadjuvant lapatinib plus paclitaxel in patients with inflammatory breast cancer. J Clin Oncol. 2010 28: 3248-55.
27. Overmoyer B. Inflammatory Breast Cancer: Novel Preoperative Therapies, Clinical Breast Cancer. Clin Breast Cancer. 2010; 10: 27-32
28. Molckovsky A, Fitzgerald B, Freedman O, Heise R, Clemons M. Approach to inflammatory breast cancer. Can Fam Physician 2009; 55: 25-31.